适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2016年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2016年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2016年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2016年')}}上传日期:2016-05-11题数:12
提示:单击题文可显示答案与解析。
题号:3138788
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】酸在溶剂中的电离实质是酸中的H
+转移给溶剂分子,如HCl + H
2O = H
3O
+ + Cl
-。已知H
2SO
4和HNO
3在冰醋酸中的电离平衡常数Ka
1(H
2SO
4)=6.3×10
-9,Ka(HNO
3)=4.2×10
-10。 下列说法正确的是
| A.冰醋酸中H2SO4的电离方程式:H2SO4+ 2CH3COOH = SO42-+ 2CH3COOH2+ |
| B.H2SO4的冰醋酸溶液中:c(CH3COOH2+) =c(HSO4-)+ 2c(SO42-)+c(CH3COO-) |
| C.浓度均为0.1mol·L-1的H2SO4或HNO3的冰醋酸溶液:pH(H2SO4)>pH(HNO3) |
D.向HNO3的冰醋酸溶液中加入冰醋酸,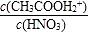 减小 减小 |
题号:3138789
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图。下列说法
错误的是

| A.Cu为负极 |
| B.PbO2电极的电极反应式为:PbO2+ 4H++ SO42-+ 2e-= PbSO4+ 2H2O |
| C.甲中应补充硫酸 |
| D.当消耗1 mol PbO2,需分离出2 mol CuSO4 |
题号:3138790
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】下列实验中,现象和对应结论均正确的是
选项
| 实 验
| 现 象
| 结 论
|
A
| T℃时,向NaCl和NaBr的混合溶液中滴加AgNO3溶液
| 先出现白色沉淀
| T℃时,Ksp:
AgCl<AgBr
|
B
| 向等浓度的Na2CO3溶液或Na2SO4溶液中滴加酚酞试剂
| Na2CO3溶液变红色Na2SO4溶液无明显现象
| 非金属性:S>C
|
C
| 常温下,取饱和CaSO4溶液或氨水做导电性实验
| 氨水实验的灯泡较亮
| CaSO4和NH3·H2O均为弱电解质
|
D
| 向品红溶液中滴加NaClO溶液或通入SO2气体
| 品红溶液均褪为无色
| 两者均有漂白性且
原理相同
|
题号:3138791
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】X、Y、Z、W均为短周期元素,原子序数依次增大。Y原子的M电子层有1个电子,同周期的简单离子的半径中Z最小。W与X同主族,其最高化合价是最低负化合价绝对值的3倍。下列说法正确的是
| A.最高价氧化物水化物的碱性:Y < Z | B.简单气态氢化物的热稳定性:X < W |
| C.X分别与Z、W形成化合物的熔点:Z < W | D.简单离子的还原性:X < W |
题号:3138792
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】某有机物X的结构简式为

,下列说法错误的是
| A.X难溶于水 |
| B.X的分子式为C11H14O2 |
| C.组成为—C4H9的烃基有3种 |
| D.X能发生加成反应、取代反应 |
题号:3138793
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】N
A代表阿伏伽德罗常数的值,下列说法正确的是
| A.0.1molCl2溶于足量水中,转移的电子数为0.1NA |
| B.标准状况下, 11.2LCH3CH2OH的分子数为0.5NA |
| C.0.1mol由16O2和18O2组成的氧气中含有氧原子的数目为0.2NA |
| D.1L0.5mol·L-1Na2SO4溶液中阴离子所带电荷数为NA |
题号:3138794
题型:选择题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】下列有关化学与生活的说法错误的是
| A.铁粉、生石灰均可作食品抗氧化剂 |
| B.明矾、氯化铁均可作净水剂 |
| C.牛奶、鸡蛋清均可用于重金属中毒解毒 |
| D.碘酒、双氧水均可用于伤口消毒 |
题号:3138787
题型:实验题
难易度:一般
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】乙二硫醇(HSCH
2CH
2SH)是一种难溶于水的精细化工产品,熔点- 41℃,沸点 144℃,具有弱酸性。实验室以硫脲和1,2—二溴乙烷为原料制取乙二硫醇钠的合成路线如下:

制备装置如图26-1所示(加热和夹持装置已略)。

回答下列问题:
(1)取适量硫脲于三口瓶中,加入乙醇,加热溶解,再加入1,2—二溴乙烷。一段时间后,有烃基异硫脲盐析出。冷凝管的作用
。使用仪器a而不用普通分液漏斗的优点是
。
(2)过滤,得到烃基异硫脲盐晶体。从滤液中回收乙醇的操作是
。
(3)仍使用图26-1的装置,将烃基异硫脲盐晶体和适量NaOH溶液加热1.5小时,冷却,再加入稀H
2SO
4即可得乙二硫醇。
①加入稀H
2SO
4生成乙二硫醇的化学方程式为
。
②从反应后的混合物中分离乙二硫醇的操作是
。
③此时使用该装置有一个明显缺陷,改进的措施是
。
(4)理论上,制取9.4 g乙二硫醇(M=94g·mol
-1)的同时可以制得NaBr
g。
(5)NaBr和Na
2SO
4的溶解度随温度的变化如图26-2所示。简述从废液中提取Na
2SO
4的方法:
。
(6)为了证明乙二硫醇中含有碳元素,某同学取少量的乙二硫醇充分燃烧,并将生成的气体通入澄清石灰水中。该同学认为发现石灰水变浑浊即可证明。该同学的做法是错误的,理由是
。
题号:3138784
题型:填空题
难易度:困难
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】芳香族化合物A(C
8H
4O
3)是化工中的重要原料,尤其用于增塑剂的制造。A与对苯二酚经脱水可合成1,4—二羟基蒽醌。以A和乙烯为原料,通过如下路线,可以合成塑化剂DBP。



回答下列问题:
(1)A的结构简式为
。
(2)C中不含氧官能团的名称为
。
(3)由B生成D的过程中,涉及的反应类型有
(填序号)。
a.取代反应 b.加成反应 c.消去反应 d.还原反应
(4)写出D与A反应合成DBP的化学方程式
。
(5)X是D的同分异构体,其
1H核磁共振谱图中有2组峰。写出X的结构简式
。
(6)A与异辛醇(

)反应可以制得另一种塑化剂DEHP。参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线。
。
题号:3138785
题型:填空题
难易度:较难
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】三氯氢硅(SiHCl
3)是生产多晶硅的主要原料。由粗硅制三氯氢硅的反应如下:

回答下列问题:
(1)写出SiHCl
3的结构式
。
(z) SiHCl
3,在NaOH溶液中剧烈反应放出H
2,该反应的化学方程式为
。
(3)硅的平衡转化率与投料比n(HCl)/n(Si)的关系如右图,则图中温度T
1、T
2、T
3的大小顺序为
。

(4)平衡时,c(SiHCl
3)/c(SiCl
4)的值
a随着c(H
2)/c(HCl)的值b的变化而变化。则

=
(用含K
l、K
2的代数式表示);根据关系式,工业上用H
2适当稀释HCl来提高SiHCl
3的纯度。 请用平衡移动原理加以解释
。
(5)也可用H
2还原SiCl
4来制取SiHCl
3。300℃时该反应的热化学方程式为
题号:3138786
题型:填空题
难易度:较难
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】以某铬矿石(主要成分是Cr
2O
3,含FeO、SiO
2等杂质)为原料生产Cr
2O
3的流程如下:

已知:Cr
2O
72-+H
2O

2CrO
42-+2H
+,K
sp[Cr(OH)
3] =6.4×10
-31,lg2 = 0.3
(1)步骤Ⅰ中为了提高反应速率应该采取的措施有
、
。(写2种)
(2)滤液1中的阴离子除CO
32-外,主要还有
、
。
(3)步骤Ⅳ发生的反应中Cr
2O
72-和蔗糖(C
12H
22O
11)的物质的量之比为
。
(4)步骤Ⅴ中为了使Cr
3+完全沉淀[此时,c(Cr
3+)≤10
-5mol·L
-1],pH至少调至
。
(5)滤液3的主要溶质是两种盐,化学式为
、
。
(6)研究发现,固态Na
2CrO
4与氨气在500℃下反应得到NaCrO
2,将NaCrO
2溶解后通入CO
2得到更为纯净的Cr(OH)
3。则NaCrO
2溶液与过量CO
2反应的离子方程式为
。
题号:4302140
题型:填空题
难易度:较难
日期:2016-05-11
来源:2016届福建省泉州市高中毕业班3月质量检查理综化学试卷(带解析)
【题文】氨是重要的化工原料,用途广泛。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+ 和CH3COO-构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是 。
②醋酸二氨合铜所含元素的单质,所属的晶体类型有 (填序号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期中,基态原子与基态Cu原子未成对电子数目相同的元素有 种(不含Cu)。
④铜单质为面心立方晶体,其晶胞边长a nm。列式表示铜单质的密度 g·cm-3。
(2)BF3气体与NH3相遇立即生成一种白色晶体:BF3 + NH3=F3B—NH3。
①晶体F3B—NH3中,B原子的杂化轨道类型为 。
②写出两种与BF3具有相同空间构型的阴离子 、 。
(3)NH3可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N4H4(SO4)2的物质。该物质在水溶液中以SO42-和N4H44+两种正四面体构型的离子存在。N4H44+遇碱生成一种形似白磷的N4分子。
①下列相关说法中,正确的是 (填序号)。
a.N4是N2的同分异构体
b.1 mol N4分解生成N2,形成了4 mol π键
c.白磷的沸点比N4高,是因为P—P键键能比N—N键大
d.白磷的化学性质比N2活泼,说明P的非金属性比N强
②画出N4H44+的结构(标明其中的配位键) 。
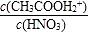 减小
减小
 ,下列说法错误的是
,下列说法错误的是 制备装置如图26-1所示(加热和夹持装置已略)。
制备装置如图26-1所示(加热和夹持装置已略)。



 )反应可以制得另一种塑化剂DEHP。参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线。
)反应可以制得另一种塑化剂DEHP。参照D的上述合成路线,设计一条由D为起始原料制备异辛醇的合成路线。

 = (用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度。 请用平衡移动原理加以解释 。
= (用含Kl、K2的代数式表示);根据关系式,工业上用H2适当稀释HCl来提高SiHCl3的纯度。 请用平衡移动原理加以解释 。
 2CrO42-+2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3
2CrO42-+2H+,Ksp[Cr(OH)3] =6.4×10-31,lg2 = 0.3