适用年级:{{getGradeNameByProperty('高一|期末考试|吉林|2015年')}} 试卷类型:{{getTestPaperTypeName('高一|期末考试|吉林|2015年')}} 使用省份:{{getAreaName('高一|期末考试|吉林|2015年')}}
试卷年份:{{getYear('高一|期末考试|吉林|2015年')}}上传日期:2015-09-11题数:26
提示:单击题文可显示答案与解析。
题号:3153757
题型:选择题
难易度:较难
日期:2016-03-30
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a
-的电子层结构与氦相同,b和c的次外层有8个电子,c
-和d
+的电子层结构相同。下列叙述错误的是
| A.元素的非金属性次序为c>b>a |
| B.a和其他3种元素均能形成共价化合物 |
| C.d和其他3种元素均能形成离子化合物 |
| D.元素a 、b、c各自最高和最低化合价的代数和分别为0、4、6 |
题号:3197310
题型:选择题
难易度:困难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】可逆反应①X(g)+2Y(g)

2Z(g)②2M(g)

N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示(隔板两侧反应室温度相同)。下列判断正确的是:

| A.反应①的正反应是吸热反应 |
| B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15 |
| C.达平衡(I)时X的转化率为5/11 |
| D.在平衡(I)和平衡(II)中M的体积分数相同 |
题号:3197311
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】将1molCO和1molNO
2充入密闭容器中,在催化剂存在下发生反应NO
2(g)+CO(g)

CO
2(g)+NO(g),并达到化学平衡,发现有50%的CO转化为CO
2。在其它条件不变的情况下,若将1molCO和2molNO
2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO
2的体积分数是
题号:3197312
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应 X(g)+Y(g)

2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:
t/min
| 2
| 4
| 7
| 9
|
n(Y)/mol
| 0.12
| 0.11
| 0.10
| 0.10
|
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10
-3mol·L
-1·min
-1B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
题号:3197313
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】将H
2(g)和Br
2(g)充入恒容密闭容器,恒温下发生反应H
2(g)+Br
2(g)

2HBr(g)△H<0,平衡时Br
2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br
2(g)的转化率为b。a与b的关系是
题号:3197314
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】下列生产或实验事实引出的相应结论不正确的是
| 事实
| 结论
|
A
| 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短
| 当其他条件不变时,升高反应温度,化学反应速率加快
|
B
| 工业合成氨中,将氨气液化分离
| 可以加快反应速率,提高N2、H2的转化率
|
C
| FeCl3+3KSCN Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体 溶液颜色加深 Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体 溶液颜色加深
| 恒温时增大反应物浓度,平衡向正反应方向移动
|
D
| A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快
| 当其他条件不变时,催化剂可以改变化学反应速率
|
题号:3197315
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl—KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO
4+2LiCl+Ca===CaCl
2+Li
2SO
4+Pb。下列有关说法正确的是

| A.正极反应式:Ca+2Cl--2e-===CaCl2 |
| B.放电过程中,Li+向负极移动 |
| C.每转移0.1 mol电子,理论上生成20.7 g Pb |
| D.常温时,在正负极间接上电流表或检流计,指针不偏转 |
题号:3197317
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】甲醇燃料电池(DMFC)可用于汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质溶液是稀硫酸。电池工作时,甲醇被氧化为二氧化碳和水。下列叙述中不正确的是
A.负极的反应式为CH3OH+H2O-6e-===CO2↑+6H+
B.氧气在电极上的反应是O2+4H++4e-===2H2O
C.电池工作时,H+由正极移向负极
D.电池工作时,电子从通入甲醇的一极流出,经外电路流入通入氧气的一极
题号:3197318
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍,A和B分别是
A.Si和Na B.B和H C.Cl和C D.C和Al
题号:3197319
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】在容积不变的密闭容器中发生反应2NO
2 (g)

2NO(g)+O
2(g),能说明该反应已达化学平衡状态的是
①生成n mol O
2的同时生成2n mol NO
2 ②生成n mol O
2的同时生成2n mol NO
③v(NO
2)∶v(NO)∶v(O
2)=2∶2∶1 ④混合气体的颜色不再改变
⑤混合气体的密度不再改变 ⑥混合气体的平均相对分子质量不再改变
题号:3197320
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】 X、Y、Z、M、N代表五种金属,有以下化学反应:
(1)水溶液中X+Y
2+===X
2++Y;
(2)Z+2H
2O(冷水)===Z(OH)
2+H
2↑;
(3)M、N为电极,与N盐溶液组成原电池,M电极反应为M-2e
-===M
2+;
(4)Y可以溶于稀硫酸中,M不被稀硫酸氧化。
则这五种金属的活动性由弱到强的顺序是
| A.M<N<Y<X<Z | B.N<M<X<Y<Z | C.N<M<Y<X<Z | D.X<Z<N<M<Y |
题号:3197321
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】已知在25 ℃、101 kPa下,1 g C
8H
18(l)燃烧生成CO
2和液态H
2O时放出48.40 kJ的热量,表示上述反应的热化学方程式正确的是
A.C8H18(l)+ O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1 O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1 |
B.C8H18(l)+ O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1 O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1 |
C.C8H18(l)+ O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1 O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1 |
| D.2C8H18(l)+25O2(g)===16CO2(g)+18 H2O(l)ΔH=-5 517.6 kJ·mol-1 |
题号:3197322
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】下图是恒温下某反应的化学反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是

| A.反应达平衡时,正反应速率和逆反应速率相等 |
| B.该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ |
| C.该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ |
| D.同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
题号:3197323
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】已知反应4CO+2NO
2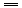
N
2+4CO
2在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
| A.v(CO)=1.5 mol·L-1·min-1 | B.v(NO2)=0.7 mol·L-1·min-1 |
| C.v(N2)=0.4 mol·L-1·min-1 | D.v(CO2)=1.1 mol·L-1·min-1 |
题号:3197324
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】100mL 4mol/L 稀硫酸与2g锌粒反应,在一定温度下为了减缓反应的速率,但又不影响生成氢气的总量,可向反应物中加入
| A.硫酸钠固体 | B.硫酸铜固体 | C.硝酸钾溶液 | D.氯化钠溶液 |
题号:3197325
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】下列关于原电池的叙述正确的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.原电池是将化学能转变为电能的装置 |
| C.在原电池中,电子流出的一极是负极,该电极被还原 |
| D.原电池放电时,电流的方向是从负极到正极 |
题号:3197326
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】下列说法中正确的是
| A.KOH中含有离子键也含有共价键,属于离子化合物 |
| B.HCl中存在离子键,属于离子化合物 |
| C.含有共价键的化合物一定是共价化合物 |
| D.阴、阳离子间通过静电引力而形成的化学键叫做离子键 |
题号:3197327
题型:选择题
难易度:一般
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】下列关于催化剂的说法正确的是
| A.使用催化剂可以增大正反应速率,减小逆反应速率 |
| B.使用催化剂可以使化学平衡正向移动 |
| C.使用催化剂可以降低反应的活化能 |
| D.使用催化剂可以改变反应的平衡常数 |
题号:3467090
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)

Z(g)+W(s) △H>0,下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的△H增大 |
题号:3467091
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】已知:2H
2(g)+O
2(g)===2H
2O(l) ΔH=-571.6 kJ·mol
-12CH
3OH(l)+3O
2(g)===2CO
2(g)+4H
2O(l) ΔH=-1452 kJ·mol
-1H
+(aq)+OH
-(aq)===H
2O(l) ΔH=-57.3 kJ·mol
-1下列说法正确的是
| A.H2(g)的燃烧热为571.6 kJ·mol-1 |
B. H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)=== Ba(OH)2(aq)=== BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| C.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| D.3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1 |
题号:3467092
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】常温下,1 mol化学键断裂成气态原子所需消耗的能量用E表示。结合表中信息判断下列说法不正确的是
共价键
| H—H
| F—F
| H—F
| H—Cl
| H—I
|
E(kJ·mol-1)
| 436
| 157
| 568
| 432
| 298
|
A.432 kJ·mol
-1>E(H—Br)>298 kJ·mol
-1B.表中最稳定的共价键是H—F键
C.H
2(g)―→2H(g) ΔH=+436 kJ·mol
-1D.H
2(g)+F
2(g)="==2HF(g)" ΔH=-25 kJ·mol
-1
题号:3467093
题型:选择题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】室温下,将1 mol的CuSO
4·5H
2O(s)溶于水会使溶液温度降低,热效应为ΔH
1;将1 mol的CuSO
4(s)溶于水会使溶液温度升高,热效应为ΔH
2;CuSO
4·5H
2O受热分解的化学方程式为CuSO
4·5H
2O(s)

CuSO
4(s)+5H
2O(l),热效应为ΔH
3。则下列判断正确的是
| A.ΔH2>ΔH3 | B.ΔH1<ΔH3 |
| C.ΔH1+ΔH3=ΔH2 | D.ΔH1+ΔH2>ΔH3 |
题号:3197308
题型:实验题
难易度:困难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】(12分)(1)已知H
+(aq)+OH
-(aq)===H
2O(l) ΔH=-57.3 kJ·mol
-1。若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q
1kJ、Q
2kJ、Q
3kJ。则三者的由小到大关系是________(用Q
1、Q
2、Q
3表示)。
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是_____________; 若实验中不加盖泡沫塑料板,则求得的中和热数值
(填偏大、偏小、无影响)。

(3)实验室用50mL 0.50mol·L
-1盐酸、50mL 0.55mol·L
-1NaOH溶液利用上图装置,进行测定中和热的实验。假设盐酸和氢氧化钠溶液的密度都是1 g/cm
3,又知中和后生成溶液的比热容c=4.18 J/(g·℃)。为了计算中和热,实验时还需测量的数据有(填序号)________。
| A.反应前盐酸的温度 |
| B.反应前盐酸的质量 |
| C.反应前氢氧化钠溶液的温度 |
| D.反应前氢氧化钠溶液的质量 |
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号
| 起始温度t1/℃
| 终止温度t2/℃
|
盐酸
| 氢氧化钠溶液
| 混合溶液
|
1
| 20.0
| 20.1
| 23.4
|
2
| 20.2
| 20.4
| 23.6
|
3
| 20.5
| 20.6
| 23.8
|
依据该学生的实验数据计算,该实验测得的中和热ΔH为________。(保留三位有效数字)
题号:3197306
题型:填空题
难易度:困难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】(14分)I.在500 ℃、2×10
7 Pa和催化剂条件下合成氨工业的核心反应是:N
2(g)+3H
2(g)

2NH
3(g) ΔH=Q kJ·mol
-1。反应过程中能量变化如图所示,回答下列问题:

(1)在500 ℃、2×10
7Pa和催化剂条件下向一密闭容器中充入0.5 mol N
2和1.5 mol H
2,充分反应后,放出的热量_____(填“<”“>”或“=”)46.2 kJ,理由是_____________。
(2)将一定量的H
2(g)和N
2(g)放入1 L密闭容器中,在500 ℃、2×10
7 Pa下达到平衡,测得N
2为0.10 mol,H
2为0.30 mol,NH
3为0.10 mol。则该条件下达到平衡时H
2的转化率为________。该温度下的平衡常数K的值为________。若升高温度,K值________(填“增大”“减小”或“不变”)。
II.一定条件下,某容积为1L的密闭容器中发生如下反应:C(s) + H
2O(g)

CO(g) + H
2(g)
(1)维持温度不变,向该容器中充入2 mol C(s)和2 mol H
2O(g),达到平衡后混合气体的平均分子量为M,则M的范围为
。
(2)在(1)中若起始时充入的是2.5 molCO(g)和4molH
2(g),达到平衡后混合气体的平均相对分子质量为
。
题号:3197307
题型:填空题
难易度:困难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】(8分) 有部分元素的性质与原子(或分子)结构如下表:
元素编号
| 元素性质与原子(或分子)结构
|
T
| 最外层电子数是次外层电子数的3倍
|
X
| 常温下单质为双原子分子,分子中含有3对共用电子对
|
Y
| M层比K层少1个电子
|
Z
| 第三周期元素的简单离子中半径最小
|
(1)写出元素T的原子结构示意图:_____________________。
(2)元素Y与元素Z相比,金属性较强的是________(用元素符号表示)。下列表述中能证明这一事实的是________(填序号)。
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈
d.Y最高价氧化物对应的水化物的碱性比Z强
(3)写出T与Y形成的化合物的化学式_______________,________________。
(4)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式:__________________。
题号:3197309
题型:填空题
难易度:较难
日期:2015-09-11
来源:【百强校】2014-2015学年吉林省实验中学高一下学期期末化学试卷(带解析)
【题文】(12分)如图是某同学设计的一个简易的原电池装置,回答下列问题。

(1)若a为镁、b为CuCl
2,则正极材料为_____,负极上的电极反应式为_________。
(2)若a为镁、b为NaOH,则Mg极上发生________反应(填“氧化”或“还原”),负极上的电极反应式为_______________。
(3)若a为铜、b为浓硝酸,则电流的方向为____→___(填电极材料),正极上的电极反应式为______。
(4)上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑________。
 2Z(g)②2M(g)
2Z(g)②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示(隔板两侧反应室温度相同)。下列判断正确的是:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示(隔板两侧反应室温度相同)。下列判断正确的是:
 CO2(g)+NO(g),并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是
CO2(g)+NO(g),并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是



 2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表: 2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是 Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体 溶液颜色加深
Fe(SCN)3+3KCl平衡体系中加入少量KSCN固体 溶液颜色加深
 2NO(g)+O2(g),能说明该反应已达化学平衡状态的是
2NO(g)+O2(g),能说明该反应已达化学平衡状态的是 O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1
O2(g)===8CO2(g)+9H2O(g)ΔH=-48.40 kJ·mol-1 O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l)ΔH=-5 517.6 kJ·mol-1 O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1
O2(g)===8CO2(g)+9H2O(g) ΔH=+5 517.6 kJ·mol-1
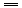 N2+4CO2在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
N2+4CO2在不同条件下的化学反应速率如下,其中表示的反应速率最快的是 Z(g)+W(s) △H>0,下列叙述正确的是
Z(g)+W(s) △H>0,下列叙述正确的是 H2SO4(aq)+
H2SO4(aq)+ Ba(OH)2(aq)===
Ba(OH)2(aq)=== BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是
 2NH3(g) ΔH=Q kJ·mol-1。反应过程中能量变化如图所示,回答下列问题:
2NH3(g) ΔH=Q kJ·mol-1。反应过程中能量变化如图所示,回答下列问题:
 CO(g) + H2(g)
CO(g) + H2(g)