适用年级:{{getGradeNameByProperty('高一|高考真卷|全国|2010年')}} 试卷类型:{{getTestPaperTypeName('高一|高考真卷|全国|2010年')}} 使用省份:{{getAreaName('高一|高考真卷|全国|2010年')}}
试卷年份:{{getYear('高一|高考真卷|全国|2010年')}} 上传日期:2010-06-29 题数:12
题号:3439864
题型:选择题
难易度:容易
日期:2012-08-07
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】能在溶液中大量共存的一组离子是
A.NH4 + 、Ag+ 、PO4 3- 、Cl- B.Fe3+ 、H+ 、I- 、HCO3 - C.K+ 、Na+ 、NO3 - 、4 - D.Al3+ 、Mg2+ 、SO4 2- 、CO3 2-
题号:3502573
题型:选择题
难易度:容易
日期:2010-06-15
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】下列物质中既有氧化性又有还原性的是
A.HClO B.Al2 O3 C.N2 03 D.SiO2
题号:3571152
题型:选择题
难易度:容易
日期:2010-06-10
来源:2010年高考化学试题分项专题五 氧化还原反应
题号:3807934
题型:选择题
难易度:容易
日期:2012-09-06
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】亚氨基锂(Li
2 NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li
2 NH+H
2 Li
2 NH+LiH,下列有关说法正确的是
A.Li2 NH中N的化合价是 B.该反应中H2 既是氧化剂又是还原剂 C. D.此法储氢和钢瓶储氢的原理相同
题号:3815319
题型:选择题
难易度:一般
日期:2012-12-24
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】下列实验设计及其对应的离子方程式均正确的是
A.用FeCl3 溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+ B.Na2 O2 与H2 O反应制备O2 :Na2 O2 + H2 O= 2Na+ + 2OH- + O2 ↑ C.将氯气溶于水制备次氯酸:Cl2 + H2 O= 2H+ + Cl- + ClO- D.用浓盐酸酸化的KMnO4 溶液与H2 O2 反应,证明H2 O2 具有还原性:
2MnO
+ 6H
+ + 5H
2 O
2 = 2Mn
2+ + 5O
2 ↑ + 8H
2 O
题号:3439875
题型:实验题
难易度:容易
日期:2010-06-11
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】(16分)某科研小组用MnO
2 和浓盐酸制备Cl
2 时,利用刚吸收过少量SO
2 的NaOH溶液对其发扬进行吸收处理。
(1)请完成SO
2 与过量NaOH溶液反应的化学方程式:SO
2 +2NaoH=_____________。
(2)反应Cl
2 +Na
2 SO
3 +2NaOH="2NaCl" + Na
2 SO
4 +H
2 O中的还原剂为______________________-。
(3)吸收尾气一段时间后,吸收液(强碱性)吵肯定存在Cl
- 、OH
- 和SO
4 2- 。请设计实验,探究该吸收液中可能存在的其它离子(
不考虑 空气的CO
2 的影响)
①提出合理假设
假设1:只存在SO
3 2- 假设2:既不存在SO
3 2- 也不存在ClO
- 假设3:_______
______
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL
L
-1 H
2 SO
4 、1moL
L
-1 NaOH、0.01mol
L
-1 KMnO
4 、淀粉-KI溶液、紫色石蕊试液.
实验步骤 预期现象和结论 步骤1:取少量吸收液于试管中,滴加3 moL-1 H2 SO4 至溶液呈酸性,然后将所得溶液分置于A、B试管中 步骤2: 步骤3:
题号:3807943
题型:实验题
难易度:容易
日期:2010-06-09
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】(13分)某研究性学习小组在网上收集到如下信息:
溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】制作银镜,并与
溶液反应,发现银镜溶解。
(1)下列有关制备银镜过程的说法正确的是
。
a. 边振荡盛有2%的
溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为止
b.将几滴银氨溶液滴入2ml乙醛中
c.制备银镜时,用酒精灯的外焰给试管底部加热
d.银氨溶液具有较弱的氧化性
e.在银氨溶液配置过程中,溶液的pH增大
【提出假设】
假设1:
具有氧化性,能氧化Ag。
假设2:
溶液显酸性,在此酸性条件下
能氧化Ag。
【设计实验方案,验证假设】
(2)甲同学从上述实验的生成物中检验出
,验证了假设1的成立。请写出
氧化Ag的离子方程式:
。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
【思考与交流】
(4)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结论:
溶液中的
和
都氧化了Ag。你是否同意丙同学的结论,并简述理由:
。
题号:3891916
题型:实验题
难易度:容易
日期:2010-06-15
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】(16分)
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO
3 )是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。请回答下列问题:
(1)碘是
(填颜色)固体物质,实验室常用
方法来分离提纯含有少量杂
质的固体碘。
(2)电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I
2 +6KOH=5KI+KIO
3 +3H
2 O,将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。电解时,阳极上发生反应的电极反应式为
;阴极上观察到的实验现象是
。
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I
— 。请设计一个检验电解液中是否有I
— 的实验方案,并按要求填写下表。
要求:所需药品只能从下列试剂中选择,实验仪器及相关用品自选。
试剂:淀粉溶液、碘化钾淀粉试纸、过氧化氢溶液、稀硫酸。
(4)电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
步骤②的操作名称是
,步骤⑤的操作名称是
。步骤④洗涤晶体的目的是
。
题号:4380606
题型:实验题
难易度:容易
日期:2010-06-15
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】(15分)某兴趣小组用题27图装置探究氨的催化氧化.
(1)氨催化氧化的化学方程式为___________________.
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”).
(3)为保证在装置4中观察到红棕色气体,装置3应装入_________;若取消3,在4中仅观察到大量白烟,原因是___________________.
(4)为实现氨催化氧化,也可用装置5替换装置_________(填装置代号);化合物X为_________(只写一种),Na
2 O
2 的作用是___________________.
题号:3571162
题型:填空题
难易度:容易
日期:2010-06-10
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】(12分)正极材料为
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
(1)橄榄石型
是一种潜在的锂离子电池正极材料,它可以通过
、
与
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
①共沉淀反应投料时,不将
和
溶液直接混合的原因是
。
②共沉淀反应的化学方程式为
。
③高温成型前,常向
中加入少量活性炭黑,其作用除了可以改善成型后的
的导电性能外,还能
。
(2)废旧锂离子电池的正极材料试样(主要含有
及少量AI、Fe等)可通过下列实验方法回收钴、锂。
① 在上述溶解过程中,
被氧化成
,
在溶解过程中反应的化学方程式为
。
②
在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为
。(填化学式);在350~400℃范围内,剩余固体的成分为
。(填化学式)。
题号:3576306
题型:填空题
难易度:一般
日期:2010-06-11
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO
3 ,并含少量的Fe
2 O
3 、FeCO
3 MgO、CaO等,生产工艺流程示意如下:
(1) 将菱锌矿研磨成粉的目的是_____。
(2) 完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)
2 +□____+□_____==□Fe(OH)
3 +□CI
- (3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液2”的ph时,理论上可选用的最大区间为______。
Mg(OH)2 Zn(OH)2 MgCO3 CaCO3 开始沉淀的pH 10.4 6.4 — — 沉淀完全的pH 12.4 8.0 — — 开始溶解的pH — 10.5 — — Ksp 5.6× — 6.8× 2.8×
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
题号:4380648
题型:填空题
难易度:一般
日期:2010-06-11
来源:2010年高考化学试题分项专题五 氧化还原反应
【题文】向盛有KL溶液的试管中加入少许
后滴加氯水,
层
变成紫色。如果继续向试管中滴加氯水,振荡,
层会逐渐变浅,最后变成无色。
完成下列填空:
1) 写出并配平
层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
2)整个过程中的还原剂是___。
3)把KL换成KBr,则
层变为__色:继续滴加氯水,
层的颜色没有变化。
、
、
氧化性由强到弱的顺序是______。
4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含
的食盐)1000kg,若庄Kl与
反应制
,至少需要消耗
________L(标准状况,保留2位小数)。
 MnO4-
MnO4- 不能自发进行,则该反应的
不能自发进行,则该反应的
 、
、 、
、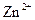 的氧化性依次减弱
的氧化性依次减弱 Li2NH+LiH,下列有关说法正确的是
Li2NH+LiH,下列有关说法正确的是
 和
和 的离子半径相等
的离子半径相等 + 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O 假设2:既不存在SO32-也不存在ClO-
假设2:既不存在SO32-也不存在ClO- ______
______ L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液. L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中
L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中
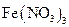 溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究: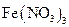 溶液反应,发现银镜溶解。
溶液反应,发现银镜溶解。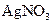 溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为止
溶液的试管,边滴入2%的氨水,至最初的沉淀恰好溶解为止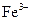 具有氧化性,能氧化Ag。
具有氧化性,能氧化Ag。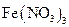 溶液显酸性,在此酸性条件下
溶液显酸性,在此酸性条件下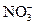 能氧化Ag。
能氧化Ag。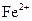 ,验证了假设1的成立。请写出
,验证了假设1的成立。请写出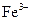 氧化Ag的离子方程式: 。
氧化Ag的离子方程式: 。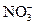 在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
在不同条件下的还原产物较复杂,有时难以观察到气体产生)。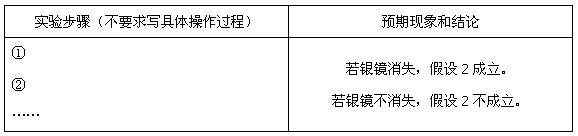
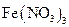 溶液中的
溶液中的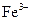 和
和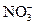 都氧化了Ag。你是否同意丙同学的结论,并简述理由: 。
都氧化了Ag。你是否同意丙同学的结论,并简述理由: 。
 质的固体碘。
质的固体碘。


 的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。
的锂离子电池已被广泛用作便携式电源。但钴的资源匮乏限制了其进一步发展。 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 、
、 与
与 溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。 和
和 溶液直接混合的原因是 。
溶液直接混合的原因是 。 中加入少量活性炭黑,其作用除了可以改善成型后的
中加入少量活性炭黑,其作用除了可以改善成型后的 的导电性能外,还能 。
的导电性能外,还能 。 及少量AI、Fe等)可通过下列实验方法回收钴、锂。
及少量AI、Fe等)可通过下列实验方法回收钴、锂。
 被氧化成
被氧化成 ,
, 在溶解过程中反应的化学方程式为 。
在溶解过程中反应的化学方程式为 。 在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。
在空气中加热时,固体残留率随温度的变化,如下图所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为 。(填化学式);在350~400℃范围内,剩余固体的成分为 。(填化学式)。




 后滴加氯水,
后滴加氯水, 层
层 变成紫色。如果继续向试管中滴加氯水,振荡,
变成紫色。如果继续向试管中滴加氯水,振荡, 层会逐渐变浅,最后变成无色。
层会逐渐变浅,最后变成无色。
 层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
 层变为__色:继续滴加氯水,
层变为__色:继续滴加氯水, 层的颜色没有变化。
层的颜色没有变化。  、
、 、
、 氧化性由强到弱的顺序是______。
氧化性由强到弱的顺序是______。 的食盐)1000kg,若庄Kl与
的食盐)1000kg,若庄Kl与 反应制
反应制 ,至少需要消耗
,至少需要消耗 ________L(标准状况,保留2位小数)。
________L(标准状况,保留2位小数)。