分【题文】联苄(
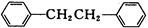
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH
2CH
2Cl)为原料,在无水AlCl
3催化下加热制得,其制取步骤为:
(一)催化剂的制备:下图是实验室制取少量无水AlCl
3的相关实验装置的仪器和药品:
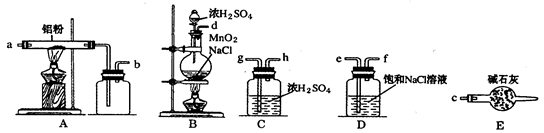
(1)将上述仪器连接成一套制备并保存无水AlCl
3的装置,各管口标号连接顺序为:d接e,_______接_______,_________接________,_________接________。
(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl
3。你认为这样做是否可行__________(填“可行”或“不可行”),你的理由是________________。
(3)装置A中隐藏着一种安全隐患,请提出一种改进方案:_____________。
(二)联苄的制备
联苄的制取原理为:

反应最佳条件为n(苯) :n(1,2-二氯乙烷)=10 :1,反应温度在60-65℃之间。
实验室制取联苄的装置如下图所示(加热和加持仪器略去):

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl
3,由滴液漏斗滴加10.7 mL1,2-二氯乙烷,控制反应温度在60-65℃,反应约60min。将反应后的混合物依次用稀盐酸、2%Na
2CO
3溶液和H
2O洗涤分离,在所得产物中加入少量无水MgSO
4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2 g。
相关物理常数和物理性质如下表
名称
| 相对分子质量
| 密度/(g•cm-1)
| 熔点/℃
| 沸点/℃
| 溶解性
|
苯
| 78
| 0.88
| 5.5
| 80.1
| 难溶水,易溶乙醇
|
1,2-二氯乙烷
| 99
| 1.27
| -35.3
| 83.5
| 难溶水,可溶苯
|
无水氯化铝
| 133.5
| 2.44
| 190
| 178(升华)
| 遇水水解,微溶苯
|
联苄
| 182
| 0.98
| 52
| 284
| 难溶水,易溶苯
|
(4)仪器a的名称为______________,和普通分液漏斗相比,使用滴液漏斗的优点是_________。
(5)洗涤操作中,水洗的目的是_____________;无水硫酸镁的作用是______________。
(6)常压蒸馏时,最低控制温度是________________。
(7)该实验的产率约为______________。(小数点后保留两位有效数字)
 Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-=Cl-(aq),若将光源移除,电池会立即恢复至初始状态。下列说法不正确的是
Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-=Cl-(aq),若将光源移除,电池会立即恢复至初始状态。下列说法不正确的是
 Ag (s) +Cu2+ (aq)+Cl-(aq)
Ag (s) +Cu2+ (aq)+Cl-(aq)
 可能大于
可能大于
 溶液中,
溶液中,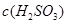 大于
大于
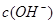 不断增大
不断增大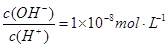 ,则该溶液中由水电离出的
,则该溶液中由水电离出的
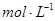

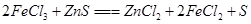 ,则氯化铁与FeS反应的方程式为 。
,则氯化铁与FeS反应的方程式为 。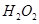 、
、 ,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。
,但生产成本高。酸性条件下,使用催化剂在50℃左右通入氧气转化的成本极低,反应的离子方程式为 。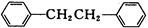 )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:


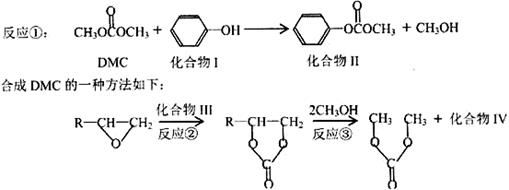
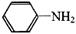 与DMC 以物质的量之比为1∶1发生类似反应①的反应,请写出该反应的化学方程式 。
与DMC 以物质的量之比为1∶1发生类似反应①的反应,请写出该反应的化学方程式 。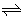 COS(g)+H2(g)
COS(g)+H2(g)

 Sn2-
Sn2- 2NH3(g)+O2(g) △H1=-272.9 kJ·mol-1, 2H2(g)+O2(g)═2H2O(g) △H2= -483.6kJ·mol-1,则4NH3(g)+5O2(g)="4NO(g)+" 6H2O(g)△H3= 。
2NH3(g)+O2(g) △H1=-272.9 kJ·mol-1, 2H2(g)+O2(g)═2H2O(g) △H2= -483.6kJ·mol-1,则4NH3(g)+5O2(g)="4NO(g)+" 6H2O(g)△H3= 。 2NH3(g) △H4 =" -" 92. 4 kJ·mol-1,
2NH3(g) △H4 =" -" 92. 4 kJ·mol-1,
 CO(NH2)2(g)+H2O(g)有影响。T℃时,在一定体积为2L的恒容密闭容器中,将物质的量之和为3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数。[n(NH3)/n(CO2)] 时,尿素产量最大;该条件下反应的平衡常数K= 。
CO(NH2)2(g)+H2O(g)有影响。T℃时,在一定体积为2L的恒容密闭容器中,将物质的量之和为3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数。[n(NH3)/n(CO2)] 时,尿素产量最大;该条件下反应的平衡常数K= 。