【题文】【化学——选修3:物质结构与性质】金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度。其单质和化合物具有广泛的应用价值。氮化钛(Ti
3N
4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl
4为原料,经过一系列反应可以制得Ti
3N
4和纳米TiO
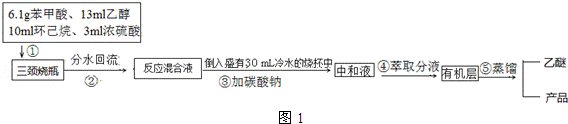
2(如图1)。
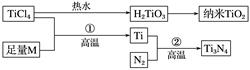
图1
上图中的M是短周期金属元素,M的部分电离能如下表:
| I1
| I2
| I3
| I4
| I5
|
电离能/kJ·mol-1
| 738
| 1451
| 7733
| 10540
| 13630
|
请回答下列问题:
(1)Ti的基态原子外围电子排布式为________________;
(2)M是______(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为________;
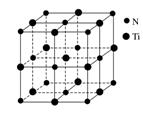
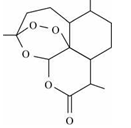
(3)纳米TiO
2是一种应用广泛的催化剂,纳米TiO
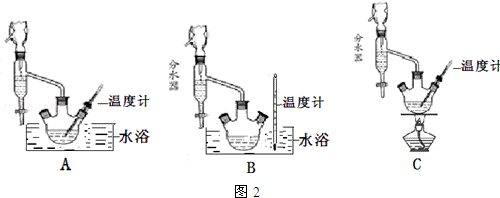
2催化的一个实例如图2所示。化合物甲的分子中采取sp
2方式杂化的碳原子有__________个,化合物乙中采取sp
3方式杂化的原子对应的元素的电负性由大到小的顺序为________________;
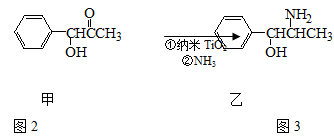
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为
a pm,则该氮化钛的密度为______________ g·cm
-3(
NA为阿伏加德罗常数的值,只列计算式)。该晶体中与N原子距离相等且最近的N原子有________个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据如下:
离子晶体
| NaCl
| KCl
| CaO
|
晶格能/kJ·mol-1
| 786
| 715
| 3401
|
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为________________。


 +C2H5OH
+C2H5OH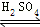
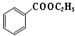 +H2O
+H2O




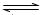 2H2(g)+S2(g) △H
2H2(g)+S2(g) △H 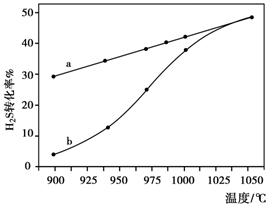
 CO(g)+H2(g)K1
CO(g)+H2(g)K1 CO2(g)+ H2(g) K2
CO2(g)+ H2(g) K2 CaCO3(s) K3
CaCO3(s) K3 CaCO3(s)+2H2(g)的K= 。(用K1、K2、K3表示)
CaCO3(s)+2H2(g)的K= 。(用K1、K2、K3表示) CaCO3(s) +2H2(g),△H=" -87.9" kJ·mol-1;采取以下措施可以提高H2产量的是 。(填字母编号)
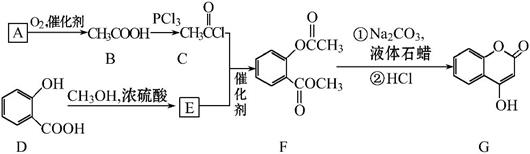
CaCO3(s) +2H2(g),△H=" -87.9" kJ·mol-1;采取以下措施可以提高H2产量的是 。(填字母编号)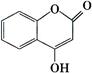 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成: