适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2012年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2012年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2012年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2012年')}}上传日期:2012-03-14题数:21
提示:单击题文可显示答案与解析。
题号:3190777
题型:选择题
难易度:一般
日期:2015-12-01
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】为了配制NH
4+浓度与Cl
-的浓度比为1:1的溶液,可在NH
4Cl溶液中加入①适量的HCl;②适量的NaCl;③适量的氨水;④适量的NaOH,正确的是
题号:3297486
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】 100 mL pH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如图所示。下列说法正确的( )
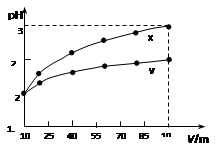
| A.x为弱酸,y为强酸 |
| B.稀释前x、y的物质的量浓度相等 |
| C.随着稀释的进行,y的电离程度减小 |
| D.等体积的x、y分别分别与足量的锌反应,y放出的氢气多 |
题号:3297488
题型:选择题
难易度:较难
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】能正确表示下列反应的离子方程式是( )
A.二氧化锰与浓盐酸加热反应:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
B.纯碱与水反应:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| C.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D.碳酸氢钠与氢氧化钠溶液反应:H++OH-= H2O |
题号:3297489
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】
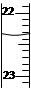
| A.将FeCl3溶液加热至沸腾,溶液由黄色变为红褐色 |
| B.滴定达终点时,右图滴定管的正确读数为23.65 mL |
| C.向AgI悬浊液中滴加少量NaCl溶液,沉淀转化为白色 |
| D.测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
题号:3297490
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】某元素的3p原子轨道中有2个未成对电子,因此其( )
| A.第三电子层上有4个电子 |
| B.最高正价为+2 |
| C.最高正价为+4 |
| D.第二电子层没有未成对电子 |
题号:3297491
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】多电子原子中,原子轨道能量高低排列错误的是( )5.
| A.2s<3s<4s | B.2px<2py<2pz |
| C.3s<3p<3d | D.2px=2py=2pz |
题号:3297492
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
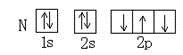
【题文】下列轨道表示式表示的原子基态(能量最低状态)核外电子排布正确的( )
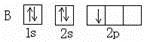
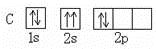
A B
C D
题号:4339167
题型:选择题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】下列叙述中,能证明某物质是弱电解质的是( )
| A.水溶液的导电能力很弱 |
| B.稀溶液中已电离的离子和未电离的分子共存 |
| C.在水溶液中,存在分子 |
| D.熔化状态时不导电 |
题号:4339168
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】常温下,下列溶液中
c(H
+)发来呀最小的是
| A.c(OH-)=1×10-11mol·L-1 | B.pH=3的CH3COOH溶液 |
| C.pH=4的H2SO4溶液 | D.c(H+)=1×10-3mol·L-1 |
题号:4339169
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
题号:4339170
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】下列说法正确的是( )
| A.因为p轨道是“8”字形的,所以p电子走“8”字形 |
| B.第三电子层,有3s、3p、3d三个轨道 |
| C.氢原子中只有一个电子,故氢原子只有一个轨道 |
| D.原子轨道与电子云都是用来形象描述电子运动状态的 |
题号:4339171
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
题号:4339172
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】甲、乙、丙、丁四种易溶于水的物

质,分别由NH
4+、Ba
2+、Mg
2+、H
+、OH
-、Cl
-、HCO
3-、SO
42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H
+)>0.1mol/L;③ 向丙溶液中滴入AgNO
3溶液有不溶于稀HNO
3的白色沉淀生成。下列结论不正确的是 ( )
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- | C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
题号:4339173
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
题号:4339174
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】已知如下物质的溶度积常数:FeS:Ksp=6.3×10
-18mol
2·L
-2;CuS:Ksp="1.3×" 10
-36mol
2·L
-2。 下列说法正确的是 ( )
| A.同温度下,CuS的溶解度大于FeS的溶解度 |
| B.同温度下,向饱和FeS溶液中呈入少量Na2S固体后,Ksp(FeS)变小 |
C.向含有等物质的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出现
的沉淀是FeS |
| D.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
题号:4339175
题型:选择题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】下列说法不正确的是( )
| A.0.2 mol·L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
| B.将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 |
| C.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+) = c(Cl-) |
| D.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
题号:3297483
题型:填空题
难易度:较难
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】(9分)镁是一种轻金属,其合金强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得”国防金属”的美誉。海水矿物质中镁的浓度仅次于氯和钠,居第三位。由于对镁的需求非常巨大,很多沿海国家都建有大型海水提镁工厂。
下表是有关物质的K
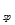
:
回答下列问题:
(1)能否直接把贝壳研磨成粉末,撒入海水中使
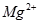
转化为
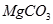
沉淀,并解释原因:
。
(2)实际生产中是把
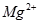
转化为
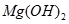
沉淀,而不是转化为
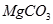
沉淀,其理由是
;请你推测应将贝壳进行怎样的加工处理
。
(3)某同学在实验室条件下模拟该生产过程,在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他
(填”能”或”不能”)将
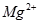
转化为
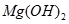
沉淀,理由是
。
题号:3297484
题型:填空题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】 (Ⅰ)(9分)
现有下列物质: ①NaCl晶体 ②液态SO
2 ③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C
2H
5OH) ⑦熔化的KCl ⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)在上述状态下能导电的物质是
;
(2)属于弱电解质的是
;
(3)属于非电解质,但溶于水后的水溶液能导电的是
;
(Ⅱ)现有下列电解质溶液:①
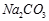
②
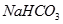
③
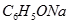
④
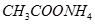
⑤
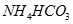
(已知酸性
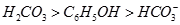
。)
(1)在这五种电解质溶液中,既能与盐酸又能与烧碱溶液反应的是(填写序号)
。
(2)常温下,物质的量浓度相同的①、②、③溶液pH大小顺序为(填序号)
>
>
。
(3)写出⑤与足量NaOH溶液混合加热时反应的离子方程式
。
题号:3297485
题型:填空题
难易度:一般
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】(16分)(Ⅰ)某元素的原子序数为33,写出该元素原子的核外电子排布式 ,此元素的原子中被电子占据的轨道有 个,有 个能级(能量不同的轨道);
(Ⅱ)有五种元素A、B、C、D、E,A2+的电子层结构为1S22S22P63S23P63d5,B原子的M层为最外层且有两个未成对电子,C原子的L电子层的P轨道上有一个空轨道,D原子的L电子层的P轨道上只有一对成对电子,E原子的M电子层的P轨道半充满。写出A---E各元素的符号:A 、B 、C 、D 、E
题号:4339176
题型:填空题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】(7分)氯气在295K、100Kpa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有三分之一与水反应。请回答下列问题:
(1)该反应的离子方程式为 ;
(2)估算该反应的平衡常数 (写计算结果)
(3)在上述平衡体系中加入少量NaOH固体,平衡将向 移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将______(填“增大”、“减小”或“不变”),平衡将向______________移动。
题号:4339177
题型:填空题
难易度:
日期:2012-03-14
来源:2011-2012学年福建省四地六校高二下学期第一次联考化学试卷
【题文】 (11分)根据废水中所含有害物质的不同,工

业上有多种废水的处理方法。

(1)①废水I若采用CO
2处理,离子方程式是
。
②废水Ⅱ常用明矾处理。实践中发现废水中的c(HCO
-3)越大,净水效果越好,这是因为
。
③废水III中的汞元素存在如下转化:
Hg
2++ CH
4 =CH
3Hg
++H
+,我国规定,Hg
2+的排放标准不能超过0.05 mg/L。若某工厂排放的废水1 L中含Hg
2+ 3×10
-7mo1,是否达到了排放标准
(填“是”或“否”)。
④废水Ⅳ常用C1
2氧化CN
-成CO
2和N
2,若参加反应的C1
2与CN
-的物质的量之比为5:2,则该反应的离子方程式
。
(2)化学需氧量(COD)可量度水体受有机物污染的程度,它是指在一定条件下,用强氧化剂处理水样时所消耗的氧化剂的量,换算成氧的含量(以mg/L计)。某研究性学习小组测定某水样的化学需氧量(COD),过程如下:
I.取V
1mL水样于锥形瓶,加入10.00 mL 0.2500 mol/L K
2Cr
2O
7溶液。
II.加碎瓷片少许,然后慢慢加入硫酸酸化,混合均匀,加热。
III.反应完毕后,冷却,加指示剂,用c mol/L硫酸亚铁铵[(NH
4)
2Fe(SO
4)
2]溶液滴定。终点时消耗硫酸亚铁铵溶液V
2 mL。
①I中,量取K
2Cr
20
7溶液的仪器是
。(酸式滴定管或碱式滴定管)
②Ⅱ中,碎瓷片的作用是
。
③III中,发生的反应为:Cr
2O
2-7+6Fe
2++14 H
+=2Cr
3++6Fe
3++7H
2O
由此可知,该水样的化学需氧量COD=
(用含c、V
1、V
2的表达式表示)。
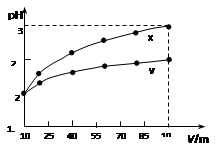
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O H2CO3+2OH-
H2CO3+2OH-

 A B
A B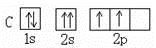
 H3O++OH-
H3O++OH- H++HS-
H++HS- Na++HS-
Na++HS- H3O++CO32-
H3O++CO32- HCOO— + H3O+
HCOO— + H3O+ HCO3— + H+
HCO3— + H+ HCO3— + OH—
HCO3— + OH—
 S2— + H3O+
S2— + H3O+ 质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是 ( )
质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;② 0.1mol/L乙溶液中c(H+)>0.1mol/L;③ 向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。下列结论不正确的是 ( )  义的水解观认为:无论是盐
义的水解观认为:无论是盐 的水解还是非盐的水解,其最终结果是发生水解的物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法不正确的是 ( )
的水解还是非盐的水解,其最终结果是发生水解的物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法不正确的是 ( ) 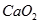 的水解产物是
的水解产物是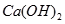 和
和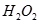
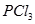 的水解产物是HClO和
的水解产物是HClO和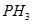
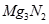 的水解产物是两种碱性物质
的水解产物是两种碱性物质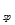 :
: 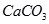
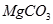
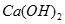
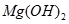
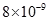
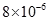
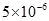
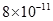
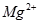 转化为
转化为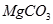 沉淀,并解释原因: 。
沉淀,并解释原因: 。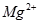 转化为
转化为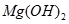 沉淀,而不是转化为
沉淀,而不是转化为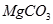 沉淀,其理由是 ;请你推测应将贝壳进行怎样的加工处理 。
沉淀,其理由是 ;请你推测应将贝壳进行怎样的加工处理 。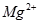 转化为
转化为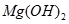 沉淀,理由是 。
沉淀,理由是 。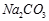 ②
②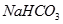 ③
③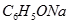 ④
④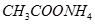 ⑤
⑤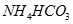 (已知酸性
(已知酸性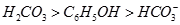 。)
。) 业上有多种废水的处理方法。
业上有多种废水的处理方法。