适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2014年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2014年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2014年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2014年')}}上传日期:2014-10-28题数:20
提示:单击题文可显示答案与解析。
题号:3232117
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】(10分)A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、 Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。现做如下实验:
①A和E的溶液显碱性,0.1mol/L A溶液的pH小于13;
②在B的溶液中逐滴加入盐酸有白色沉淀生成
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断部分A~E物质的化学式:
A ,C 。
(2)D的阳离子的结构示意图是 ;E的阴离子的电子式是 。
(3)写出③、④的离子方程式:
③ ;
④ 。
题号:3232118
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:
a HClO
3 = bO
2↑+ c Cl
2↑+ d HClO
4 + e H
2O。下列有关说法不正确的是
| A.由反应可确定:氧化性HClO3>O2 |
| B.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O |
| C.由非金属性Cl>S,可推知酸性HClO3>H2SO4 |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
题号:3232119
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】用0.2 mol/L Na
2SO
3溶液32 mL,还原含2×10
-3 mol X
2O
72-的溶液,过量的Na
2SO
3用0.1 mol/L KMnO
4酸性溶液氧化(其中KMnO
4被还原成Mn
2+),共消耗KMnO
4溶液1.6 mL,则元素X在还原产物中的化合价是
题号:3232120
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】有下列三个氧化还原反应
①2FeCl
3+2KI=2KCl+2FeCl
2+I
2 ②2Fe+3Cl
2=2FeCl
3 ③2KMnO
4+16HCl=2KCl+2MnCl
2+5Cl
2↑+8H
2O
若某溶液中有Fe
2+、I
-和Cl
-共存,要氧化除去I
-而不影响Fe
2+和Cl
-,可加入的试剂是 ( )
题号:3232121
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】
| A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B.用100 mL容量瓶配制90mL1mol/L的NaOH溶液 |
| C.用pH试纸测得新制氯水的pH为2 |
| D.用酸式滴定管准确量取10.00mLKMnO4溶液 |
题号:3232122
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】能正确表示下列反应的离子反应方程式为
| A.大理石溶于醋酸溶液: CaCO3 + 2H+==Ca2+ + CO2↑+ H2O |
| B.向FeBr2溶液中通入足量氯气:2Fe2+ + 4Br- + 3Cl2===2Fe3+ + 2Br2 + 6Cl- |
| C.NH4HCO3溶于过量的NaOH溶液中:HCO3- + OH-===CO32- + H2O |
| D.向明矾(KAl(SO4)2·12H2O)溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全: |
2Al
3+ + 3SO
42- + 3Ba
2+ + 6OH
-=== 2Al(OH)
3↓ + 3BaSO
4↓
题号:3232123
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】某溶液中大量存在五种离子:NO
3-、SO
42-、Fe
3+、H
+、X,其物质的量之比为:n(NO
3-):n(SO
42-) :n(Fe
3+) :n(H
+) :n (X) =" 2" :3 :1 :3 :1,则X 可能为 ( )
题号:3232124
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】被称为万能还原剂的NaBH
4溶于水并和水发生反应:NaBH
4+2H
2O=NaBO
2+4H
2↑,下列说法中正确的是(NaBH
4中H为-1价)
| A.NaBH4是氧化剂,H2O是还原剂 | B.被氧化的元素与被还原的元素质量比为1︰1 |
| C.硼元素被氧化,氢元素被还原 | D.NaBH4既是氧化剂又是还原剂 |
题号:3232125
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列叙述中,正确的是
| A.金属氧化物都是碱性氧化物 |
| B.含金属元素的离子一定是阳离子 |
| C.金属阳离子被还原不一定得到金属单质 |
| D.某元素从化合态变为游离态时,该元素一定被还原 |
题号:3232126
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的是( )
| A.Mg2+、Na+、SO42-、Cl— | B.K+、CO32-、Cl—、NO3— |
| C.NH4+、Na+、SO42-、NO3— | D.Na+、K+、NO3—、SO32— |
题号:3232127
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】设N
A为阿伏加德罗常数的值,下列叙述中正确的是
| A.1 L 1 mol/L的Na2CO3溶液中含有的CO32-数目为NA |
| B.标准状况下,1.8 g H2O所含有的质子数为NA |
| C.25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2NA |
| D.标准状况下,2.24 L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.2NA |
题号:3232128
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列条件下,两种气体的分子数一定不相等的是
| A.相同体积、相同密度的CO和C2H4 |
| B.相同质量、不同密度的N2和C2H4 |
| C.相同压强、相同体积、相同质量的O2和N2 |
| D.相同温度、相同压强、相同体积的O2和N2 |
题号:3232129
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列有关物质分类或归类正确的一组是
① 酸性氧化物:SO
2、NO、CO
2、SiO
2② 氢氟酸、盐酸、水玻璃、氨水均为混合物
③ 明矾、小苏打、硫酸钡、HClO均为电解质
④ 碘酒、牛奶、豆浆、漂粉精均为胶体
⑤ 液氨、液氯、干冰、碘化银均为化合物
题号:3232130
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】英国物理学家约翰·丁达尔首先发现了入射光透过胶体时,从侧面可以看到一条光亮的通路。下列液体中,不会出现丁达尔效应的分散系的是
①鸡蛋白溶液 ②肥皂水 ③淀粉溶液 ④硝酸钾溶液
题号:4311133
题型:选择题
难易度:较易
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法中正确的是 ( )
| A.在该反应中维生素C作催化剂 |
| B.砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷可能是+3价砷 |
| C.因为河虾中含有砷元素,所以不能食用 |
| D.上述反应中维生素C作氧化剂 |
题号:4311134
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列离子方程式书写正确的是
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| B.一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ |
| C.用氢氧化钠溶液吸收过量二氧化碳 OH-+CO2=HCO3- |
| D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3+ +2I-=2Fe2+ + I2 |
题号:4311135
题型:选择题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】下列装置所示的实验不能达到目的的是
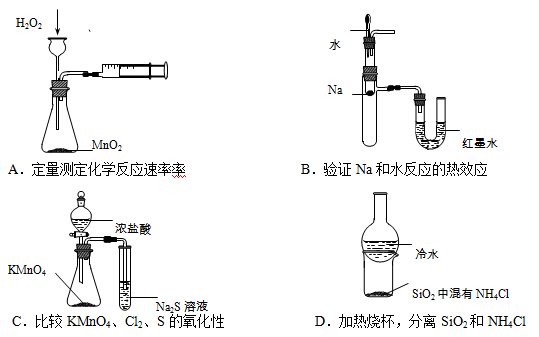
题号:3232114
题型:填空题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】(13分) N元素有多种化合物,它们之间可以发生转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与O电负性较大的是 。
(2)NaN3的晶体类型是 。
(3)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8K,主要原因是 。
(4)N2H4中的N原子的杂化类型是 。
(5)NO2-离子是一种很好的配位体,能提供孤电子对是 。
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式 。
题号:3232115
题型:填空题
难易度:较难
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】(16分)亚氯酸钠(NaClO
2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO
2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO
2•3H
2O。
②纯ClO
2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③80 g·L
-1 NaOH溶液是指80 g NaOH固体溶于水所得溶液的体积为1L。
(1)80 g·L
-1 NaOH溶液的物质的量浓度为
;
(2)发生器中鼓入空气的作用可能是
(选填序号);
a.将SO
2氧化成SO
3,增强酸性 b.将NaClO
3氧化成ClO
2 c.稀释ClO
2以防止爆炸
(3)从“母液”中可回收的主要物质是
;
(4)吸收塔内的反应的化学方程式为
;
吸收塔的温度不能超过20℃,其目的是
;
(5)在碱性溶液中NaClO
2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是
;
(6)吸收塔中为防止NaClO
2被还原成NaCl,所用还原剂的还原性应适中。除H
2O
2外,还可以选择的还原剂是
(选填序号);
a.Na
2S b.Na
2O
2 c.FeCl
2(7) 从吸收塔出来的溶液中得到NaClO
2•3H
2O粗晶体的实验操作依次是
(选填序号)。
a.蒸发浓缩 b.蒸馏 c.过滤 d.灼烧 e.冷却结晶
题号:3232116
题型:填空题
难易度:一般
日期:2014-10-28
来源:2015届福建省四地六校高三上学期第一次月考化学试卷(带解析)
【题文】(13分)已知工业盐中含有NaNO
2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3~0.5g。已知NaNO
2能发生如下反应(方程式已配平):2NO
2-+xI
-+yH
+=2NO↑+I
2+zH
2O,请回答下列问题:
(1)上述反应中,x =________, y =________,z =________,氧化剂是________________。
(2)根据上述反应,鉴别NaNO
2和NaCl可选用的物质有:①碘化钾淀粉试纸、②淀粉、③食醋、④白酒,你认为必须选用的物质有________________(填序号)。
(3)某工厂废切削液中含有2%~5%的NaNO
2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO
2转化为不引起污染的N
2,该物质是________________。
| A.NaCl | B.KMnO4 | C.浓硫酸 | D.NH4Cl |
(4)饮用水中的NO
3- 对人类健康会产生危害,为了降低饮用水中NO
3- 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO
3- 还原为N
2,请配平化学方程式:
10Al+6NaNO
3 + 4NaOH + 18H
2O=□ ________ + 3N
2↑。若反应过程中转移0.5mol电子,则生成标况下的N
2体积为________。
 Fe(OH)3+3H+
Fe(OH)3+3H+
