适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2017年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2017年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2017年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2017年')}} 上传日期:2017-03-30 题数:12
题号:3194607
题型:选择题
难易度:一般
日期:2015-10-23
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】下列说法不正确的是
A.液晶态介于晶体状态和液态之间,液晶具有一定程度的晶体的有序性和液体的流动性 B.常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 C.石油裂解、煤的干馏、玉米制醇、蛋白质的变性和纳米银粒子的聚集都是化学变化 D.燃料的脱硫脱氮、SO2 的回收利用和NOx 的催化转化都是减少酸雨产生的措施
题号:3210323
题型:选择题
难易度:较难
日期:2015-04-17
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】在25℃时,H
2 R及其钠盐的溶液中,H
2 R、HR
- 、R
2- 分别在三者中所占的物质的量分数(α)随溶液pH变化关系如下图所示,下列叙述错误的是
A.H2 R是二元弱酸,其Ka1 =1×10-2 B.当溶液恰好呈中性时,c( Na + )="2c" ( R2- ) + c( HR- ) C.NaHR在溶液中水解倾向大于电离倾向 D.含Na2 R与NaHR各0.1 mol的混合溶液的pH=7.2
题号:3279879
题型:选择题
难易度:一般
日期:2013-01-08
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】a、b、c、d、e分别为MgCl
2 、KHSO
4 、KOH、NaHCO
3 、AlCl
3 五种溶液中的一种,其中a能与其余四种溶液反应,且与c、e反应时有明显的现象;b与d反应只产生气泡;e只能与a反应。下列推理不正确的是( )
A.a一定为KOH B.b一定为KHSO4 C.c一定为AlCl3 D.e一定为MgCl2
题号:3449535
题型:选择题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】溶液的酸碱性可用酸度(AG)表示,
。室温下,将0.0100mol•L
-l 盐酸逐滴滴入20.0mL 0.0100mol•L
-l 氨水中,溶液的AG变化如图所示。下列说法正确的是( )
A.M点以后NH4 + 的水解程度逐渐增大 B.室温下,0. 0100mol•L-l 盐酸的AG =12 C.M点加入盐酸的体积大于20.0 mL D.M点时溶液中:c (NH4 + ) =c (Cl- )
题号:3449536
题型:选择题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】在密闭容器中将2molNaHCO
3 (s)和一定量Na
2 O
2 混合,在加热条件下让其充分反应,150℃下所得气体仅含2种组分,反应后固体的物质的量(
n )的取值范围是( )
题号:3449537
题型:选择题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
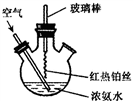
【题文】利用如图所示装置进行下列实验,实验现象与结论均正确的是( )
选项 实验试剂 实验现象 实验结论 a b c A 浓氨水 碱石灰 FeCl2 溶液 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 氨气具有氧化性 B 稀硫酸 FeS AgCl悬浊液 悬浊液由白色变为黑色 K sp (AgCl)>K sp (Ag2 S)C 浓硝酸 铜 BaSO3 悬浊液 悬浊液变澄清 +4价硫具有还原性 D 浓盐酸 KMnO4 紫色石蕊试液 溶液先变红后褪色 Cl2 有酸性和漂白性
A. A B. B C. C D. D
题号:3449538
题型:选择题
难易度:一般
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
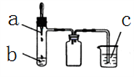
【题文】在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是( )
A.反应后溶液中含有NO3 - B.反应后溶液中c (H+ )增大 C.实验过程中有化合反应发生 D.实验过程中NH3 •H2 O的电离常数不可能发生变化
题号:3449533
题型:实验题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】目前流行的关于生命起源假设的理论认为,生命起源于约40亿年前的古洋底的热液环境。这种环境系统中普遍存在铁硫簇结构,如Fe
2 S
2 、Fe
4 S
4 、Fe
8 S
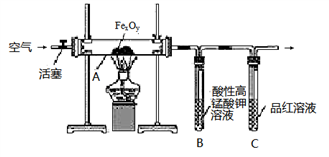
7 等,这些铁硫簇结构参与了生命起源的相关反应。某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验。【实验Ⅰ】硫的质量确定
按图连接装置,检查好装置的气密性后,在硬质玻璃管A中放入1.00 g铁硫簇结构(含有部分不反应的杂质),在试管B中加入50.00 mL 0.1000 mol•L
-1 的酸性KMnO
4 溶液,在试管C中加入品红溶液。通入空气并加热,发现固体逐渐转变为红棕色。待固体完全转化后将B中溶液转移至250 mL容量瓶,洗涤试管B后定容。取25.00 mL该溶液用0.01000 mol•L
-1 的草酸(H
2 C
2 O
4 )进行测定剩余KMnO
4 溶液浓度的滴定。记录数据如下:
滴定次数 待测溶液体积/mL 草酸溶液体积/mL 滴定前刻度 滴定后刻度 1 25.00 1.50 23.70 2 25.00 1.02 26.03 3 25.00 0.00 24.99
相关反应:① 2MnO
4 - + 2H
2 O + 5SO
2 2Mn
2+ + 5SO
4 2- + 4H
+ ② 2MnO
4 - + 6H
+ + 5H
2 C
2 O
4 2Mn
2+ +10CO
2 ↑+ 8H
2 O
【实验Ⅱ】铁的质量确定
将实验Ⅰ硬质玻璃管A中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH溶液,过滤后取滤渣,经充分灼烧得0.600 g固体。
试回答下列问题:
(1)检查“实验Ⅰ”中装置气密性的方法是_______________。
(2)滴定终点的判断方法是______________。
(3)试管C中品红溶液的作用是_______________;有同学提出,撤去C装置,对实验没有影响,你的看法是___(选填“同意”或“不同意”),理由是________________。
(4)根据实验Ⅰ和实验Ⅱ中的数据可确定该铁硫簇结构的化学式为___________________。
【问题探究】
滴定过程中,细心的小明发现该KMnO
4 颜色褪去的速率较平常滴定时要快得多。为研究快的原因,甲同学继续进行了下列实验,实验数据如下表:
编号 温度/℃ 酸化的H2 C2 O4 溶液/mL KMnO4 溶液/mL 溶液褪色时间/s 1 25 5.0 2.0 40 2 25 5.0(另加少量可溶于水的MnSO4 粉末) 2.0 4 3 60 5.0 2.0 25
(5)分析上述数据,滴定过程中反应速率较快的原因可能是_____________。
题号:3311253
题型:填空题
难易度:一般
日期:2011-10-20
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】实验室可由软锰矿(主要成分为MnO2 )制备KMnO4 ,方法如下:软锰矿与过量固体KOH和KClO3 在高温下反应,生成锰酸钾(K2 MnO4 )和KCl;用水溶解,滤去残渣,滤液酸化后,K2 MnO4 转变为MnO2 和KMnO4 ;滤去MnO2 沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4 。请回答: 2 MnO4 的化学方程式是_______________________;2 MnO4 制备KMnO4 的离子方程式是_______________;2 80%)进行上述实验,KMnO4 的理论产量为_______________。4 能与热的经硫酸酸化的Na2 C2 O4 溶液反应生成Mn2+ 和CO2 ,该反应的化学方程式是________________________;4 产品0.165g,恰好与0.335g Na2 C2 O4 反应完全,该KMnO4 的纯度为___。
题号:3449532
题型:填空题
难易度:一般
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】铜是应用较为广泛的有色金属。
(1)基态铜原子的价电子排布式为_____________。
(2)金属化合物Cu
2 Zn合金具有较高的熔点、较大的强度、硬度和耐磨度。则Cu
2 Zn合金的晶体类型是______。
(3)某含铜化合物的离子结构如图所示。
① 该离子中存在的作用力有__________。
a.离子键 b.共价键 c.配位键
d.氢键 e.范德华力
② 该离子中第二周期的非金属元素的第一电离能由大到小的顺序是______。
③ 该离子中N原子的杂化类型有_________。
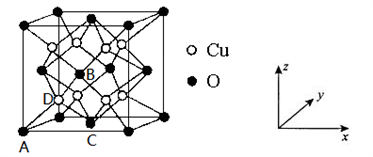
(4)晶胞有两个基本要素:
① 原子坐标参数,表示晶胞内部各原子的相对位置,下图为铜与氧形成的某化合物晶胞,其中原子坐标参数A 为(0,0,0);B为(
,0,
);C为(
,
,0),则D原子的坐标参数为_____________。
② 晶胞参数,描述晶胞的大小和形状,设晶胞的边长为apm,则O的配位数是_______。
题号:3449534
题型:填空题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
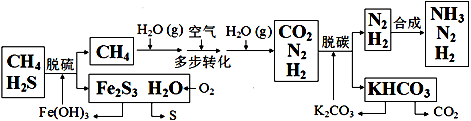
【题文】下图是工业上以天然气、空气为原料合成氨的一种工艺流程:
(1)脱硫反应第一步是利用Fe(OH)
3 除去H
2 S,该反应的化学方程式是____________。
(2)脱硫反应第二步是利用空气氧化回收硫,该反应中氧化剂与还原剂的物质的量之比为_________,下列试剂中也适宜作此反应的氧化剂的是________(填选项)。
A.Cl
2 B.H
2 O
2 C.KMnO
4 D.O
3 (3)流程中Fe(OH)
3 和K
2 CO
3 可循环利用,你认为流程中还可循环利用的物质有_______。
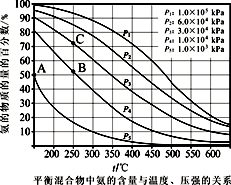
(4)合成氨反应的原料气中V(N
2 )∶V(H
2 )=1∶3。平衡混合物中氨的含量与温度、压强的关系如下图所示:
则A、B、C三点对应的化学平衡常数K
A 、K
B 、K
C 的关系是___________(用“>”、“<”或“=”表示);A点H
2 的平衡转化率为________。
题号:3449531
题型:推断题
难易度:较难
日期:2017-03-30
来源:【全国百强校】福建省福州第一中学2017届高三下学期模考4理科综合-化学试题
【题文】A是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合物;B称作冰片,可用于医药和制香精,樟脑等;C的核磁共振氢谱显示其分子中含有4种氢原子;D中只含一个氧原子,与Na反应放出H
2 ;F为烃。仔细阅读以下转化关系:
回答以下问题:
(1)B的分子式为__________。
(2)B不能发生的反应是___________(填序号)。
a.氧化反应 b.聚合反应 c.消去反应 d.取代反应 e.与Br
2 加成反应
(3)E→F的反应类型是____________。
(4)F的分子式为_________,化合物H是F的同系物,相对分子质量为56,H所有可能的结构有______种。
(5)用系统命名法给F命名的名称为______________。
(6)写出E→D的化学力程式______________。

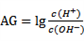 。室温下,将0.0100mol•L-l盐酸逐滴滴入20.0mL 0.0100mol•L-l氨水中,溶液的AG变化如图所示。下列说法正确的是( )
。室温下,将0.0100mol•L-l盐酸逐滴滴入20.0mL 0.0100mol•L-l氨水中,溶液的AG变化如图所示。下列说法正确的是( )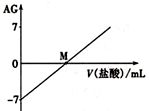
 2Mn2+ + 5SO42- + 4H+
2Mn2+ + 5SO42- + 4H+ 2Mn2+ +10CO2↑+ 8H2O
2Mn2+ +10CO2↑+ 8H2O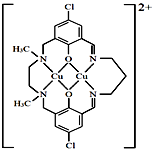
 ,0,
,0, );C为(
);C为( ,
, ,0),则D原子的坐标参数为_____________。
,0),则D原子的坐标参数为_____________。