适用年级:{{getGradeNameByProperty('高二|期末考试|吉林|2014年')}} 试卷类型:{{getTestPaperTypeName('高二|期末考试|吉林|2014年')}} 使用省份:{{getAreaName('高二|期末考试|吉林|2014年')}}
试卷年份:{{getYear('高二|期末考试|吉林|2014年')}}上传日期:2014-01-21题数:24
提示:单击题文可显示答案与解析。
题号:1433472
题型:选择题
难易度:较难
日期:2016-06-24
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】1体积某气态烃和2体积氯化氢发生加成反应后,最多还能和6体积氯气发生取代反应。由此可以断定原气态烃是(气体体积均在相同条件下测定)
题号:3256928
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列说法中,正确的是
| A.两种物质的组成元素相同,各元素的质量分数也相同,则两者一定互为同分异构体 |
| B.分子式为CnH2n的化合物,可能使酸性KMnO4溶液褪色,也可能不使其褪色 |
| C.通式相同,分子组成上相差一个或若干个CH2原子团的化合物,一定互为同系物 |
| D.凡含有苯环的物质都是芳香烃 |
题号:3256929
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】两种气态烃的混合气体共0.5mol,在空气中燃烧得到0.8mol二氧化碳和18g水,关于该混合气体的说法合理的是
| A.一定含甲烷,不含乙烷 | B.一定含乙烷,不含甲烷 |
| C.一定是甲烷和乙烯的混合物 | D.一定含甲烷,不含乙烯 |
题号:3256930
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】分子式C
3H
6Cl
2的氯代烷分子中的一个氢原子被氯原子取代后,可得到两种同分异构体,则C
3H
6Cl
2的名称是
| A.1,3-二氯丙烷 | B.1,1-二氯丙烷 | C.1,2-二氯丙烷 | D.2,2-二氯丙烷 |
题号:3256931
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】已知:25℃时,K
sp[Mg(OH)
2]=5.61×10
-12,K
sp[MgF
2]=7.42×10
-11。下列说法正确的是
| A.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)小 |
| B.25℃时,向Mg(OH)2的澄清饱和溶液中加入少量的NH4Cl固体,c(Mg2+)降低 |
| C.25℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/LNH4Cl溶液中的Ksp小 |
| D.25℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
题号:3256932
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】苯乙烯的结构为
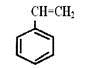
,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有
题号:3256933
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】在C
2H
2、C
6H
6、C
2H
4O组成的混合物中,已知氧元素的质量分数为8%,则混合物中碳元素的质量分数是
题号:3256934
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列化学用语的书写正确的是
| A.乙酸的分子式:C2H4O2 |
| B.乙醇的结构简式:C2H6O |
C.F原子结构示意图: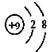 |
D.四氯化碳的电子式: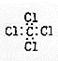 |
题号:3256935
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列有关描述不正确的是
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.常温下,可以用铁或铝制容器盛装浓硫酸和浓硝酸 |
| D.检验某溶液中是否含有SO42-的方法是向该溶液中加入BaCl2溶液,再加入稀HNO3 |
题号:3256936
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】关于铜电极的叙述中不正确的是
| A.铜锌原电池中铜是正极 |
| B.在镀件上镀铜时可用金属铜作阳极 |
| C.用电解法精炼铜时粗铜做阳极 |
| D.用电解法精炼铜时纯铜做阳极 |
题号:3256937
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】在一定条件下,对于A
2(g)+3B
2(g)

2AB
3(g)反应来说,下列所表示的化学反应速率中最大的是
| A.v(A2)=0.8mol·L-1·s-1 | B.v(A2)=40mol·L-1·min-1 |
| C.v(AB3)=1.0mol·L-1·s-1 | D.v(B2)=1.2mol·L-1·s-1 |
题号:3256938
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列三种化合物由左到右是按强电解质、弱电解质、非电解质的顺序排列的一组是
| A.HCl、CaCO3、SO2 | B.KNO3、CH3COOH、NH3 |
| C.HClO、H2S、C2H5OH | D.BaSO4、H3PO4、H2O |
题号:3256939
题型:选择题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列说法正确的是
| A.任何化学反应不一定都有反应热 |
| B.使用催化剂可以改变反应的平衡常数 |
| C.升高温度使反应加快,是因为降低了反应的活化能 |
| D.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
题号:4317760
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列各基态原子或离子的电子排布式错误的是
| A.Al 1s22s22p63s23p1 | B.S2- 1s22s22p63s23p4 |
| C.Na+ 1s22s22p6 | D.F 1s22s22p5 |
题号:4317761
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】检验SO
2气体中是否含有CO
2气体应用的方法是
| A.通过石灰水 | B.先通过酸性KMnO4溶液再通过石灰水 |
| C.通过品红溶液 | D.先通过小苏打溶液再通过石灰水 |
题号:4317762
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】下列叙述正确的是
| A.1.00mol NaCl中含有6.02×1023个NaCl分子 |
| B.1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C.欲配制1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠 |
题号:4317763
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。若以铜为原料制取硫酸铜或硝酸铜,下列设计你认为符合“绿色化学”思想的反应路线(用化学方程式表示)是
| A.制CuSO4:Cu + 2H2SO4(浓) = CuSO4 + SO2↑+ 2H2O |
| B.制CuSO4:2Cu + O2= 2CuO; CuO + H2SO4(稀) = CuSO4 + H2O |
| C.制Cu(NO3)2:Cu + 4HNO3(浓)=Cu(NO3)2 +2NO2↑+ 2H2O |
| D.制Cu(NO3)2:3Cu + 8HNO3(稀)=3Cu(NO3)2 +2NO↑+ 4H2O |
题号:4317765
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】由两种气态烃组成的混合物,体积为10ml。与过量的氧气混合再充分燃烧,将生成物通过浓H
2SO
4气体体积减少15ml,再通过碱石灰气体体积又减少20ml(气体体积均为同温同压下)。混合烃的组成可能为
| A.C2H4和C2H2 | B.C2H6和C2H4 | C.CH4和C3H4 | D.C4H10和C2H4 |
题号:4317766
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】设某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,且X>11,将上述两溶液分别取等体积充分混合,混合液中各离子的浓度由大到小的顺序是
| A.c(Cl-)>c(NH4+)>c(H+) >c(OH-) |
| B.c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| C.c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D.c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
题号:4317767
题型:选择题
难易度:一般
日期:2014-01-22
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】硫酸锶(SrSO
4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
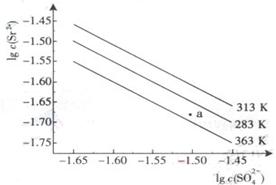
| A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 |
| B.三个不同温度中,363K时Ksp(SrSO4)最大 |
| C.283K时,图中a点对应的溶液是不饱和溶液 |
| D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
题号:3256924
题型:填空题
难易度:一般
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】A、B、C三种强电解质,它们在水中电离出的离子为Na
+、Ag
+、NO
3-、SO
42-、Cl
-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
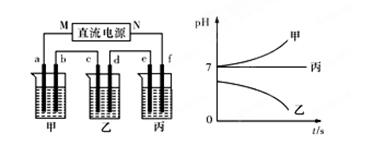
(1)M为电源的
极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为
、
(填写化学式)。
(2)计算电极f上生成的气体在标准状况下体积为
L。
(3)写出乙烧杯中的电解反应方程式:
。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为
。
题号:3256925
题型:填空题
难易度:较难
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物在常温下均呈气态,在周期表中Z与W左右相邻,Y的最高价氧化物的水化物与其氢化物反应生成盐,且Y的核电荷数与W的最外层电子数相同。请回答下列问题:
(1)Z的离子结构示意图是 ;
(2)X、Y、W可组成一化合物,其原子个数之比为4:1:1。其化学式中含有的化学键有 。
(3)YX3分子的空间构型是 ,Z的氢化物的稳定性比W的氢化物的稳定性_____(填“强”或“弱”)。
(4)Z2W2分子中,W与Z均满足8e-稳定结构,则Z 2W2的电子式为 。
题号:3256926
题型:填空题
难易度:较难
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】A~F是中学化学中常见物质,常温下A、C、E、F为气体,B、D为液体,其中B的分子为4原子分子,D在常温下不具有挥发性。F的浓溶液与X共热通常用于实验室制备单质C,X是
一种黑色粉末。这些物质之间满足如下图所示的转化关系,图中部分生成物已略去。
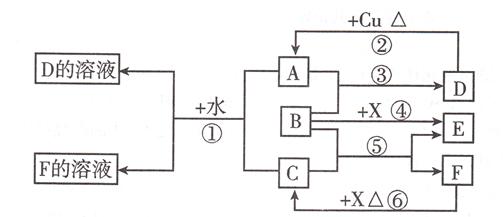
(1)写出下列物质的化学式:A______,F______。
(2)B的电子式是______。根据图中信息,B、C、X的氧化性由强到弱的顺序是_
_____(用化学式表示)。
(3)反应⑥的离子方程式是__
____。
(4)在反应⑥中,F表现的性质是___
____,当生成0.75mol C时,被氧化的还原剂的物质的量是___
____。
题号:3256927
题型:填空题
难易度:较难
日期:2014-01-21
来源:2013-2014学年吉林省白山市第一中学高二上学期期末考试化学试卷(带解析)
【题文】工业上制备BaCl
2的工艺流程图如下:
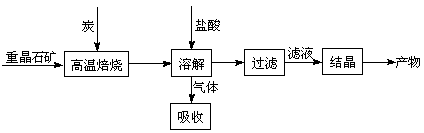
某研究小组在实验室用重晶石(主要成分BaSO
4)对工业过程进行模拟实验。查表得
BaSO
4(s) + 4C(s)

4CO(g) + BaS(s) △H
1 =+571.2 kJ·mol
-1 ①
BaSO
4(s) + 2C(s)

2CO
2(g) + BaS(s) △H
2=+226.2 kJ·mol
-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na
2S水解的离子方程式为
。
(2)向BaCl
2溶液中加入AgNO
3和KBr,当两种沉淀共存时,
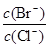
=
。[K
sp(AgBr)=5.4×10
-13,K
sp(AgCl)=2.0×10
-10]
(3)反应C(s) + CO
2(g)

2CO(g)的△H=
kJ·mol
-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是
。
 ,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有
,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有

 2AB3(g)反应来说,下列所表示的化学反应速率中最大的是
2AB3(g)反应来说,下列所表示的化学反应速率中最大的是



 4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ①
4CO(g) + BaS(s) △H1 =+571.2 kJ·mol-1 ① 2CO2(g) + BaS(s) △H2=+226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) △H2=+226.2 kJ·mol-1 ②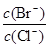 = 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
= 。[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10] 2CO(g)的△H= kJ·mol-1。
2CO(g)的△H= kJ·mol-1。