适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2010年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2010年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2010年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2010年')}} 上传日期:2010-12-07 题数:20
题号:3189538
题型:选择题
难易度:一般
日期:2015-12-14
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】常温下,将0.1 mol·L
-1 氢氧化钠溶液与0.06 mol·L
-1 硫酸溶液等体积混合,该混合溶液的pH等于
题号:3191339
题型:选择题
难易度:较易
日期:2015-11-24
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】分类方法在化学学科的发展中起到重要的作用。下列分类标准合理的是
A.根据纯净物的元素组成,将纯净物分为单质和化合物 B.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质 C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 D.根据反应中的能量变化,将化学反应分为“化合、分解、复分解、置换”四类
题号:4367908
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
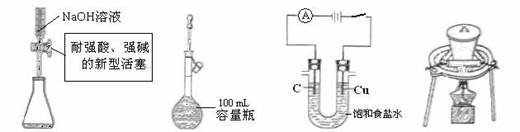
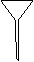
【题文】下列实验操作或装置符合实例实验要求的是
A.量取15.00 mL B.定容 C.电解制Cl2 、H2 D.高温煅烧石灰石.
题号:4367909
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】
A B C D
题号:4367910
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】下列实验操作正确的是
A.用洁净的玻璃棒蘸取试液,点在湿润的pH试纸上测定试液pH B.将称量好的固体直接加入容量瓶中,加水溶解并稀释至刻度,配制成一定物质的量浓度的溶液 C.欲从碘水中分离出I2 ,可将适量的CCl4 加入碘水中振荡静置分层后分液 D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
题号:4367911
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
题号:4367912
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】华裔科学家高琨因“在光纤传输信息领域中的突破性成就”获得2009年诺贝尔物理学奖,下列有关硅材料的说法正确的是
A.光纤的主要成分是高纯度的单质硅 B.刚玉的主要成分是二氧化硅 C.28g硅含有6.02×1023 个电子 D.28 Si、29 Si、30 Si是不同的核素
题号:4367915
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为cmol/L,则下列关
系中不正确的是
A. ρ =" (17V" + 22400) / (22.4 + 22.4V) B. ω =" 17c" / (1000ρ) C. ω =" 17V" / (17V + 22400) D. c =" 1000Vρ" /(17V + 22400)
题号:4367916
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】下图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是
A.根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子 B.该反应类型是分解反应 C.反应生成的丙物质属于单质 D.化学反应中分子的种类发生了改变
题号:4367918
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】完全沉淀等物质的量浓度的NaCl、MgCl
2 、AlCl
3 溶液中的Cl
- ,消耗等物质的量浓度的AgNO
3 溶液的体积比为1:1:1,则上述溶液的体积比为
A.1:1:1 B.3:2:1 C.6:3:2 D.9:3:1
题号:4367919
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
题号:4367920
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】相同体积、相同pH的某一元
强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
题号:4367921
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】下列关于电解质溶液的正确判断是
A.在pH = 12的溶液中,K+ 、Cl- 、HCO3 - 、Na+ 可以常量共存 B.在pH=0的溶液中,Na+ 、NO3 - 、SO3 2 - 、K+ 可以常量共存 C.由0.1 mol·L-1 一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH=B+ +OH- D.由0.1 mol·L-1 一元碱HA溶液的pH=3,可推知NaA溶液存在A- +H2 O
题号:4367922
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】已知:
K sp (AgCl)=1.8×10
—10 ,
K sp (AgI)=1.5×10
—16 ,
K sp (Ag
2 CrO
4 )=2.0×10
—12 ,则下列难溶盐的饱和溶液中,Ag
+ 浓度大小顺序正确的是
A.AgCl>AgI> Ag2 CrO4 B.AgCl> Ag2 CrO4 >AgI C.Ag2 CrO4 >AgCl>AgI D.Ag2 CrO4 >AgI>AgCl
题号:4367923
题型:选择题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】有关①100mL0.1mol/LNaHCO
3 、②100mL0.1mol/LNa
2 CO
3 两种溶液的叙述
不正确 的
是
A.溶液中水电离出的H+ 个数:②>① B.溶液中阴离子的物质的量浓度之和:②>① C.①溶液中:c(CO3 2 - )>c(H2 CO3 ) D.②溶液中:c(HCO3 - )>c(H2 CO3 )
题号:4367926
题型:实验题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】纳米TiO
2 在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO
2 的方法之一是TiCl
4 水解生成TiO
2 ·xH
2 O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO
2 。用氧化还原滴定法测定TiO
2 的质量分数:一定条件下,将TiO
2 溶解并还原为Ti
3+ ,再以KSCN溶液作指示剂,用NH
4 Fe(SO
4 )
2 标准溶液滴定Ti
3+ 至全部生成Ti
4+ 。
请回答下列问题:
⑴ TiCl
4 水解生成TiO
2 ·xH
2 O的化学方程式为_______________________________。
⑵检验TiO
2 ·xH
2 O中Cl
- 是否被除净的方法是______________________________。
(3)配制NH
4 Fe(SO
4 )
2 标准溶液时,加入一定量H
2 SO
4 的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。
a b c d e
⑸滴定终点的现象是___________________________________________________。
⑹滴定分析时,称取TiO
2 (摩尔质量为M g·mol
-1 )试样w g,
消耗c mol·L
-1 NH
4 Fe(SO
4 )
2 标准溶液V mL,则TiO
2 质量分数表达式为_________________________。
题号:4367914
题型:填空题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】硅单质及其化合物应用范围很广。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备纯硅:
Ⅰ.高温下用碳还原二氧化硅制得粗硅
Ⅱ.粗硅与干燥的氯气在450 ℃~500 ℃ 反应制得SiCl
4 Ⅲ. S
iCl
4 液体经精馏提纯后与过量H
2 在1100 ℃~1200 ℃ 反应制得纯硅
已知SiCl
4 沸点为57.6 ℃,能与H
2 O强烈反应。1 mol H
2 与SiCl
4 气体完全反应吸收的热量为120.2 kJ。请回答下列问题:
① 第Ⅰ步制备粗硅的化学反应方程式为
,第Ⅲ步反应的热化学方程式是
。
②整个制备纯硅过程必须严格控制无水无氧。SiCl
4 在潮湿的空气中因水解而产生白色烟雾,其生成物是
;H
2 还原SiCl
4 过程中若混O
2 ,可能引起的后果是
。
(2)二氧化硅大量用于生产玻璃。工业上用SiO
2 、Na
2 CO
3 和CaCO
3 共283 kg在高温下完全反应时放出CO
2 44 kg,生产出的玻璃可用化学式Na
2 SiO
3 ·CaSiO
3 ·
x SiO
2 表示,则其中
x =
。
题号:4367924
题型:填空题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4 C1、FeC13 、N2 、Fe2 O3 、Fe和X。 (写化学式)。 ,反应中4mol的氧化剂能 (填“失去”或“得到”) mol电子. 。
题号:4367925
题型:填空题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH值:
溶质 CH3 COONa NaHCO3 Na2 CO3 NaClO NaCN NaR pH 8.8 9.7 11.6 10.3 11.1 11.3
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH
3 COOH+Na
2 CO
3 ===2CH
3 COONa+CO
2 ↑+H
2 O 若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能成立的是_______________________(填编号)。
A.CO2 +H2 O +2NaClO===Na2 CO3 +2HClO B.CO2 +H2 O +NaClO===NaHCO3 +HClO C.CO2 +H2 O +NaR3 +HR D.CO2 +H2 O +2NaR2 CO3 +2HR
E.Na
2 CO
3 +HR
NaHCO
3 +NaR
F.CH
3 COOH+NaCN===CH
3 COONa+HCN
(2)根据前述信息判断,浓度均为0.05 mol/L的下列六种物质的溶液中,pH最小的是______(填编号); 其pH为___________(
填数值);pH最大的是_________(填编号)。
①HR ②CH
3 COOH ③HCN ④HClO ⑤H
2 SO
4 ⑥HClO
4 (3)一些复分解反应的发生还遵循其它的规律。下列转化都属于复分解反应:
①工业上将石灰乳与纯碱溶液混合可制得苛性钠溶液
②侯氏制碱法中,向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打晶体
③蒸发KCl和NaNO
3 混合溶液,首先析出NaCl晶体
根据上述反应,总结出复分解反应发生的另一规律:______________________;
将KI溶液和AgCl固体混合搅拌,会观察到的现象是_______________________,
请写出反应的离子方程式:____________________________________________。
题号:4367927
题型:填空题
难易度:一般
日期:2010-12-07
来源:2011届福建省厦门外国语学校高三11月月考化学试卷
【题文】用实验确定某酸HA是弱电解质。两同学的方案是: 1(选填>、<、=) (多选扣分)2 的速率快;2 的速率快; 、

 系中不正确的是
系中不正确的是

 的半导体材料
的半导体材料 CaSiO3+CO2↑
CaSiO3+CO2↑  Si + 2CO↑
Si + 2CO↑ 强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是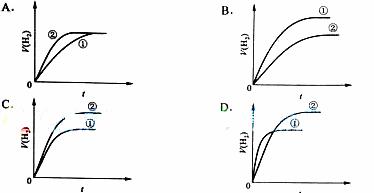
 HA+OH
HA+OH 是
是
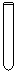
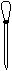
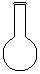
 消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。 iCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
iCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
 。
。 2O +2NaClO===Na2CO3+2HClO
2O +2NaClO===Na2CO3+2HClO NaHCO3+HR
NaHCO3+HR Na2CO3+2HR
Na2CO3+2HR NaHCO3+NaR
NaHCO3+NaR 填数值);pH最大的是_________(填编号)。
填数值);pH最大的是_________(填编号)。