适用年级:{{getGradeNameByProperty('高一|高考真卷|全国|2009年')}} 试卷类型:{{getTestPaperTypeName('高一|高考真卷|全国|2009年')}} 使用省份:{{getAreaName('高一|高考真卷|全国|2009年')}}
试卷年份:{{getYear('高一|高考真卷|全国|2009年')}}上传日期:2010-03-22题数:18
提示:单击题文可显示答案与解析。
题号:3502634
题型:选择题
难易度:一般
日期:2009-11-24
来源:2009高考真题汇编-化学计算
【题文】在5mL 0.05 mo1/L的某金属氯化物溶液中,滴加0.1 mo1/L AgNO
3溶液,生成沉淀质量与加入AgNO
3溶液体积关系如图所示,则该氯化物中金属元素的化合价为:



题号:3571126
题型:选择题
难易度:一般
日期:2012-11-02
来源:2009高考真题汇编-化学计算
【题文】已知:2CO(g)+O
2(g)=2CO
2(g) ΔH=" --" 566 kJ/mol
Na
2O
2(s)+CO
2(g)=Na
2CO
3(s)+ 1/2O
2(g)ΔH=" --226" kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )

| A.CO的燃烧热为283 kJ |
| B.上图可表示由CO生成CO2的反应过程和能量关系 |
| C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH< --452 kJ/mol |
| D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为2×6.02×1023 |
题号:3829560
题型:选择题
难易度:一般
日期:2009-11-17
来源:2009高考真题汇编-化学计算
题号:3891892
题型:选择题
难易度:一般
日期:2009-11-17
来源:2009高考真题汇编-化学计算
【题文】向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。

向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的

沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )

题号:4385780
题型:选择题
难易度:容易
日期:2009-11-17
来源:2009高考真题汇编-化学计算
【题文】将22.4L某气态氮氧化合物与足量的灼热铜粉完全反应后,气体体积11.2L(体积均在相同条件下测定),则该氮氧化合物的化学式为
题号:4385793
题型:选择题
难易度:一般
日期:2013-03-21
来源:2009高考真题汇编-化学计算
题号:4385795
题型:选择题
难易度:一般
日期:2012-11-08
来源:2009高考真题汇编-化学计算
【题文】将15 mL 2 mol·L
-1 Na
2CO
3溶液逐滴加入到40 mL 0.5 mol·L
-1 MCln盐溶液中,恰好将溶液中的M
n+离子完全沉淀为碳酸盐,则MCln中n值是
题号:4385796
题型:选择题
难易度:一般
日期:2013-01-31
来源:2009高考真题汇编-化学计算
【题文】为了检验某含有NaHCO
3杂质的Na
2CO
3样品的纯度,现将w
1 g 样品加热,其质量变为w
2 g ,则该样品的纯度(质量分数)是( )

题号:4385798
题型:选择题
难易度:一般
日期:2010-02-09
来源:2009高考真题汇编-化学计算
【题文】设N
A为阿伏伽德罗常数,下列叙述正确的是( )
| A.24g镁的原子量最外层电子数为NA |
| B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA |
| C.1mol甲烷分子所含质子数为10NA |
| D.标准状况下,22.4L乙醇的分子数为NA |
题号:4385799
题型:选择题
难易度:一般
日期:2010-03-03
来源:2009高考真题汇编-化学计算
题号:4385800
题型:选择题
难易度:一般
日期:2010-03-05
来源:2009高考真题汇编-化学计算
【题文】N
A代表阿伏加德罗常数。下列有关叙述正确的是( )
| A.标准状况下,2.24LH2O含有的分子数等于0.1NA |
B.常温下, 溶液中阴离子总数大于0.1NA 溶液中阴离子总数大于0.1NA |
| C.分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
D.3.4 中含N—H键数目为 中含N—H键数目为 |
题号:3714622
题型:实验题
难易度:一般
日期:2009-11-23
来源:2009高考真题汇编-化学计算
【题文】

某研究性小组借助A-D的仪器装置完成有关实验



【实验一】收集NO气体。
(1)

用装置A收集NO气体,正确的操作上
(填序号)。

a.从①口进气,用排水法集气 b.从①口进气,用排气法集气

c.从②口进气,用排水法集气 d..从②口进气,用排气法集气

【实验二】为了探究镀锌薄铁板上的锌的质量分数

和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na
2ZnO
3+H
2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m
1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。

方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。

(2)选用B和
(填仪器标号)两个装置进行实验。

(3)测得充分反应后生成氢气的体积为VL(标准状况),

=
。

(4)计算镀层厚度,还需要检索的一个物理量是
。

(5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。

方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m
2g 。

(6)

。

方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H
2的质量)实现探究目标。实验同样使用仪器C。

(7)从实验误差角度分析,方案丙
方案乙(填“优于”、“劣于”或“等同于”)。
题号:4385788
题型:实验题
难易度:一般
日期:2013-08-29
来源:2009高考真题汇编-化学计算
【题文】

以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);

(1 )从废液中提纯并结晶处FeSO
4·7H
2O。

(2)将
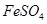
溶液与稍过量的
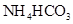
溶液混合,得到含
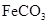
的浊液

(3 )将浊液过滤,用90°C热水洗涤沉淀,干燥后得到
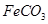
固体

(4)煅烧
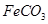
,得到
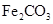
固体

已知:
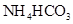
在热水中分解

(1 )中,加足量的铁屑出去废液中的
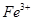
,该反应的离子方程式是

(2)中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用

(3 )中,生成
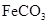
的离子方程式是
。若
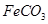
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。

(4)中,通过检验

来判断沉淀是否洗涤干净。检验

操作是是
。

(5)已知煅烧
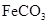
的化学方程式是
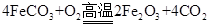
,现煅烧464.0kg
的
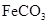
,得到316.8kg产品,若产品中杂质只有

,则该产品中
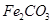
的质量是
kg(摩尔质量/g·
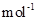
;
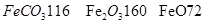
)
题号:3714624
题型:填空题
难易度:一般
日期:2009-12-28
来源:2009高考真题汇编-化学计算
【题文】某厂废水中含5.00×10
-3mol·L
-1的

,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料

(

的化合价依次为+3、+2),设计了如下实验流程:

(1)第①步反应的离子方程式是
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)
3外,还有
(4)欲使1L该废水中的

完全转化为

。理论上需要加入
GFeSO
4·7H
2O。
题号:3895851
题型:填空题
难易度:一般
日期:2009-11-17
来源:2009高考真题汇编-化学计算
【题文】工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是
;NaOH溶液的出口为
(填字母);精制饱和食盐水的进口为
(填字母);干燥塔中应使用的液体是
。

(2)多晶硅主要采用SiHCl
3还原工艺生产,其副产物SiCl
4的综合利用收到广泛关注。
①SiCl
4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl
4与H
2和O
2反应,产物有两种,化学方程式为
。
②SiCl
4可转化为SiHCl
3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl
4(g)+2H
2(g)+Si(s)

4SiHCl
3(g)
达平衡后,H
2与SiHCl
3物质的量浓度分别为0.140mol/L和0.020mol/L,若H
2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为
kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气

(标准状况)。
题号:4385792
题型:填空题
难易度:一般
日期:2009-11-16
来源:2009高考真题汇编-化学计算
【题文】 (10分)联氨(N
2H
4)及其衍生物是一类重要的火箭燃料,N
2H
4与N
2O
4能放出大量的热。
(1)已知:2NO
2(g)=N
2O
4(g) △H=-57.20kJ·mol
-1。
一定温度下,在密闭容器中反应2NO
2(g)=N
2O
4(g) 达到平衡。
其它条件不变时,下列措施能提高NO
2转化率的是
(填字母)。
| A.减小NO2的浓度 | B.降低温度 | C.增加NO2的浓度 | D.升高温度 |
(2)25℃时,1.00gN
2H
4(l)与足量N
2O
4(l)完全反应生成N
2(g)和H
2O (l) ,放出19.14kJ
的热量。则反应2N
2H
4(l)+N
2O
4(l)=3N
2(g)+4H
2O (l)的△H=
kJ·mol
-1 (3)17℃、1.01×10
5Pa,密闭容器中N
2O
4和NO
2的混合气体达到平衡时,
c(NO
2)=0.0300mol·L
-1、c(N
2O
4)=0.0120mol·L
-1。
计算反应2 NO
2(g)

N
2O
4(g)的平衡常数K。
(4)现用一定量的Cu 与足量的浓HNO
3反应,制得1.00L已达平衡的N
2O
4和NO
2混合气体(17℃、1.01×10
5Pa),理论上至少需消耗Cu 多少克?
题号:4385794
题型:填空题
难易度:一般
日期:2009-11-18
来源:2009高考真题汇编-化学计算
题号:4385797
题型:计算题
难易度:容易
日期:2013-01-15
来源:2009高考真题汇编-化学计算
【题文】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:



(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为______g/mol
(保留一位小数)。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为_____________L。
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为__________________。





 的蔗糖溶液
的蔗糖溶液 的
的 溶液
溶液
 的
的 溶液
溶液 的
的 溶液
溶液 向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的
向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的 沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )
沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是( )
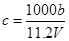
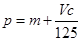
 <
< 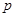 <
<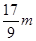









 与足量的NaOH
与足量的NaOH




 溶液充分反应,消耗的NaOH的物质的量为
溶液充分反应,消耗的NaOH的物质的量为

 溶液中阴离子总数大于0.1NA
溶液中阴离子总数大于0.1NA 中含N—H键数目为
中含N—H键数目为
 某研究性小组借助A-D的仪器装置完成有关实验
某研究性小组借助A-D的仪器装置完成有关实验

 【实验一】收集NO气体。
【实验一】收集NO气体。 用装置A收集NO气体,正确的操作上 (填序号)。
用装置A收集NO气体,正确的操作上 (填序号)。 a.从①口进气,用排水法集气 b.从①口进气,用排气法集气
a.从①口进气,用排水法集气 b.从①口进气,用排气法集气 c.从②口进气,用排水法集气 d..从②口进气,用排气法集气
c.从②口进气,用排水法集气 d..从②口进气,用排气法集气 【实验二】为了探究镀锌薄铁板上的锌的质量分数
【实验二】为了探究镀锌薄铁板上的锌的质量分数 和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。
和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。 方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究木目标。 (2)选用B和 (填仪器标号)两个装置进行实验。
(2)选用B和 (填仪器标号)两个装置进行实验。 (3)测得充分反应后生成氢气的体积为VL(标准状况),
(3)测得充分反应后生成氢气的体积为VL(标准状况), = 。
= 。 (4)计算镀层厚度,还需要检索的一个物理量是 。
(4)计算镀层厚度,还需要检索的一个物理量是 。 (5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。
(5)若装置B中的恒压分液漏斗改为普通分液漏斗,测量结果将(填“偏大”、“偏小”或“无影响”)。 方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g 。
方案乙:通过称量试样与碱反应前后的质量实现探究目标。选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g 。 (6)
(6) 。
。 方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标。实验同样使用仪器C。
方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标。实验同样使用仪器C。 (7)从实验误差角度分析,方案丙 方案乙(填“优于”、“劣于”或“等同于”)。
(7)从实验误差角度分析,方案丙 方案乙(填“优于”、“劣于”或“等同于”)。 以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略); (1 )从废液中提纯并结晶处FeSO4·7H2O。
(1 )从废液中提纯并结晶处FeSO4·7H2O。 (2)将
(2)将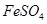 溶液与稍过量的
溶液与稍过量的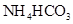 溶液混合,得到含
溶液混合,得到含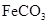 的浊液
的浊液 (3 )将浊液过滤,用90°C热水洗涤沉淀,干燥后得到
(3 )将浊液过滤,用90°C热水洗涤沉淀,干燥后得到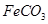 固体
固体 (4)煅烧
(4)煅烧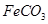 ,得到
,得到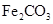 固体
固体 已知:
已知: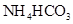 在热水中分解
在热水中分解 (1 )中,加足量的铁屑出去废液中的
(1 )中,加足量的铁屑出去废液中的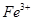 ,该反应的离子方程式是
,该反应的离子方程式是  (2)中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用
(2)中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用  (3 )中,生成
(3 )中,生成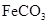 的离子方程式是 。若
的离子方程式是 。若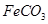 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是 。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是 。 (4)中,通过检验
(4)中,通过检验 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 操作是是 。
操作是是 。 (5)已知煅烧
(5)已知煅烧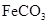 的化学方程式是
的化学方程式是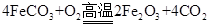 ,现煅烧464.0kg
,现煅烧464.0kg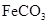 ,得到316.8kg产品,若产品中杂质只有
,得到316.8kg产品,若产品中杂质只有 ,则该产品中
,则该产品中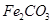 的质量是 kg(摩尔质量/g·
的质量是 kg(摩尔质量/g·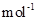 ;
;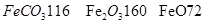 )
) ,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料
,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料 (
( 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程:
 完全转化为
完全转化为 。理论上需要加入
。理论上需要加入 
 4SiHCl3(g)
4SiHCl3(g) (标准状况)。
(标准状况)。 N2O4(g)的平衡常数K。
N2O4(g)的平衡常数K。
 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。

 (1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(1)根据左表中数据,在右图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:

 (2) 体系中发生反应的化学方程式是___________________________;
(2) 体系中发生反应的化学方程式是___________________________;
 (3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________;
 (4) 该反应达到平衡时反应物X的转化率
(4) 该反应达到平衡时反应物X的转化率 等于___________________________;
等于___________________________;
 (5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
(5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
 ① _________________ ②________________ ③__________________
① _________________ ②________________ ③__________________





