适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2016年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2016年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2016年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2016年')}}上传日期:2016-04-19题数:20
提示:单击题文可显示答案与解析。
题号:3132237
题型:选择题
难易度:一般
日期:2016-05-27
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】下列各组中化合物的性质比较,不正确的是
| A.酸性:HClO4>HBrO4>HIO4 | B.碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C.稳定性:PH3>H2S> HCl | D.非金属性:F>O>S |
题号:3145334
题型:选择题
难易度:较难
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】几种短周期元素的主要化合价及原子的原子半径数据见下表:
元素代号
| L
| M
| Q
|
| T
|
主要化合价
| +2
| +3
| +6、-2
| +7、-1
| -2
|
原子半径/nm
| 0.160
| 0.143
| 0.102
| 0.099
| 0.074
|
R
据表中信息判断,下列有关叙述中,正确的是
A.L、M的单质分别与同浓度的稀盐酸反应时,M的单质反应更剧烈
B.M与T形成的化合物能和强酸、强碱反应
C.Q、T两元素的氢化物热稳定性比较:Q的氢化物大于T的氢化物
D.L与R两元素形成的化合物中,含有共价键
题号:3145335
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】下列两种微粒一定属于同种元素原子的是
| A.3p能级有一个成对电子的基态原子和核外电子的排布式为1s22s22p63s23p2的原子 |
| B.2p能级有一个未成对电子的基态原子和原子的价电子排布为2s22p5的原子 |
| C.M层全充满而N层为4s2的原子和核外电子排布式为1s22s22p63s23p63d64s2的原子 |
| D.最外层电子数是核外电子总数的1/5的原子和价电子排布式为4s24p5的原子 |
题号:3145356
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】科学研究证明:核外电子的能量不仅与电子所处的能层、能级有关,还与核外电子的数目及核电荷的数目有关。氩原子与硫离子的核外电子排布相同,都是1s
22s
22p
63s
23p
6。下列说法正确的是
| A.两粒子的1s能级上电子的能量相同 |
| B.两粒子的3p能级上的电子离核的距离相同 |
| C.两粒子的电子发生跃迁时,产生的光谱不同 |
| D.两粒子都达8电子稳定结构,化学性质相同 |
题号:3145357
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】若
aA
m+与
bB
n-的核外电子排布相同,则下列关系不正确的是
| A.b=a-n-m | B.离子半径Am+<Bn- |
| C.原子半径A<B | D.A的原子序数比B大(m+n) |
题号:3145358
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】氧化钙在2973 K时熔化,而NaCl在1074 K时熔化,二者的离子间距和晶体结构都类似,有关它们熔点差别较大的原因叙述不正确的是
| A.氧化钙晶体中阴、阳离子所带电荷数多 |
| B.氧化钙晶格能比氯化钠的晶格能大 |
| C.两种晶体的晶胞结构类型不同 |
| D.氧化钙、氯化钠的离子间距类似情况下,晶格能主要由阴、阳离子所带电荷数决定 |
题号:3145359
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】下列关于金属晶体的叙述正确的是
| A.用铂金做首饰不能用金属键理论解释 |
| B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体 |
| C.Li、Na、K的熔点逐渐升高 |
| D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。 |
题号:3145360
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】右图为氯化钠的晶体结构模型,下列说法不正确的是
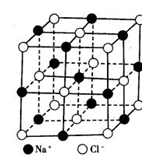
| A.NaC1晶体中Na+与C1— 的个数比为1:1 |
| B.每个Na+周围距离最近的C1— 数为6 |
| C.和Na+距离相等且最近的C1— 构成的多面体是正八面体 |
| D.每个Na+周围距离最近的Na+数为8 |
题号:3145361
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】在核电荷数为1~36的元素中,原子的最外层电子排布满足4S
1的元素共有()
题号:3145362
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】甲、乙是周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是[
题号:3145363
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】现有三种元素的基态原子的电子排布式如下:①1s
22s
22p
63s
23p
1;②1s
22s
22p
63s
23p
3;③1s
22s
22p
5。则下列有关比较中正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③< ②< ① | D.最高正化合价:③>②>① |
题号:3145365
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】某元素最高正价氧化物对应的水化物的化学式是H
2XO
4,这种元素的气态氢化物的化学式为
题号:3145366
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】“各能级最多容纳的电子数,是该能级原子轨道数的二倍”,支撑这一结论的理论是
| A.构造原理 | B.泡利不相容原理 |
| C.洪特规则 | D.能量最低原理 |
题号:3145367
题型:选择题
难易度:较易
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
题号:3145368
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】简单原子的原子结构可用右下图表示方法形象表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述错误的是
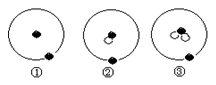
| A.①②③属同种元素 |
| B.①②③互为同位素 |
| C.①②③为氢元素的三种核素 |
| D.①②③是三种化学性质不同的粒子 |
题号:4302333
题型:选择题
难易度:一般
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】已知X、Y是主族元素,I为电离能,单位是kJ·mol
-1。请根据下表所列数据判断,错误的是
元素
| I1
| I2
| I3
| I4
|
X
| 500
| 4600
| 6900
| 9500
|
Y
| 580
| 1800
| 2700
| 11600
|
A.元素X的常见化合价是+1价
B.元素Y是IIIA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第3周期,它可与冷水剧烈反应
题号:3145330
题型:填空题
难易度:较难
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】C、Be、Cl、Fe等元素及其化合物有重要的应用。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl
2应为
(填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl
2应与
(填MgCl
2或AlCl
3)化学性质更相似。
(2)上述四种元素的原子中,未成对电子数最多的元素是_________________。
(3)①试根据原子核外电子排布所遵循的原理解释Fe
2+具有较的强还原性,易被氧化为Fe
3+的原因
。②当然Fe
3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式
。
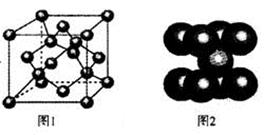
(4)一定条件下,C元素可形成多种晶体。下图1是其中某种晶体的一个晶胞,该晶胞中含有________个C原子。
(5)下图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol
-1,该晶体的密度为a g•cm
-3,N
A为阿伏加德罗常数的值,则该晶胞的体积为_________cm
3。
题号:3145331
题型:填空题
难易度:较难
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】(1)在Ni基催化剂作用下,CH
4和CO
2反应可获得化工原料CO和H
2。基态Ni原子的外围电子排布式为
,该元素位于元素周期表中的第
族。
(2)碳元素能够形成不同的单质,如C
60、C
70、金刚石等等。
①C
60、C
70、金刚石这些单质间互称为
。
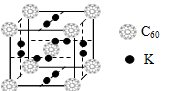
②科学家把C
60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C
60分子的个数比为
。
③继C
60后,科学家又合成了Si
60、N
60, C、Si、N三种原子电负性由大到小的顺序是
。
(3)铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
①Cu位于元素周期表第ⅠB族。Cu
2+的核外电子排布式为
。
②Cu
2O的熔点比Cu
2S的
(填“高”或“低”),请解释原因
。
题号:3145332
题型:填空题
难易度:较难
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层数;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为__________________,Y的轨道表示式为___________________。
(2)ZX2的分子式是__________________,YX2电子式是_____ _____________。
(3)Z形成的简单阴离子的结构示意图是 。
(4)Y和Z一定条件下形成简单分子的结构式是 。
题号:3145333
题型:推断题
难易度:较难
日期:2016-04-19
来源:2015-2016学年福建省四地六校高二下学期第一次联考化学试卷(带解析)
【题文】下表是元素周期表的一部分。
族
周期
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0
|
1
| A
| ]
|
|
|
|
|
|
|
2
|
|
|
|
| D
|
| F
| H
|
3
| B
|
| C
|
| E
|
| G
|
|
根据A~G元素在周期表中的位置,用化学式填写空白。
(1)氧化性最强的单质是__________,还原性最强的单质是__________,化学性质最不活泼的单质是__________。(填相应的化学式)
(2)最稳定的氢化物是__________。(填相应的化学式)
(3)按碱性逐渐减弱、酸性逐渐增强的顺序,将B、C、E、G四种元素的最高价氧化物对应水化物的化学式排列成序是
。(填相应的化学式)
(4)一个E原子的核外电子总共有几
种运动状态。



