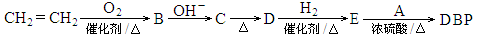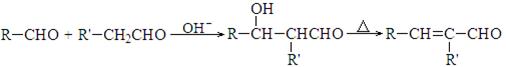适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2015年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2015年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2015年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2015年')}} 上传日期:2015-07-01 题数:12
题号:3204237
题型:选择题
难易度:一般
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】往密闭容器中通入一定量N
2 O
4 ,发生反应N
2 O
4 (g)
2NO
2 (g),随温度升高,气体颜色变深。下图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律。X、Y分别是
A.温度T,逆反应速率υ逆 B.温度T,气体的密度ρ C.压强P,平衡常数K D.压强P,N2 O4 转化率α
题号:3204238
题型:选择题
难易度:一般
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
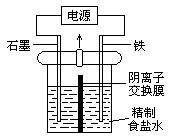
【题文】一定温度和电压下,电解精制食盐水可制取NaClO
3 。电解装置如图。已知:3Cl
2 + 6OH
- = ClO
3 - + 5Cl
- + 3H
2 O。下列说法正确的是
A.铁为阳极,电极反应式为2H2 O + 2e- = H2 ↑+ 2OH- B.若阴极产生3.36L(标况)气体,则溶液中的反应转移电子0.30mol C.电解槽内总反应方程式为:NaCl + 3H2 O 3 + 3H2 ↑ D.用阳离子交换膜代替阴离子交换膜,也一样可以制得NaClO3
题号:3204239
题型:选择题
难易度:一般
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】实验室对茶叶中铁元素的检验,可经以下四个步骤完成:①将茶叶灼烧灰化;②茶叶灰用浓硝酸浸取并加蒸馏水稀释;③过滤得到滤液;④用KSCN溶液进行检验。下列说法中正确的是
A.步骤①所用仪器包括蒸发皿、酒精灯、玻璃棒等 B.步骤②所用的浓硝酸应保存在带橡皮塞的棕色试剂瓶中 C.步骤③可以不做,改为将悬浊液静置一段时间 D.步骤④观察到溶液变红色,证明茶叶中含有Fe3+
题号:3204240
题型:选择题
难易度:一般
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示,下列说法正确的是
A.金属性:N>Q B.最高价氧化物对应水化物酸性:M>Y>N C.简单离子半径:Q>N>X D.原子序数:Z>M>Y>X
题号:3204241
题型:选择题
难易度:一般
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】下列措施,一定能使NaCl溶液中c(OH
- )减小的是
A.加热使c(H+ )增大 B.投入一小块金属钠 C.加入少量NH4 Cl固体 D.以铁为电极进行电解
题号:3204242
题型:选择题
难易度:较易
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】下列关于有机物的说法中,正确的是
A.油脂和蛋白质都是天然高分子化合物,都能水解 B.天然气和液化石油气的主要成分都是烃,都能燃烧 C.苯和乙烯都含有碳碳双键,都能和H2 发生加成反应 D.裂化汽油和四氯化碳都不溶于水,都可用于萃取溴
题号:3204243
题型:选择题
难易度:容易
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】下列过程中没有发生化学反应的是
A.用活性炭去除汽车内室的异味 B.用硝酸对钢船舱进行钝化处理 C.用经硫酸酸化处理的三氧化铬硅胶检验酒精 D.用小苏打溶水拌入面中一起蒸煮使馒头蓬松
题号:3204234
题型:实验题
难易度:困难
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
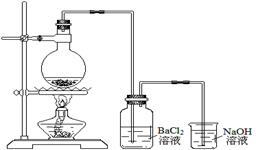
【题文】(15分)某学习小组探究铜跟浓硫酸反应的情况。取6.4g铜片和10mL 18mol·L
-1 的浓硫酸放在圆底烧瓶中,按下图所示装置进行实验。
(1)铜和浓硫酸反应的化学方程式为
。
(2)实验结束后,发现广口瓶中产生白色沉淀,加入足量盐酸后沉淀几乎完全溶解。简要分析广口瓶中产生沉淀的主要原因:
。
(3)实验结束后,发现烧瓶中有铜片剩余。根据所学知识,他们认为烧瓶中还有较多的硫酸剩余。选择合适的试剂,设计简单易行的实验方案证明有余酸:
。
供选择的试剂:铁粉、银粉、BaCl
2 溶液、Na
2 CO
3 溶液
(4)甲同学设计如下方案:测定产生气体的量,再计算余酸的浓度。下列测定产生气体的量的实验方法中,不可行的是
(填编号)。
a.将气体缓缓通过预先称量、盛有碱石灰的干燥管,反应结束后再次称量
b.将气体通入硫酸酸化的KMnO
4 溶液,再加足量BaCl
2 溶液,过滤、洗涤、干燥,称量沉淀
c.用排水法测定产生气体的体积
d.用排饱和NaHSO
3 的方法测定产生气体的体积
(5)乙同学设计通过酸碱中和滴定来测定余酸的浓度:待烧瓶冷却至室温后,将其中的溶液用蒸馏水稀释至100mL,移取25mL到锥形瓶中,滴加2滴酚酞试液,用标准NaOH溶液滴至终点。平行实验三次。
①稀释时,应先往
(填仪器名称)中加入
(填“烧瓶中的溶液”或“蒸馏水”)。
②该方法测得的余酸浓度
(填“偏大”、“偏小”或“准确”)。
(6)丙设计了测定余酸浓度的较为简易的实验方案:取出反应后剩余的铜片,进行洗涤、干燥、称量。若称得剩余铜片的质量为3.2g,反应后溶液体积变化忽略不计,则剩余硫酸的物质的量浓度为____。
题号:3204235
题型:填空题
难易度:困难
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】(15分)K
2 CO
3 有广泛的用途。
(1)钾肥草木灰中含有K
2 CO
3 、K
2 SO
4 、KCl等。将草木灰用水浸取,过滤、蒸发得浓缩液。
①该浓缩液呈碱性的原因用离子方程式表示为
。
②检验该浓缩液中Cl
- 所用的试剂有
。
A.AgNO3 溶液 B.硝酸 C.盐酸 D.Ba(NO3 )2 溶液
E.BaCl
2 溶液
(2)工业上曾利用如下反应生产碳酸钾:K
2 SO
4 + C + CaCO
3 → K
2 CO
3 + X+ CO
2 ↑(未配平)
已知X为两种元素组成的化合物,则X的化学式为
;反应中氧化剂与还原剂物质的量之比为
。
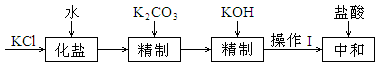
(3)离子膜电解-炭化法是目前生产碳酸钾的常用的方法。
第一步:精制KCl溶液
粗KCl中含有Ca
2+ 、Mg
2+ 等离子,按以下流程精制:
已知:加入K
2 CO
3 后,溶液中部分Mg
2+ 转化为MgCO
3 沉淀。
K
sp [Mg(OH)
2 ]=5.6×10
-12 ,K
sp (CaCO
3 )=2.8×10
-9 ,K
sp (MgCO
3 )=6.8×10
-6 。
①操作Ⅰ的名称是
。
②当加入KOH后,溶液中n(CO
3 2 - )增大,主要原因是
。
第二步:电解精制后的KCl溶液制取KOH,其它产物制取盐酸。
第三步:将KOH与CO
2 反应转化为KHCO
3 ,再将KHCO
3 分解得到产品。
③离子膜电解-炭化法的整个过程中,可以循环利用的物质有
。
题号:3204236
题型:填空题
难易度:较难
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】(15分)A、B、C、X是中学化学常见物质,它们在一定条件下具有如下转化关系:
A + X → B + C + H
2 O
(1)若X是淀粉水解的最终产物,B为砖红色难溶于水的氧化物。
①X的化学式为
。
②A溶于硝酸的离子方程式为
。
③将淀粉水解液中和后,与A的悬浊液(含NaOH)共热至沸腾,产生砖红色沉淀则证明淀粉已经水解。若要进一步探究淀粉是否完全水解,还需用到的试剂是
。
(2)若A是由M
+ 和R
- 构成的盐,X为二元强碱,B为气体。
①B与氧气一定条件下可以发生置换反应,当生成18g液态水时,放出能量Q kJ,该反应的热化学方程式为
;若将该反应设计成燃料电池(以硫酸溶液为电解质溶液),其负极反应式为
。
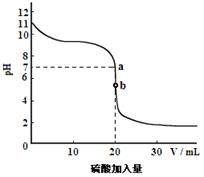
②室温时,20mL 0.10mol·L
-1 的B溶液用0.050mol·L
-1 的硫酸溶液滴定,所得滴定曲线如图所示。曲线上a点,c(M
+ )
c(SO
4 2 - )(填“>”、“<”或“=”)。曲线上b点,溶液中c(H
+ )≈
(只保留一位有效数字)。
题号:4306345
题型:填空题
难易度:困难
日期:2015-07-03
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
【题文】选做[化学—物质结构与性质](13分)氨是重要的化工原料,用途很广。
(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH
3 )
2 ]
+ 和CH
3 COO
- 构成)溶液吸收对氨合成催化剂有毒害的CO气体。
①醋酸二氨合铜所含的元素中,第一电离能最大的是
(填元素名称)。
②醋酸二氨合铜所含元素组成的单质,所属的晶体类型有
(填标号)。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
③第4周期元素中,基态原子与基态Cu原子具有相同未成对电子数的有
种(不含Cu)。
(2)BF
3 气体与NH
3 相遇立即生成一种白色晶体:BF
3 + NH
3 = F
3 B—NH
3 。
①BF
3 和NH
3 分子的空间构型分别为
、
。
②晶体F
3 B—NH
3 中,B原子的杂化轨道类型为
。
(3)NH
3 可用于合成尿素、硫酸铵等氮肥。某化肥厂从生产的硫酸铵中检出一种组成为N
4 H
4 (SO
4 )
2 的物质。该物质易溶于水,在水溶液中以SO
4 2 - 和N
4 H
4 4+ 两种正四面体构型的离子存在。N
4 H
4 4+ 遇碱生成一种形似白磷的N
4 分子。
①下列相关说法中,正确的是
(填序号)。
a.N
4 是N
2 的同分异构体
b.1mol N
4 分解生成N
2 ,形成了4mol π键
c.白磷的沸点比N
4 高,原因是P—P键键能比N—N键大
d.白磷的化学性质比N
2 活泼,说明P的非金属性比N强
②画出N
4 H
4 4+ 的结构(标明其中的配位键):
。
题号:3204233
题型:推断题
难易度:困难
日期:2015-07-01
来源:【百强校】2015届福建省泉州五中高三5月模拟理综化学试卷(带解析)
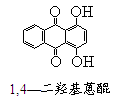
【题文】选做[化学——有机化学基础](13分)芳香族化合物A(C
8 H
6 O
4 )能与NaHCO
3 溶液反应生成CO
2 。由A与对二氯苯(
)为原料经多步反应可合成1,4—二羟基蒽醌(结构如下图所示)。
(1)A的结构简式为
。
(2)下列关于对二氯苯的说法中,正确的是
(填序号)。
a.对二氯苯分子中所有原子都在同一平面上
b.对二氯苯进行氯化得到的三氯苯有三种
c.由苯和氯气制取对二氯苯的反应是加成反应
d.对二氯苯水解生成对氯苯酚的反应是氧化反应
以A和乙烯为原料,通过如下路线,可以合成塑化剂DBP(C
16 H
22 O
4 )。
已知:
(3)D中不含氧官能团的名称为
。
(4)由B生成E的过程中,涉及的反应类型有
(填序号)。
a.取代反应 b.加成反应 c.消去反应 d.还原反应
(5)写出E与A反应合成DBP的化学方程式:
。
(6)直链化合物X是C的同分异构体,X分子中不含甲基,其
1 H核磁共振谱图中有3种峰。X的结构简式为
。
 2NO2(g),随温度升高,气体颜色变深。下图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律。X、Y分别是
2NO2(g),随温度升高,气体颜色变深。下图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律。X、Y分别是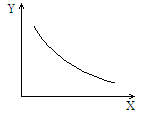
 NaClO3 + 3H2↑
NaClO3 + 3H2↑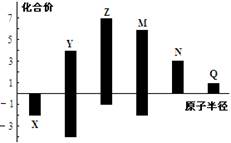

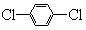 )为原料经多步反应可合成1,4—二羟基蒽醌(结构如下图所示)。
)为原料经多步反应可合成1,4—二羟基蒽醌(结构如下图所示)。