适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2016年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2016年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2016年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2016年')}} 上传日期:2016-04-13 题数:30
题号:3147024
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,下列有关说法中,正确的是
A. 当有0.1 mol电子转移时,a极产生1.12 L O
2 (标准状况下)
B. b极上发生的电极反应是:4H
2 O+4e
- ===2H
2 ↑+4OH
- C. c极上发生的电极反应是:O
2 +4H
+ +4e
- ===2H
2 O
D. d极上进行还原反应,产生的H
+ 可以通过隔膜进入A中
题号:3147025
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】用惰性电极电解物质的量浓度相同、体积比为1:3的CuSO
4 和NaCl的混合溶液,可能发生的反应有:
①2Cu
2+ +2H
2 O
2Cu+4H
+ +O
2 ↑;
②Cu
2+ +2Cl
- Cu+Cl
2 ↑;
③2Cl
- +2H
2 O
2OH
- +H
2 ↑+Cl
2 ↑;
④2H
2 O
2H
2 ↑+O
2 ↑
题号:3147026
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】在密闭容器中发生反应N
2 O
4 (g)
2NO
2 (g) ΔH=+57kJ·mol
-1 ,在温度为T
1 、T
2 时,平衡体系中NO
2 的体积分数随压强变化曲线如图所示.下列说法正确的是
A.反应温度:T1 >T2 B.b、c两点的反应速率:v(b)>v(c) C.a、c两点气体的颜色:a浅,c深 D.a、b两点的平衡常数:Kb >Ka
题号:3147027
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在10L密闭容器中,将CO和H
2 S混合加热并达到下列平衡:CO(g)+H
2 S(g)
COS(g) +H
2 (g) K=0.1反应前CO的物质的量为10mol,平衡后CO的物质的量为8mol。下列说法正确的是
A.升高温度,H2 S浓度增加,表明该反应是吸热反应 B.反应前H2 S物质的量为7mol C.CO的平衡转化率为80% D.通入CO后,正反应速率逐渐增大
题号:3147028
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】温度一定时,在密闭容器中发生可逆反应:mA(g) +nB(g)
pC(g),达平衡后,若将混合气体的体积压缩到原来的一半。当再次达到平衡时,C的浓度为原来浓度的1.8倍,下列叙述中正确的是
A.平衡向逆反应方向移动 B.气体C的体积分数增大 C.m+n>p D.气体A的转化率升高
题号:3147029
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】根据以下三个热化学方程式:
2H
2 S(g) +3O
2 (g) ===2SO
2 (g) +2H
2 O(l) ΔH
1 = -akJ•mol
-1 2H
2 S(g) +O
2 (g) ==="2S(s)" +2H
2 O(l) ΔH
2 = -bkJ•mol
-1 2H
2 S(g) +O
2 (g) ==="2S(s)" +2H
2 O(g) ΔH
3 = -c kJ•mol
-1 (a、b、c均为正数)
对a、b、c三者大小关系的判断正确的是( )
A.a>c>b B.a>b>c C.c>b>a D.b>a>c
题号:3147030
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图Ⅰ所示,若其它条件不变,当温度分别为 T
1 和T
2 时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是
A.该反应的热化学方程式为X(g)+3Y(g) B.若其它条件不变,升高温度,正、逆反应速度均增大,X的转化率增大 C.达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 D.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动
题号:3147031
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】反应3H
2 (g)+CO
2 (g)
CH
3 OH(g)+H
2 O (g) ΔH<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH
3 OH物质的量分数的变化情况如图所示,下列判断正确的是
A.P3 >P2 T3 >T2 B.P2 >P4 T4 >T2 C.P1 >P3 T1 >T3 D.P1 >P4 T2 < T3
题号:3147032
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
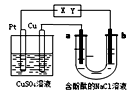
【题文】如图所示,a、b都是惰性电极,通电一段时间后,a极附近溶液显红色。下列说法中正确的是
A.CuSO4 溶液的n(SO4 2- )保持不变 B.U型管中溶液pH值逐渐变小 C.CuSO4 溶液的c(Cu2+ )逐渐减小 D.X是正极,Y是负极
题号:3147033
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】根据碘与氢气反应的热化学方程式:
①I
2 (g)+H
2 (g)
2HI(g) ΔH=-9.48kJ•mol
-1 ;
②I
2 (s) +H
2 (g)
2HI(g) ΔH=+26.48kJ•mol
-1 .
下列判断正确的是
A.反应①的产物比反应②的产物稳定 B.254gI2 (g)中通入2gH2 (g),反应放热9.48kJ C.反应②的反应物总能量比反应①的反应物总能量低 D.1mol固态碘与1mol气态碘所含的能量相差17.00kJ
题号:3147034
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】下列有关电化学知识的说法正确的是
A.电解CuSO4 溶液一段时间后,加入适量Cu(OH)2 可以使溶液恢复至原状态 B.将钢闸门与直流电源的负极相连,可以防止钢闸门腐蚀 C.电解AlCl3 、FeCl3 、CuCl2 的混合溶液,在阴极上依次析出Cu、Fe、Al D.铅蓄电池在充电时,连接电源正极的电极上发生:PbSO4 +2e- ===Pb+SO4 2-
题号:3147035
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】相同材料的铁在图中的四种情况下最不易被腐蚀的是
题号:3147056
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
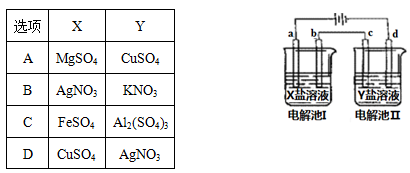
【题文】下图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b﹤d。符合上述实验结果的盐溶液是
题号:3147057
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】在一定温度下的恒容容器中进行反应:A(g)+2B(g)
C(g)+D(g),当下列哪些物理量不再发生变化时,能表明该可逆反应已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体总体积 ⑤混合气体总物质的量 ⑥混合气体的平均相对分子质量 ⑦混合气体总质量
A.①③⑤⑥ B.①②④⑦ C.①②③④⑤⑥⑦ D.①②③④⑤
题号:3147058
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】下列说法正确的是
A.pH=7的溶液一定呈中性 B.[OH- ]=1×10-6 mol•L-1 的溶液一定呈碱性 C.[OH- ]<[H+ ]的溶液一定呈酸性 D.室温下由水电离出来的[H+ ]=1×10-12 mol•L-1 的溶液一定呈碱性
题号:3147059
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】下列关于铜电极的叙述中不正确的是
A.铜锌原电池中铜是正极 B.铁壳船底部镶嵌铜块,铜块更易被腐蚀 C.用电解法精炼粗铜时粗铜作阳极 D.在镀件上镀铜是可用金属铜作阳极
题号:3147060
题型:选择题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na
2 S
2 O
3 +H
2 SO
4 ===Na
2 SO
4 +SO
2 +S↓+H
2 O,下列各组实验中最先出现浑浊的是
实验 反应温度/℃ Na2 S2 O3 溶液 稀H2 SO4 H2 O V/mL c/(mol•L-1 ) V/mL c/(mol•L-1 ) V/mL A 25 5 0.1 10 0.1 5 B 25 5 0.2 5 0.2 10 C 35 5 0.1 10 0.1 5 D 35 5 0.2 5 0.2 10
题号:3147061
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】在一个密闭的容器中发生如下反应:2SO
2 (g)+O
2 (g)
2SO
3 (g),反应过程中某一时刻SO
2 、O
2 、SO
3 的浓度均为0.1 mol·L
-1 ,当达到平衡时可能的数据是
A.c(SO3 )=0.15mol·L-1 B.c(SO3 )= c(SO2 )="0.075" mol·L-1 C.c(SO3 )=0.2 mol·L-1 D.c(O2 )="0.05" mol·L-1
题号:3147062
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
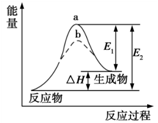
【题文】对于反应C(s)+H
2 O(g)⇌CO(g)+H
2 (g);ΔH>0,下列有关说法正确的是
A.升高体系温度,平衡常数K减小 B.增加C(s)的量,平衡正向移动 C.增大体系压强,平衡常数K不发生变化 D.平衡常数表达式为K=
题号:3147063
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】某化学反应的能量变化如图所示。下列有关叙述正确的是
A.该反应为吸热反应,ΔH=E1 -E2 B.使用催化剂,ΔH减小 C.使用催化剂,可以改变化学平衡常数 D.如图可知b使用了催化剂,反应速率加快
题号:3147064
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】反应CH
3 OH(g) + NH
3 (g) === CH
3 NH
2 (s) + H
2 O(g)在高温下才能自发向右进行,则该反应的ΔH、ΔS应为
A.ΔH>0、ΔS<0 B.ΔH<0、ΔS>0 C.ΔH>0、ΔS>0 D.ΔH<0、ΔS<0
题号:3147065
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】二氧化硫与氧气的反应为:2SO
2 (g)+O
2 (g)
2SO
3 (g) ΔH <0, 在硫酸工业生产中应采取的适宜条件是
A.低温、低压、催化剂 B.高温、高压、催化剂 C.低温、常压、催化剂 D.适宜的温度、常压、催化剂
题号:3147066
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】向一个2L容密闭容器中充入3.6molN
2 和10.8molH
2 ,一定的条件下反应生成NH
3 ,10min后测得N
2 的浓度是0.8 mol·L
-1 , 则在这10min内NH
3 的平均反应速率是
A.0.1 mol·L-1 ·min-1 B.0.2 mol·L-1 ·min-1 C.0.3 mol·L-1 ·min-1 D.0.6 mol·L-1 ·min-1
题号:3147067
题型:选择题
难易度:一般
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热。甲烷的燃烧热是890.3kJ·mol
-1 ,则下列热化学方程式中书写正确的是
A.CH4 (g)+2 (g)=CO(g)+2H2 O(l)ΔH=-890.3kJ·mol-1 B.CH4 (g)+2O2 (g)=CO2 (g)+2H2 O(g)ΔH=-890.3kJ C.CH4 (g)+2O2 (g)=CO2 (g)+2H2 O(l)ΔH=+890.3kJ·mol-1 D.CH4 (g)+2O2 (g)=CO2 (g)+2H2 O(l)ΔH=-890.3kJ·mol-1
题号:3147068
题型:选择题
难易度:较易
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】下列物质对水的电离平衡不产生影响的是
A.H2 SO4 B.Ba(OH)2 C.KCl D.CH3 COONa
题号:3147021
题型:实验题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】(1)已知:①C(s)+O
2 (g)=CO
2 (g) ΔH =" a" kJ·mol
-1 ②2CO(g)+O
2 (g)=2CO
2 (g) ΔH =" b" kJ·mol
-1 ;
③TiO
2 (s)+2Cl
2 (g)=TiCl
4 (s)+O
2 (g) ΔH ="c" kJ·mol
-1 ;
则TiO
2 (s)+2Cl
2 (g)+2C(s)=TiCl
4 (s)+2CO(g)的ΔH =
kJ·mol
-1 。(用含a、b、c的式子表示)
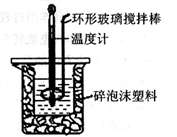
(2)用50 mL 0.50mol·L
-1 盐酸与50 mL 0.55 mol·L
-1 NaOH溶液,在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
起始温度t1 /℃ 终止温度t2 /℃ 温度差2 - t1 )/℃ 平均值 1 25.5 25.0 25.25 28.5 3.25 2 24.5 24.2 24.45 27.6 3.15 3 25.0 24.5 24.75 26.5 1.75
①该实验中,量取50 mL盐酸或NaOH溶液,需要用到的玻璃仪器除胶头滴管外还要
;
②装置中大、小烧杯之间填满碎泡沫塑料的目的是
;
③某同学实验记录的数据如上表所示,其中记录的终止温度是指
温度;
④计算该实验发生中和反应时放出的热量为
J[中和后生成的溶液的比热容c="4.2" J·(g·℃)
-1 ,稀溶液的密度都为1 g·cm
-3 ];
⑤若用50 mL 0.55 mol·L
-1 的氨水(NH
3 ·H
2 O)代替NaOH溶液进行上述实验,通过测得的反应热来计算中和热,测得的中和热ΔH会
(填“偏大”、 “偏大”或“不变”,其原因是
。
题号:3147019
题型:填空题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】工业上合成甲醇的反应为:CO(g) + 2H
2 (g)
CH
3 OH(g) ΔH <0。300℃,5MPa条件下,将0.20mol CO与0.58mol H
2 的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示.
(1)计算300℃时该反应的平衡常数K=_______________.
(2)CO 的平衡转化率为_______________.
(3)下列措施可增大甲醇产率的是____________.
A.压缩容器体积 B.将CO(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H
2 (4)可判断可逆反应达到平衡状态的依据是______.
A.v
正 (CO)= 2v
逆 (H
2 )
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.容器中CO、H
2 、CH
3 OH的物质的量之比为1:2:1
E.混合气体压强不再随时间变化而变化
(5)若其它条件不变,使反应在500℃下进行,在上图中作出甲醇的物质的量浓度随时间的变化的示意图.
(6)甲醇与水蒸气反应生成氢气的反应方程式:CH
3 OH(g)+H
2 O(g)
CO
2 (g)+3H
2 (g) ΔH>0;反应在图2中进行。其中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1mol CH
3 OH(g)和2mol H
2 O(g),向B容器中充入1.2mol CH
3 OH(g)和2.4mol H
2 O(g),两容器分别发生上述反应.已知起始时容器A和B的体积均为a L.试回答:反应达到平衡时容器B的体积为1.5a L,容器B中CH
3 OH的转化率为______,A、B两容器中H
2 O(g)的体积百分含量的大小关系为B______A(填“>”“<”或“=”).
题号:3147020
题型:填空题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO
2 、NO
2 和CO是其中3项中的污染物。
(1)一定温度下,向固定体积为2 L的密闭容器中充入SO
2 和NO
2 各1 mol,发生反应SO
2 (g)+NO
2 (g)
SO
3 (g)+NO(g),测得上述反应5 min末到达平衡,此时容器中NO与NO
2 的体积比为3︰1,则这段时间内SO
2 的反应速率υ(SO
2 )=
,此反应在该温度下的平衡常数表达式为K=
。
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H
2 合成甲醇,其反应的化学方程式为CO(g)+2H
2 (g)
CH
3 OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H
2 用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为
反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数K
A 、K
B 、K
C 的大小关系为
。A、B两点对应的压强大小关系是P
A P
B (填“大于”、 “小于”或“等于”)。
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时负极的电极反应式为
,理论上通过外电路的电子最多为
mol。
题号:3147022
题型:填空题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
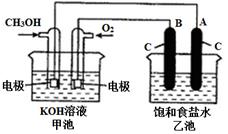
【题文】甲醇是一种可再生能源,具有广泛的开发和应用前景.下图是用甲醇燃料电池电解饱和食盐水的装置示意图。已知甲池的总反应式为: 2CH
3 OH+3O
2 +4KOH==2K
2 CO
3 +6H
2 O
请回答下列问题
(1)甲池是________装置,通入CH
3 OH的电极名称是______(填“正极”或“负极”); 通入O
2 的电极上发生: ____________________
(2)乙池中A是________极(填“阴”或“阳”);用湿润的淀粉碘化钾试纸来检验B电极 上产生的_________________。
(3)乙池中反应的总反应的化学方程式为_____________________;
(4)若将乙池中的NaCl溶液换成AgNO
3 溶液,B电极上发生的电极反应:_____________;
(5)若将乙池中B电极换成铜电极,B电极上发生的电极反应:_____________;
(6)若反应结束后乙池中A(石墨)电极上共收集到气体0.050mol,则甲池中理论上消耗O
2 _____mL(标准状况下)。
题号:3147023
题型:填空题
难易度:较难
日期:2016-04-13
来源:【百强校】2015-2016学年福建省三明一中高二下第一次月考化学试卷(带解析)
【题文】利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值。
已知:①CH
4 (g)+H
2 O(g)
CO(g)+3H
2 (g)ΔH=+206.2kJ·mol
-1 ②CO(g)+H
2 O(g)
CO
2 (g)+H
2 (g)ΔH=-42.3kJ·mol
-1 (1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为___________________。
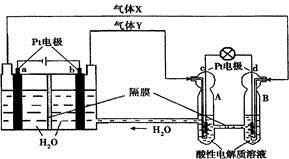
(2)为了探究反应条件对反应CO(g)+H
2 O(g)
CO
2 (g)+H
2 (g)ΔH=-42.3kJ·mol
-1 的影响,某活动小组设计了三个实验,实验曲线如图3所示
编号 温度 压强 c始 (CO) c始 (H2 O) Ⅰ 530℃ 3MPa 1.0mol·L-1 3.0mol·L-1 Ⅱ X Y 1.0mol·L-1 3.0mol·L-1 Ⅲ 630℃ 5MPa 1.0mol·L-1 3.0mol·L-1
①请依据实验曲线图补充完整表格中的实验条件:X=______℃,Y=______MPa。
②实验Ⅲ从开始至平衡,其平均反应速度率v(CO)=___________mol·L
-1 ·min
-1 。
③实验Ⅱ达平衡时CO的转化率________实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”)。
④在530℃时,平衡常数K=1,若往1L容器中投入0.2molCO(g)、0.2molH
2 O(g)、0.1molCO
2 (g) 、0.1 mol H
2 (g),此时化学反应将_________(填“正向”、“逆向”或“不”) 移动。
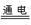 2Cu+4H++O2↑;
2Cu+4H++O2↑; Cu+Cl2↑;
Cu+Cl2↑; 2OH-+H2↑+Cl2↑;
2OH-+H2↑+Cl2↑; 2H2↑+O2↑
2H2↑+O2↑ 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是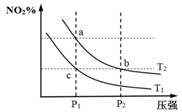
 COS(g) +H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO的物质的量为8mol。下列说法正确的是
COS(g) +H2(g) K=0.1反应前CO的物质的量为10mol,平衡后CO的物质的量为8mol。下列说法正确的是 pC(g),达平衡后,若将混合气体的体积压缩到原来的一半。当再次达到平衡时,C的浓度为原来浓度的1.8倍,下列叙述中正确的是
pC(g),达平衡后,若将混合气体的体积压缩到原来的一半。当再次达到平衡时,C的浓度为原来浓度的1.8倍,下列叙述中正确的是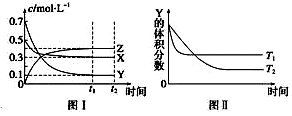
 2Z(g) ΔH<0
2Z(g) ΔH<0 CH3OH(g)+H2O (g) ΔH<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,下列判断正确的是
CH3OH(g)+H2O (g) ΔH<0,在一定条件下达到平衡时,改变温度(T)和压强(P),CH3OH物质的量分数的变化情况如图所示,下列判断正确的是
 2HI(g) ΔH=-9.48kJ•mol-1;
2HI(g) ΔH=-9.48kJ•mol-1; 2HI(g) ΔH=+26.48kJ•mol-1.
2HI(g) ΔH=+26.48kJ•mol-1.
 C(g)+D(g),当下列哪些物理量不再发生变化时,能表明该可逆反应已达到平衡状态的是
C(g)+D(g),当下列哪些物理量不再发生变化时,能表明该可逆反应已达到平衡状态的是 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是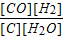
 2SO3(g) ΔH <0, 在硫酸工业生产中应采取的适宜条件是
2SO3(g) ΔH <0, 在硫酸工业生产中应采取的适宜条件是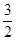 O2(g)=CO(g)+2H2O(l)ΔH=-890.3kJ·mol-1
O2(g)=CO(g)+2H2O(l)ΔH=-890.3kJ·mol-1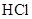
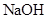
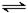 CH3OH(g) ΔH <0。300℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示.
CH3OH(g) ΔH <0。300℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示.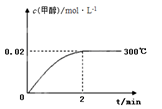
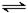 CO2(g)+3H2(g) ΔH>0;反应在图2中进行。其中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1mol CH3OH(g)和2mol H2O(g),向B容器中充入1.2mol CH3OH(g)和2.4mol H2O(g),两容器分别发生上述反应.已知起始时容器A和B的体积均为a L.试回答:反应达到平衡时容器B的体积为1.5a L,容器B中CH3OH的转化率为______,A、B两容器中H2O(g)的体积百分含量的大小关系为B______A(填“>”“<”或“=”).
CO2(g)+3H2(g) ΔH>0;反应在图2中进行。其中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1mol CH3OH(g)和2mol H2O(g),向B容器中充入1.2mol CH3OH(g)和2.4mol H2O(g),两容器分别发生上述反应.已知起始时容器A和B的体积均为a L.试回答:反应达到平衡时容器B的体积为1.5a L,容器B中CH3OH的转化率为______,A、B两容器中H2O(g)的体积百分含量的大小关系为B______A(填“>”“<”或“=”).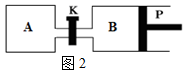
 SO3(g)+NO(g),测得上述反应5 min末到达平衡,此时容器中NO与NO2的体积比为3︰1,则这段时间内SO2的反应速率υ(SO2)= ,此反应在该温度下的平衡常数表达式为K= 。
SO3(g)+NO(g),测得上述反应5 min末到达平衡,此时容器中NO与NO2的体积比为3︰1,则这段时间内SO2的反应速率υ(SO2)= ,此反应在该温度下的平衡常数表达式为K= 。 CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: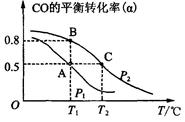
 CO(g)+3H2(g)ΔH=+206.2kJ·mol-1
CO(g)+3H2(g)ΔH=+206.2kJ·mol-1 CO2(g)+H2(g)ΔH=-42.3kJ·mol-1
CO2(g)+H2(g)ΔH=-42.3kJ·mol-1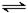 CO2(g)+H2(g)ΔH=-42.3kJ·mol-1
CO2(g)+H2(g)ΔH=-42.3kJ·mol-1