适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2014年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2014年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2014年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2014年')}}上传日期:2014-10-24题数:31
提示:单击题文可显示答案与解析。
题号:3232463
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。RFC的工作原理如图如示。下列有关说法正确的是

A.当有0.1mol电子转移时,a电极产生标况下2.24LH
2B.b电极上发生的电极反应式为4H
2O+4e
-=2H
2↑+4OH
-C.c电极上进行还原反应,B池中的H
+可以通过隔膜进入A池
D.d电极上发生的电极反应式为O
2+4H
++4e
-=2H
2O
题号:3232464
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】.下列事实中,能用化学平衡移动原理来解释的是
| A.加入催化剂有利于合成氨的反应 |
B.对于反应2HI(g) H2(g)+I2(g),增大平衡体系的压强(压缩体积),可使体系颜色变深 H2(g)+I2(g),增大平衡体系的压强(压缩体积),可使体系颜色变深 |
| C.500℃左右比室温更有利于合成氨反应 |
| D.高压条件有利于合成氨反应 |
题号:3232465
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】已知可逆反应aA+bB

cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是

| A.该反应在T1、T3温度时达到化学平衡 |
| B.该反应在T2温度时达到化学平衡 |
| C.该反应的逆反应是放热反应 |
| D.升高温度,平衡会向正反应方向移动 |
题号:3232466
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】在100mLH
2SO
4、CuSO
4的混合液中,用石墨做电极电解,两极均收集到2.24L气体(标准状况),则原混合液中Cu
2+的物质的量浓度为
| A.1 mol •L-1 | B.2 mol •L-1 | C.3 mol •L-1 | D.4 mol •L-1 |
题号:3232467
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】在1100℃,一定容积的密闭容器中发生反应:FeO(s) + CO(g)

Fe(s) + CO
2(g) ΔH ="a" kJ/mol (a >0),该温度下K=0.263,下列有关该反应的说法正确的是
| A.若增加CO的用量,上式中的ΔH增大 |
| B.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| C.若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| D.达到化学平衡状态时,若c(CO)="0.100" mol/L,则c(CO2)="0.0263" mol/L |
题号:3232468
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】下图为某种甲醇燃料电池示意图,工作时电子流方向如图所示。下列判断正确的是

| A.X为氧气 |
| B.电极A反应式:CH3OH-6e-+H2O = CO2+6H+ |
| C.B电极附近溶液pH增大 |
| D.电极材料活泼性:A>B |
题号:3232469
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是

| A.a和b不连接时,铁片上会有金属铜析出 |
| B.a和b用导线连接时,铜片上发生的反应为:Cu2+ + 2e- = Cu |
| C.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D.a和b分别连接直流电源正、负极,Cu2+向铜电极移动 |
题号:3232470
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】已知合成氨反应N
2(g)+3H
2(g)

2NH
3(g)△H=-92.30kJ ·mol
-1,在某温度下,2L的密闭容器中进行,测得如下数据:

下列说法正确的是
| A.反应进行到1小时时放出的热量为9.23kJ |
| B.反应3h内,反应速率v(N2)为0.17mol·L-1·h-1 |
| C.此温度下,该反应的平衡常数为0.037 |
| D.4h时,若再加入1mol N2,达到新的平衡时,N2的转化率是原来的两倍 |
题号:3232471
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】在密闭容器中进行下列反应:M(g)+N(g)===R(g)+2L。此反应符合下列图象,R%为R在平衡混合物中的体积分数,该反应是

| A.正反应为吸热反应 L是气体 |
| B.正反应为放热反应 L是气体 |
| C.正反应为吸热反应 L是固体 |
| D.正反应为放热反应 L是固体或液体 |
题号:3232472
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】在密闭容器中充入一定量的NO
2,发生反应2NO
2(g)

N
2O
4(g)△H=﹣57kJ/mol,在温度为T
1、T
2时,平衡体系中NO
2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
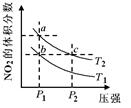
| A.a、c两点的反应速率:a>c |
| B.a、b两点的转化率:a<b |
| C.a、c两点气体的颜色:a深,c浅 |
| D.由a点到b点,可以用加热的方法 |
题号:3232473
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】对于可逆反应2AB
3(g)

A
2(g) +3B
2(g) ; ΔH>0,下列图像正确的是

题号:3232474
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】某密闭容器中发生如下反应:X(g)+3Y(g)

2Z(g);ΔH<0
下图表示该反应的速率(v)随时间(t)变化的关系,t
2、t
3、t
5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
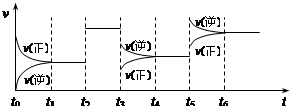
| A.t2时加入了催化剂 | B.t3时降低了温度 |
| C.t5时增大了压强 | D.t4~t5时间内转化率最低 |
题号:3232475
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】密闭容器中mA(气)+nB(气)

pC(气)达平衡后, 温度一定时, 将气体体积压缩到原来的一半, 当重新达平衡时, C的浓度为原来的1.9倍, 下列说法不正确的是
| A.m+n<p | B.平衡向逆反应方向移动 |
| C.A转化率降低 | D.C的体积分数增大 |
题号:3232476
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】体积相同的甲、乙两个容器中,分别都充有等物质的量的SO
2和O
2在相同温度下发生反应:2SO
2+O
2
2SO
3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO
2的转化率为p%,则乙容器中SO
2的转化率
题号:3232477
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】可逆反应:3A(g) = 3B(?)+ C(?)(正反应吸热),随着温度的升高,气体平均相对分子质量变小,则下列判断正确的是
| A.B和C都是固体 | B.B和C一定都是气体 | C.B和C可能都是气体 | D.无法判断 |
题号:3232478
题型:选择题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】对于反应2SO
2(g)+O
2(g)

2SO
3(g),能增大正反应速率且提高O
2的转化率的措施是
| A.移去部分SO3 | B.降低体系温度 | C.通入大量O2 | D.通入大量SO2 |
题号:3232479
题型:选择题
难易度:较易
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】甲、乙两个容器内都进行A―→B的反应,甲容器内每分钟减少4 mol A,乙容器内每分钟减少2 mol A,则甲容器内的反应速率比乙容器内的反应速率
题号:3232480
题型:选择题
难易度:较易
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】电解稀H
2SO
4、Cu(NO
3)
2、NaCl的混合液,最初一段时间阴极和阳极上分别析出的物质分别是
| A.H2和Cl2 | B.Cu和Cl2 | C.H2和O2 | D.Cu和O2 |
题号:3232481
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】高温下,某反应达平衡,平衡常数K=

, 恒容时,温度升高,H
2浓度减小。下列说法正确的是
A.该反应的化学方程式为 CO + H2O CO2 + H2 CO2 + H2 |
| B.该反应的焓变为正值 |
| C.升高温度,逆反应速率减小 |
| D.恒温恒容下,充入稀有气体, H2浓度增大 |
题号:3232482
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】反应2X(g)+Y(s)

2Z(g) ΔH<0,达到平衡时,下列说法正确的是
| A.减小容器体积,平衡不移动 | B.增大Y的量,Z的百分含量增大 |
| C.加入催化剂,X的转化率增大 | D.降低温度,正反应速率增大、逆反应速率减小 |
题号:3232483
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】已知:H
2O(g)===H
2O(l) ΔH=Q
1kJ·mol
-1C
2H
5OH(g)===C
2H
5OH(l)ΔH=Q
2kJ·mol
-1C
2H
5OH(g)+3O
2(g)===2CO
2(g)+3H
2O(g) ΔH=Q
3kJ·mol
-1若使46 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为
| A.(Q1+Q2+Q3) kJ | B.0.5(Q1+Q2+Q3) kJ |
| C.(0.5Q1-1.5Q2+0.5Q3) kJ | D.(3Q1-Q2+Q3) kJ |
题号:3232484
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】通常人们把拆开1 mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下列是一些化学键的键能。
化学键
| C—H
| C—F
| H—F
| F—F
|
键能/(kJ·mol ) )
| 414
| 489
| 565
| 155
|
根据键能数据估算下列反应的反应热ΔH为:CH
4 (g)+4F
2 (g) ===CF
4(g)+4HF(g)
A.–1940 kJ · mol
-1 B.1940 kJ · mol
-1C.–485 kJ · mol
-1 D.485 kJ · mol
-1
题号:3232485
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】下列有关热化学方程式的叙述正确的是
A.已知2H2(g)+O2(g) ===2H2O(g) △H=-483.6 kJ/mol,则氢气的
标准燃烧热为241.8 kJ |
| B.已知C(石墨,s) === C(金刚石,s);△H>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq) ===NaCl(aq)+H2O(l);△H=-57.4 kJ/mol |
| D.已知2C(s)+2O2(g) ===2CO2(g);△H1。2C(s)+O2(g)=2CO(g);△H2。则△H1>△H2 |
题号:3232486
题型:选择题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】以下一定能说明化学平衡发生移动的是
| A.正、逆反应速率改变 | B.加入催化剂 |
| C.增大压强 | D.反应转化率的改变 |
题号:4311192
题型:选择题
难易度:一般
日期:2014-10-25
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】已知化学反应A
2(g) + B
2(g) = 2AB(g)的能量变化如图所示,下列叙述正确的是
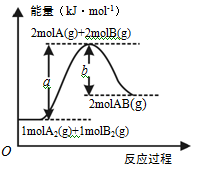
| A.每生成2分子AB吸收bkJ热量 |
| B.该反应热△H=(b -a)kJ·mol-1 |
| C.反应物的总能量低于生成物的总能量 |
| D.断裂1molA—A和1molB—B键,放出akJ能量 |
题号:3232458
题型:填空题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】(6分)降低大气中CO
2的含量及有效利用CO
2,目前已引起各国普遍重视。
(1)在载人航天器的生态系统中,不仅要求分离去除CO
2,还要求提供充足的O
2。某种电化学装置可实现如下转化:2CO
2=2CO+O
2,CO可用作燃料。已知该反应的阳极反应为:4OH
--4e
-=O
2↑+2H
2O,则阴极反应式为
。
(2)工业上有一种方法是用CO
2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1 mol CO
2和3 mol H
2,在500℃下发生反应:
CO
2(g)+3H
2(g)

CH
3OH(g)+H
2O(g) 。
实验测得CO
2(g)和CH
3OH(g)的浓度随时间变化如下图1所示。
①图2是改变温度时H
2的化学反应速率随时间变化的示意图,则该反应的正反应
是
(填“吸热”或“放热”)反应。

②500℃达平衡时,CH
3OH的体积分数为
。
题号:3232459
题型:填空题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】(8分)(1)将反应2H
2(g)+O
2(g)=2H
2O(1) △H<0,以KOH溶液为电解质溶液,设计一个原电池,其负极反应为:
。
(2)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:

①若X和Y均为惰性电极,a为CuSO
4溶液,则电解时的化学反应方程式为:
。
通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为
。
②若X、Y分别为铁和铜,a仍为CuSO
4溶液,则Y极的电极反应式为
。
题号:3232460
题型:填空题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】(8分)一定温度下,在一个10L密闭容器中只投反应物发生某可逆反应,其平衡常数表达式为K=

,请回答下列问题:
(1)该反应的化学方程式为___________________________________;若温度升高,K增大,则该反应是____反应(填“吸热”或“放热”)。
(2)能判断该反应一定达到平衡状态的是__________(填字母序号)。
| A.υ正(H2O)=υ逆(H2) |
| B.容器中气体的平均相对分子质量不随时间改变 |
| C.消耗nmolH2的同时消耗nmolCO |
| D.容器中物质的总物质的量不随时间改变 |
(3)该反应的υ
正随时间变化的关系如图,在t
2时改变了某种条件,改变的条件可能是_________________________、________________________。

题号:3232461
题型:填空题
难易度:较难
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】(10分)某兴趣小组利用如图所示装置进行实验。

(1)断开K
2、闭合K
1,U形管内除电极上有气泡外,还可观察到的现象是
;阳极电极反应式为
。当电路中转移0.001mol电子时,右侧注射器最多可以收集到气体
mL
(折算为标准状况)。
(2)断开K
2、闭合K
1一段时间,待注射器中充有一定量的气体后,断开K
1、闭合K
2,此时装置内化学能转化为电能。实现能量转化的化学方程式为
;
(3)假设实验装置不漏气,当(2)中注射器内气体全部参加反应后,U形管内的溶液理论上
(填“能”或“不能”)恢复原样。
题号:3232462
题型:填空题
难易度:一般
日期:2014-10-24
来源:【百强校】2014-2015学年福建三明市一中高二上第一次月考化学试卷(带解析)
【题文】(10分)发射卫星时可用肼(N
2H
4)为燃料和二氧化氮(NO
2)作氧化剂,两者反应生成氮气和气态
水。已知:
N
2(g)+2O
2(g)===2NO
2(g) ΔH=+67.7 kJ·mol
-1①
N
2H
4(g)+O
2(g)===N
2(g)+2H
2O(g)ΔH=-543 kJ·mol
-1②

H
2(g)+

F
2(g)===HF(g)ΔH=-269 kJ·mol
-1③
H
2(g)+

O
2(g)===H
2O(g) ΔH=-242 kJ·mol
-1④
(1)肼和二氧化氮反应的热化学方程式为______________________________________
(2)有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大,试写出肼和氟气反应的热化学方程式:____________________________________________________

 H2(g)+I2(g),增大平衡体系的压强(压缩体积),可使体系颜色变深
H2(g)+I2(g),增大平衡体系的压强(压缩体积),可使体系颜色变深 cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是
cC中,物质的含量A%和C%随温度的变化曲线如图所示,下列说法正确的是 
 Fe(s) + CO2(g) ΔH ="a" kJ/mol (a >0),该温度下K=0.263,下列有关该反应的说法正确的是
Fe(s) + CO2(g) ΔH ="a" kJ/mol (a >0),该温度下K=0.263,下列有关该反应的说法正确的是

 2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:
2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:

 N2O4(g)△H=﹣57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
N2O4(g)△H=﹣57kJ/mol,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如下图所示。下列说法正确的是
 A2(g) +3B2(g) ; ΔH>0,下列图像正确的是
A2(g) +3B2(g) ; ΔH>0,下列图像正确的是
 2Z(g);ΔH<0
2Z(g);ΔH<0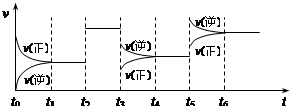
 pC(气)达平衡后, 温度一定时, 将气体体积压缩到原来的一半, 当重新达平衡时, C的浓度为原来的1.9倍, 下列说法不正确的是
pC(气)达平衡后, 温度一定时, 将气体体积压缩到原来的一半, 当重新达平衡时, C的浓度为原来的1.9倍, 下列说法不正确的是 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率 2SO3(g),能增大正反应速率且提高O2的转化率的措施是
2SO3(g),能增大正反应速率且提高O2的转化率的措施是 , 恒容时,温度升高,H2浓度减小。下列说法正确的是
, 恒容时,温度升高,H2浓度减小。下列说法正确的是 CO2 + H2
CO2 + H2 2Z(g) ΔH<0,达到平衡时,下列说法正确的是
2Z(g) ΔH<0,达到平衡时,下列说法正确的是 )
)
 CH3OH(g)+H2O(g) 。
CH3OH(g)+H2O(g) 。

 ,请回答下列问题:
,请回答下列问题:

 H2(g)+
H2(g)+ F2(g)===HF(g)ΔH=-269 kJ·mol-1③
F2(g)===HF(g)ΔH=-269 kJ·mol-1③ O2(g)===H2O(g) ΔH=-242 kJ·mol-1④
O2(g)===H2O(g) ΔH=-242 kJ·mol-1④