| A.浓硫酸和水 | B.生石灰和水 | C.氯化铵和水 | D.氯化钠和水 |
| A.AlCl3 | B.KHCO3 | C.Fe2(SO4)3 | D.NH4HCO3 |
| A.等于7 | B.大于等于7 | C.小于等于7 | D.无法判断 |
| A.溶解度的大小 | B.属于离子化合物还是共价化合物 |
| C.是否存在电离平衡 | D.导电性的强弱 |
| A.以酚酞作指示剂 |
| B.锥形瓶含有少量水 |
| C.滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.滴定前仰视滴定管读数,滴定后平视刻度读数 |
| A.Na+、Cu2+、Cl-、SO42― | B.Ba2+、K+、OH-、NO3― |
| C.H+、Al3+、NH4+、CO32― | D.Na+、Ca2+、Cl-、HCO3― |
| 酸 | HX | HY | HZ | ||||||||||||||||||||||||||||||
| 浓度mol/L | 0,1 | 0.5 | 0.9 | 1 | 1 | ||||||||||||||||||||||||||||
| 电离度% | 0.3 | 0.15 | 0.1 | 0.3 | 10
题号:4366542
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】某探究小组在某温度下测定溶液的pH值时发现,0.01mol·L-1的NaOH溶液中,由水电离出的c(H+)·c(OH-)=10-22(mol·L-1)2,则该小组在该温度下测得0.1mol·L-1的NaOH溶液pH值应为( )
题号:4366543
题型:选择题
难易度:较易
日期:2013-06-28
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是( )
题号:4366544
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】下图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。下列判断正确的是( ) 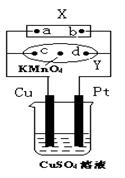
题号:4366549
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】某学生的实验报告所列出的下列数据中合理的是( )
题号:4366550
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为( ) A. A>B; B. A=10-4 B; . B=10-4 A; D. A="B "
题号:4366551
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】物质的量浓度相同的三种盐,NaX、NaY、NaZ的溶液,其中PH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
题号:4366552
题型:选择题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】反应N2O4(g)  2NO2(g);△H=" +57" kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( ) 2NO2(g);△H=" +57" kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( ) A.A、C两点的反应速率:A>C B.A、C两点气体的颜色:A深,C浅 C.由状态B到状态A,可以用加热的方法 D.A、C两点气体的平均相对分子质量:A>C
题号:4366545
题型:填空题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】 (1)证明该一元酸是不是盐酸。(简要写出所用试剂、步骤及现象和结论) 。 (2)探究HA是强酸还是弱酸:取上述HA和BOH的溶液各20mL混合后溶液的pH=5,试推测HA是强酸还是弱酸。你的结论是 ,理由是 。 (3)若HA是强酸、BOH是强碱,现将此HA溶液和BOH溶液按一定体积比混合后测得溶液的pH=4(设混合后溶液的体积变化忽略不计)。则混合时酸和碱的体积之比为V(HA):V(BOH)= 。
题号:4366546
题型:填空题
难易度:较易
日期:2013-07-22
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】25℃时,(1)、将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<” )。 (2)、pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 , 溶液中c(Na+) c(CH3COO-) (3)、物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。 (4)、将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。 (5)、相同物质的量浓度的NH4HSO4和(NH4)2SO4溶液,都呈 性,前者显酸性的主要原因是 ;后者显酸性的主要原因是 。
题号:4366547
题型:填空题
难易度:较易
日期:2013-03-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(2)若上述关系中C是正确的,则溶液中溶质的化学式是 。 (3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)(填“>”、“<”、或“=”,下同) c(NH3·H2O),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+) c(Cl-)。
题号:4366553
题型:填空题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为(填序号)__ __。 A.9 B.13 C.11~13之间 D.9~11之间 (2)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)__ ___。 A.氨水与氯化铵发生化学反应; B.氯化铵溶液水解显酸性,增加了c(H+); C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH―)减小; (3)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失), ①__ _、_ __和_ __三种粒子的物质的量之和等于0.1mol。 ②_ __和_ __两种粒子的物质的量之和比OH―多0.05mol。
题号:4366554
题型:填空题
难易度:较易
日期:2010-12-27
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】已知2SO2 (g)+ O2(g) 2SO3(g) △H =-196kJ·mol-1,5000C时将2mol SO2和1molO2装入一体积恒定的10L密闭容器中,2分钟(t1)时达到平衡。如下图所示:高考资源  网 网请回答下列问题: (1)用O2表示2分钟内该反应的平均反应速率为 mol·L-1·min-1。计算500℃时该反应的平衡常数K= 。 (2)上图表示该反应在时刻t1达到平衡后,时刻t2因改变某个条件而发生变化的情况: 图中时刻t2发生改变的条件可能是 (写一个即可)。 (3)在上述条件下起始装入的SO2和O2各2mol,达平衡后设SO2的转化率为x,列出求x的方程 。(不必求出x) (4)某温度时,该反应的平衡常数K=5000,则该温度 500℃(填“>”、“<”、“=”)。 (5)500℃时,若起始装入的SO2、O2和SO3分别为0.2mol、y mol、wmol,达到平衡时各组分的含量与第(3)完全相同,则y= mol。刚开始时反应向 (填“正”或“逆”)反应方向进行。
题号:4366548
题型:计算题
难易度:较易
日期:2012-05-21
来源:2010年福建省四地六校联考高二上学期第三次月考化学试卷
【题文】常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1︰2的体积比混合,所得溶液的pH=12。用上述NaOH溶液滴定pH=3的某一元弱酸溶液20ml,达到终点时消耗NaOH溶液13ml,试求: (1)NaOH溶液的物质的量浓度 (2)此一元弱酸的物质的量浓度 (3)求此条件下该一元弱酸的电离平衡常数 | ||||||||||||||||||||||||||||