适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2017年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2017年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2017年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2017年')}}上传日期:2017-04-17题数:21
提示:单击题文可显示答案与解析。
题号:1218888
题型:选择题
难易度:一般
日期:2016-12-21
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】对①100 mL 0.1 mol/L NaHCO
3,②100mL 0.1 mol/L Na
2CO
3两溶液叙述正确的是( )
| A.两溶液中c(OH--):①>② |
| B.两溶液中阳离子数目:②是①的2倍 |
| C.②溶液中:c(HCO3--)<c(H2CO3) |
| D.①溶液中:c(CO32-)<c(H2CO3) |
题号:1222702
题型:选择题
难易度:较难
日期:2016-12-15
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】如图曲线 a 和 b 是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是 ( )。
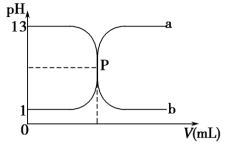
| A.盐酸的物质的量浓度为 1 mol·L-1 |
| B.P 点时恰好完全中和,溶液呈中性 |
| C.曲线 a 是盐酸滴定氢氧化钠溶液的滴定曲线 |
| D.酚酞不能用作本实验的指示剂 |
题号:1231604
题型:选择题
难易度:较难
日期:2016-12-06
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】溶液的酸碱性可用酸度(AG)表示,已知AG =lg

,室温下将0.01mol•L
﹣l盐酸逐滴滴入20.00mL 0.01 mol•L
﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
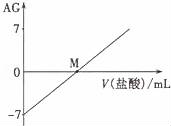
| A.室温下,0.01 mol•L﹣l盐酸的AG=12 |
| B.M点时溶液中:c(NH4+)=c(Cl﹣) |
| C.M点加入盐酸的体积大于20.00 mL |
| D.M点以后NH4+的水解程度逐渐增大 |
题号:3173164
题型:选择题
难易度:较易
日期:2016-01-28
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列说法不正确的是( )
| A.Ksp只与难溶电解质的性质和温度有关 |
| B.由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C.其他条件不变,离子浓度改变时,Ksp不变 |
| D.两种难溶电解质作比较时,Ksp小的,溶解度一定小 |
题号:3182426
题型:选择题
难易度:一般
日期:2016-01-11
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的K
sp=4×10
-10,下列说法不正确的是

| A.在t ℃时,AgBr的Ksp为4.9×10-13 |
| B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点 |
| C.图中a点对应的是AgBr 的不饱和溶液 |
D.在t ℃时,AgCl(s)+Br-(aq) 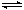 AgBr(s)+Cl-(aq)的平衡常数K≈816 AgBr(s)+Cl-(aq)的平衡常数K≈816 |
题号:3247926
题型:选择题
难易度:一般
日期:2014-04-19
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】有四种物质的量浓度相等、且都由一价阳离子A
+和B
+及一价阴离子X
-和Y
-组成的盐
溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
题号:3267076
题型:选择题
难易度:较易
日期:2013-07-18
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列物质中不属于电解质的是
| A.固体氯化钾 | B.液态氯化氢 | C.气态硝酸 | D.作电极的碳棒 |
题号:3315310
题型:选择题
难易度:一般
日期:2017-01-14
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】常温下,将pH=3的盐酸a L分别与下列三种溶液混合后,混合液均呈中性:
①1×10
-3mol·L
-1的氨水b L
②c(OH
-)=1×10
-3mol·L
-1的氨水c L
③c(OH
-)=1×10
-3mol·L
-1的Ba(OH)
2溶液d
其中a、b、c、d的关系正确的是()
| A.a=b>c>d | B.b>a=d>c | C.a=b>d>c | D.c>a=d>b |
题号:3541539
题型:选择题
难易度:较难
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】一定温度下,下列溶液的离子浓度关系式正确的是( )
| A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol•L-1 |
| B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |
| C.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
| D.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-) |
题号:3541540
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列说法正确的是( )
| A.25℃时,0.1mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
| B.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量)后者用时少 |
| C.将氢氧化钠溶液和氨水各稀释一倍,两者的c(OH-)均减少到原来的一半 |
| D.常温下,pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合,溶液显碱性 |
题号:3541541
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】25℃时,由水电离出
c(OH
-)=1×10
-11mol/L 的溶液中,可能能大量共存的离子组是( )
| A.Al3+、Na+、SO42― 、AlO2- | B.Na+、CH3COO-、K+、Cu2+ |
| C.K+、I-、SO42―、Na+ | D.Fe2+、Cl-、Na+、HCO3― |
题号:3541542
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列不能证明一元酸HA为弱酸的是( )
| A.NaA溶液的pH>7(室温下) |
| B.HA溶液能与CH3COONa溶液反应生成CH3COOH |
| C.0.1 mol/L的HCl和HA溶液,前者的导电能力明显更强 |
| D.跟同浓度的盐酸比较和锌反应较慢 |
题号:3541543
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列实验符合要求的是 ( )
| A.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
| B.用托盘天平称取NaOH固体时需先在左右两盘中各放上大小相同的纸片 |
| C.用玻璃棒蘸取溶液滴在表面皿上的已润湿pH试纸上测得其pH为12 |
| D.若25 mL滴定管中液面的位置在刻度为10mL处,则滴定管中液体的体积一定大15 mL |
题号:3541544
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列物质的溶液中,所含离子种类最多的是( )
| A.K2S | B.NaHCO3 | C.Na3PO4 | D.AlCl3 |
题号:3541545
题型:选择题
难易度:较易
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】在CH
3COOH

H
++CH
3COO
-的电离平衡中,要使电离平衡向左移动,应采取的措施是( )
| A.加冰醋酸 | B.加水 | C.加CH3COONa | D.加NaOH |
题号:3541546
题型:选择题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】下列应用与盐类的水解无关的是( )
| A.为了较好地保存FeCl3溶液加入少量HCl |
| B.FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |
| C.NaCl可用作防腐剂和调味剂 |
| D.实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃 |
题号:1303520
题型:实验题
难易度:较难
日期:2016-10-12
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol/L醋酸溶液,用0.2 mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol/L醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和
。
(2)为标定某醋酸溶液的准确浓度,用0.2000 mol/L NaOH溶液对20.00 mL醋酸溶液进行滴定(酚酞作指示剂),几次滴定消耗NaOH溶液的体积如下:
实验序号
| 1
| 2
| 3
| 4
|
消耗NaOH溶液的体积(ml)
| 20.05
| 20.00
| 18.80
| 19.95
|
则该醋酸溶液的准确浓度为
mol/L。(保留小数点后四位)
(3)判断滴定终点的方法是
。
(4)下列操作中可能使所测醋酸溶液的浓度数值偏低的是
(填字母序号)。
A.碱式滴定管未用标准液润洗就直接注入标准液
B.滴定前盛放醋酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.碱式滴定管在滴定前有气泡,滴定后气泡消失
D.量取醋酸体积时,开始俯视读数,滴定结束时仰视读数
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
醋酸浓度(mol·L-1)
| 0.0010
| 0.0100
| 0.0200
| 0.1000
|
pH
| 3.88
| 3.38
| 3.23
| 2.88
|
(5)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
。
题号:3541535
题型:填空题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】按要求完成下列填空:
(1)常温时,AlCl
3的水溶液呈________(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):________________________。AlCl
3溶液蒸干并灼烧得到的物质是__________(填化学式)。
(2)泡沫灭火器灭火时发生反应的离子方程是____________;
(3)为了使Na
2S溶液中
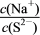
的比值变小,可加入的物质是_______
| A.适量盐酸 | B.适量NaOH溶液 |
| C.适量KOH溶液 | D.适量蒸馏水 |
(4)已知25℃ 时,Ksp[Cu(OH)
2]=2×10
-20,某CuSO
4溶液里c(Cu
2+)=0.02mol•L
-1,如要生成Cu(OH)
2沉淀,应调整溶液的pH,使之大于______________。
(5)已知
c(Ca
2+)≤10
-5 mol·L
-1时可视为沉淀完全;
Ksp(CaCO
3)=4.96×10
-9。在Ca(NO
3)
2溶液中加入(NH
4)
2CO
3溶液后过滤,若测得滤液中
c(CO
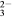
)=10
-3 mol·L
-1,则Ca
2+是否沉淀完全?________(填“是”或“否”)。
题号:3541536
题型:填空题
难易度:较难
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】Ⅰ.现有NH4Cl和氨水组成的混合溶液。请回答下列问题(填“>”、“<”或“=”):
(1)若溶液的pH=7,则该溶液中c(NH4+)________c(Cl-)。
(2)若溶液中pH>7,则该溶液中c(NH4+)________c(Cl-)。
Ⅱ.常温下有浓度均为0.1mol•L-1的三种溶液:①Na2CO3、②NaHCO3、③HCl
(1)溶液②中按物质的量浓度由大到小顺序排列该溶液中各离子浓度__________________;
(2)溶液②中,c(CO32-)+c(HCO3-)+c(H2CO3)= __________mol•L-1;
(3)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)=_____mol•L-1。
题号:3541537
题型:填空题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】请回答下列问题。
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
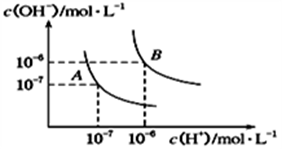
①100℃时1 mol·L
-1的NaOH溶液中,由水电离出的
c(H
+)=______mol·L
-1,
Kw(25℃)________
Kw(100℃) (填“>”、“<”或“=”)。
②25℃时,向水的电离平衡体系中加入少量 NH
4Cl固体,对水的电离平衡的影响是_____(填“促进”、“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式
| 电离平衡常数(25℃)
|
HCN
| K=4.9×10-10
|
CH3COOH
| K=1.8×10-5
|
H2CO3
| K1=4.3×10-7、K2=5.6×10-11
|
①25℃时,有等浓度的a.NaCN溶液 b.CH
3COONa 溶液 c.Na
2CO
3溶液,三种溶液的pH由大到小的顺序为_____________________;(填序号)
②25℃时,等浓度的CH
3COOH溶液和NaOH溶液等体积混合,则
c(Na
+)__________
c(CH
3COO
-)(填“>”、“<”或“=”);
(3)25℃,两种酸的电离平衡常数如下表。
| Ka1
| Ka2
|
H2SO3
| 1.3×10-2
| 6.3×10-4
|
H2CO3
| 4.2×10-7
| 5.6×10-11
|
①HSO
3-的电离平衡常数表达式K=_________。
②H
2SO
3溶液和NaHCO
3溶液反应的主要离子方程式为__________________。
题号:3541538
题型:填空题
难易度:一般
日期:2017-04-10
来源:2016-2017学年福建省泉州市南安第一中学高二下学期第一次阶段考试(3月)化学试卷(带解析)
【题文】Ⅰ.已知室温时,0.1 mol/L某一元酸HA在水中有0.1%发生电离,回答下列问题:
(1)该溶液中c(H+)=___________。
(2)HA的电离平衡常数K=______________;
(3)由HA电离出的c(H+)约为水电离出的c(H+)的________倍。
Ⅱ.室温下,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。
(1)如果加入蒸馏水,就加入__________mL
(2)如果加入pH = 10的NaOH溶液,应加入_________ mL
(3)如果加入0.008 mol/L HCl溶液,应加入___________ mL

 ,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0.01 mol•L﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0.01 mol•L﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是

 AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816 H++CH3COO-的电离平衡中,要使电离平衡向左移动,应采取的措施是( )
H++CH3COO-的电离平衡中,要使电离平衡向左移动,应采取的措施是( )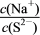 的比值变小,可加入的物质是_______
的比值变小,可加入的物质是_______ )=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
)=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。