适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2017年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2017年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2017年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2017年')}}上传日期:2017-07-01题数:22
提示:单击题文可显示答案与解析。
题号:1401551
题型:选择题
难易度:一般
日期:2016-07-08
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】若某基态原子的外围电子排布式为4d
15s
2,则下列说法正确的是()
| A.该元素基态原子中共有3个电子 |
| B.该元素原子核外有5个电子层 |
| C.该元素原子最外层共有3个电子 |
| D.该元素原子M能层共有8个电子 |
题号:3242766
题型:选择题
难易度:一般
日期:2014-06-20
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】溴酸银(AgBrO
3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
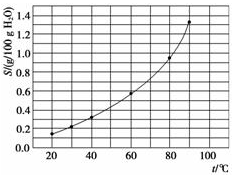
| A.溴酸银的溶解时放热过程 |
| B.温度升高时溴酸银溶解速度加快 |
| C.60 ℃时溴酸银的Ksp约等于6×10-4 |
| D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
题号:3250914
题型:选择题
难易度:一般
日期:2014-04-01
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】下列各组表述中,两个微粒不属于同种元素原子的是( )。
| A.3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2的原子 |
| B.2p能级无空轨道,且有一个未成对电子的基态原子和原子的最外层电子排布为2s22p5的原子 |
| C.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p64s2的原子 |
D.最外层电子数是核外电子总数的 的原子和最外层电子排布为4s24p5的原子 的原子和最外层电子排布为4s24p5的原子 |
题号:3254205
题型:选择题
难易度:一般
日期:2014-03-14
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是 ,
| A.pH=3的硝酸和pH=11的氢氧化钠溶液 |
| B.pH=3的盐酸和pH=11的氨水 |
| C.pH=3的硫酸和pH=11的氢氧化钠溶液 |
| D.pH=3的醋酸和pH=11的氢氧化钠溶液 |
题号:3267269
题型:选择题
难易度:较易
日期:2013-07-17
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】第四周期元素原子中未成对电子数最多可达( )
题号:3288784
题型:选择题
难易度:一般
日期:2012-08-03
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】已知某元素+3价离子的电子排布式为1s
22s
22p
63s
23p
63d
5,该元素在周期表中的位置是()
| A.第3周期第Ⅷ族 | B.第3周期第ⅤB族 |
| C.第4周期第Ⅷ族 | D.第4周期第ⅤB族 |
题号:3302360
题型:选择题
难易度:一般
日期:2011-12-29
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】下列原子的外围电子排布式正确的是
| A.Zn:3d104s2 | B.Cr:3d44s2 | C.Ga:4s24p2 | D.S:3p4 |
题号:3304421
题型:选择题
难易度:一般
日期:2011-12-10
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】具有下列电子排布式的原子中,半径最大的是( )
| A.1s22s22p63s23p2 | B.1s22s22p3 |
| C.1s22s22p2 | D.1s22s22p63s23p4 |
题号:3840053
题型:选择题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】加热蒸干下列溶液后,能得到原溶液中溶质的是( )
| A.AlCl3 | B.CuSO4 | C.NaHCO3 | D.(NH4)2S |
题号:3840054
题型:选择题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】下列化学符号表示正确的是( )
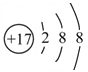
A.钾原子的原子结构示意图: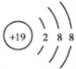 |
| B.铜原子的外围电子排布式:3d104s1 |
| C.铍原子的电子式: :Be: |
D.碳原子的原子轨道表示式: |
题号:3840055
题型:选择题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】室温时,M(OH)
2(S)
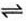
M
2+(aq)+2OH
-(aq),

=a;c(M
2+)=bmol·L-1时,溶液的pH等于( )
A. lg( lg( ) ) | B. lg( lg(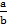 ) ) | C.14+ lg( lg(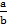 ) ) | D.14+ lg( lg( ) ) |
题号:3840056
题型:选择题
难易度:较难
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】己知某溶液中含有C1
-, Br
-和CrO
42-,浓度均为0.010mo1·L
-,向该溶液中逐滴加入0.010mol·L
-1的AgNO
3溶液时,三种阴离子产生沉淀的先后顺序为(K
sp(AgCl)=1.56
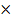
10
-10, K
sp(AgBr)=7.7
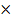
10
-13,K
sp(Ag
2CrO
4)=9.0
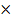
10
-12)
| A.C1-、Br-、CrO42- | B.CrO42-、Br-、C1- | C.Br-、C1-、CrO42- | D.Br-、CrO42-、C1- |
题号:3840057
题型:选择题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】人体血液内的血红蛋白(Hb)易与O
2结合生成HbO
2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO
2==O
2+HbCO ,37 ℃时,该反应的平衡常数K="220" 。HbCO的浓度达到HbO
2浓度的0.02倍,会使人智力受损。下列结论错误的是 ( )
A.CO与HbO2反应的平衡常数K=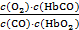 |
| B.人体吸入的CO越多,与血红蛋白结合的O2越少 |
| C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损 |
| D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动 |
题号:3840058
题型:选择题
难易度:较易
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
题号:4358194
题型:选择题
难易度:一般
日期:2011-04-20
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
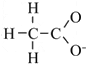
【题文】常温下,将醋酸和氢氧化钠溶液混合,所得溶液pH=7,则此溶液中
| A.c(CH3COO-)>c(Na+) | B.c(CH3COO-<c(Na+) |
| C.c(CH3COO-)=c(Na+) | D.无法确定c(CH3COO-)与c(Na+)的关系 |
题号:4749553
题型:选择题
难易度:一般
日期:2017-07-24
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】中科大陈乾旺教授等人发明
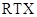
合成金刚石的新方法,化学原理为:①
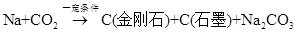
(未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②
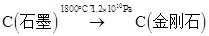
。以下表述正确的是( )
| A.反应①中既有旧化学键的断裂又有新化学键的形成 |
| B.新方法利用的是物理变化,旧方法利用的是化学变化 |
C.在反应①中每生成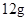 金刚石需要消耗 金刚石需要消耗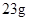 金属钠 金属钠 |
| D.反应①和反应②中所得的金刚石都是还原产物 |
题号:1301385
题型:实验题
难易度:容易
日期:2016-10-12
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】氯化锶晶体在工业上常用作铝的缓蚀剂。工业上一般用难溶于水的的碳酸锶(SrCO
3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体(SrCl
2•6H
2O)的过程为:
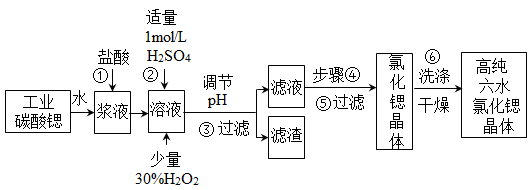
已知:Ⅰ.SrCl
2•6H
2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水;
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
| Fe(OH)3
| Fe(OH)2
|
开始沉淀的pH
| 1.5
| 6.5
|
沉淀完全的pH
| 3.7
| 9.7
|
(1)操作①在实际工业生产中常常把碳酸锶粉碎并加以搅拌,其目的是
。碳酸锶与盐酸反应的化学方程式为__________________。
(2)酸性条件下,加入30% H
2O
2溶液,将Fe
2+氧化成Fe
3+,其离子方程式为
。能否用新制氯水代替双氧水________(填“能”或“否”)。
(3)在步骤②~③的过程中,将溶液的pH值由1调节至
;宜用的试剂为_______。
A.1.5 B.4 C.9.7 D.氧化钠
E氢氧化锶粉末 F碳酸钠晶体 G氧化锶粉末
(4)操作③中所得滤渣的主要成分是
__________(填化学式)。
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是
__________。
(6)步骤⑥中,洗涤氯化锶晶体最好选用___________。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
题号:3840049
题型:填空题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回收处理该废电池可以得到多种化工原料,有关数据下图所示:
化合物
| Zn(OH)2
| Fe(OH)2
| Fe(OH)3
|
Ksp近似值
| 10-17
| 10-17
| 10-39
|
用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入新硫酸和双氧水,溶解,铁变为_____加碱调节PH为_____,铁刚好完全沉淀(离子浓度小于1×10
-5mol/L时,即可认为该离子沉淀完全)。继续加碱调节pH为______,锌开始沉淀(假定Zn
2+浓度为0.1mol/L)。若上述过程不加双氧水的后果是_____________,原因是__________________________。
题号:3840050
题型:填空题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】(1)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。
已知浓缩液中含有I
-、Cl
-等离子,取一定量的浓缩液,向其中滴加AgNO
3溶液,当AgCl开始沉淀时,溶液中
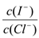
为:_______,已知Ksp(AgCl)=1.8×10
-10,Ksp(AgI)=8.5×10
-17。
(2)在化学分析中采用K
2CrO
4为指示剂,以AgNO
3标准溶液滴定溶液中Cl
−,利用Ag
+与CrO
42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl
−恰好沉淀完全(浓度等于1.0×10
−5 mol·L
−1)时,溶液中c(Ag
+)为_______mol·L−1,此时溶液中c(CrO
42−)等于__________mol·L
−1。(已知Ag
2CrO
4、AgCl的Ksp分别为2.0×10
−12和2.0×10
−10)。
题号:3840051
题型:填空题
难易度:一般
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】(1)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,则基态Ge原子的核外电子排布式为[Ar]____________,有__________个未成对电子。
(2)碳及其化合物广泛存在于自然界中,则处于一定空间运动状态的电子在原子核外出现的概率密度分布可用__________形象化描述。在基态原子中,核外存在_______对自旋相反的电子。
(3)基态铁原子有 ______个未成对电子,三价铁离子的电子排布式为:____________,可用硫氰化钾奉验三价铁离子,形成配合物的颜色为____________
(4)基态Si原子中,电子占据的最高能层符号_____,该能层具有的原子轨道数为_____、电子数为________ 。
题号:3840052
题型:填空题
难易度:较易
日期:2017-06-30
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】写出下列原子的轨道表示式
(1) O _________________________________;
(2) Al _________________________________。
题号:3620067
题型:简答题
难易度:一般
日期:2017-05-08
来源:福建省莆田市第七中学2016-2017学年高二下学期第二次月考化学试题
【题文】原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________周期第________族。
(2)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:____________。
(3)写出3p轨道上只有2个未成对电子的元素的符号:____________、____________。

 的原子和最外层电子排布为4s24p5的原子
的原子和最外层电子排布为4s24p5的原子

 M2+(aq)+2OH-(aq),
M2+(aq)+2OH-(aq), =a;c(M2+)=bmol·L-1时,溶液的pH等于( )
=a;c(M2+)=bmol·L-1时,溶液的pH等于( ) lg(
lg( )
) lg(
lg(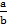 )
) lg(
lg(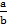 )
) lg(
lg( )
) 10-10, Ksp(AgBr)=7.7
10-10, Ksp(AgBr)=7.7 10-13,Ksp(Ag2CrO4)=9.0
10-13,Ksp(Ag2CrO4)=9.0 10-12)
10-12)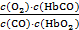
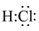
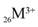
 合成金刚石的新方法,化学原理为:①
合成金刚石的新方法,化学原理为:①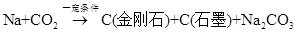 (未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②
(未配平)该方法比1955年人工首次制得金刚石的旧方法容易得多。②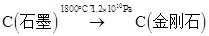 。以下表述正确的是( )
。以下表述正确的是( )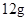 金刚石需要消耗
金刚石需要消耗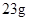 金属钠
金属钠
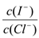 为:_______,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_______,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。