适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2015年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2015年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2015年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2015年')}}上传日期:2016-01-28题数:20
提示:单击题文可显示答案与解析。
题号:3173109
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】 LiOH是制备锂离子电池的材料,可由电解法制备。工业上利用如图装置电解制备 LiOH,两电极区电解液分别为LiOH和LiCl溶液,下列叙述正确的是
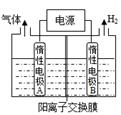
| A.B极区电解液为LiOH溶液 |
| B.电极每产生22.4L气体,电路中转移2mole- |
| C.电解过程中Li+迁移入B电极区、OH-迁移入A电极区 |
D.电解池中总反应方程式为:2HCl 2H2↑+Cl2↑ 2H2↑+Cl2↑ |
题号:3173110
题型:选择题
难易度:一般
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)

2Z(g)+W(s)
Δ
H<0,下列叙述正确的是
| A.平衡常数K值越大,X的转化率越小 |
| B.若混合气体的平均摩尔质量保持不变,则反应达到平衡 |
| C.达平衡时继续通入气体X,平衡正移则上述ΔH减小 |
| D.升高温度或增大压强都有利于该反应平衡向逆反应方向移动 |
题号:3173111
题型:选择题
难易度:容易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】已知:A(g)+3B(g)

M(g)+N(g);
△H=﹣49.0kJ·mol
-1。一定条件下,向体积为2L的密闭容器中充入2mol A和6molB,测得A和M的浓度随时间变化曲线如图所示。下列叙述中正确的是
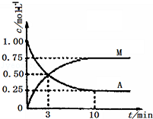
A.充分反应后该反应放出98 kJ的热量
B.10min后,升高温度能使n(M)/ n(A)增大
C.3min时生成3molB的同时生成1mol M
D.反应到达平衡时刻B的转化率为75%
题号:3173112
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】一定量的混合气体,在密闭容器中发生如下反应:xA(g)+yB(g)

zC(g),达到平衡后测得A气体的浓度为1mol·L
-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.7mol·L
-1,则下列叙述正确的是
| A.平衡向正反应方向移动 | B.x + y = z |
| C.C的体积分数升高 | D.B的转化率降低 |
题号:3173113
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】已知断裂1molH—H键所需要的能量为436 kJ,断裂1molN—H键所需要的能量为391 kJ。根据热化学方程式:N
2(g)+3H
2(g)

2NH
3(g) Δ
H=-92.4 kJ·mol
-1,则断裂1molN≡N键所需要的能量是
| A.431 kJ | B.945.6 kJ | C.649 kJ | D.896 kJ |
题号:3173114
题型:选择题
难易度:容易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
题号:3173115
题型:选择题
难易度:较难
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】如图所示,
△H1=-393.5kJ·mol
-1,
△H2=-395.4 kJ·mol
-1,下列说法正确的是
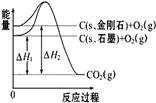
| A.C(s、石墨)═C(s、金刚石)△H="+1.9" kJ·mol-1 |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
| D.1 mol石墨的能量比1 mol金刚石的总能量大 |
题号:3173116
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】铅蓄电池的电池反应为 Pb(s)+PbO
2(s)+2H
2SO
4(aq)

2PbSO
4(s)+2H
2O(l),下列说法错误的是
| A.放电时电解质溶液的H+浓度逐渐减小 |
| B.利用铅蓄电池电解饱和食盐水制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少0.10 mol |
| C.充电时阴极的电极反应为 PbSO4(s) + 2e-="Pb(s)" + SO42-(aq) |
| D.放电时负极材料质量减小 |
题号:3173117
题型:选择题
难易度:一般
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】某温度时,N
2(g)+3H
2(g)

2NH
3(g)的平衡常数
K=a, 则此温度下,
NH
3(g)

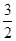
H
2(g)+
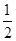
N
2(g)的平衡常数为
| A.aˉ½ | B.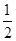 a a | C.a½ | D.aˉ2 |
题号:3173118
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】用石墨电极分别电解下列足量物质的水溶液一段时间后,向剩余电解质溶液中加入一定量的一种物质(括号内),溶液能恢复到与原来溶液完全一样的是
| A.CuCl2(HCl) | B.NaOH(NaOH) | C.NaCl(HCl) | D.CuSO4[Cu(OH)2] |
题号:3173119
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】有关金属腐蚀的叙述正确的是
| A.生铁抗腐蚀能力比纯铁强 |
| B.钢瓶在储存液氯前彻底干燥可减缓腐蚀 |
| C.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| D.常温下浓硝酸比浓盐酸更易使铁腐蚀 |
题号:3173120
题型:选择题
难易度:一般
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】某小组同学进行氢氧化钠与硫酸反应的中和热测定实验时,数值结果小于57.3kJ·mol
-1,产生偏差的原因不可能是
| A.实验装置保温、隔热效果差 |
| B.所用硫酸为浓硫酸 |
| C.玻璃搅拌器改为铜质搅拌器 |
| D.倒完NaOH溶液后,发现装NaOH烧杯内有极少量残留液 |
题号:3173121
题型:选择题
难易度:容易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】下列各图所表示的反应是吸热反应的是
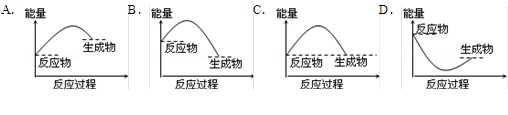
题号:3173122
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】下列说法正确的是
| A.放热反应均是自发反应 |
| B.△S为正值的反应均是自发反应 |
| C.物质的量增加的反应,△S为正值 |
| D.如果△H和△S均为正值,当高温时,反应可能自发进行 |
题号:4303041
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是
①天然气 ② 核能 ③ 石油 ④ 太阳能 ⑤风能 ⑥ 氢能
题号:4303042
题型:选择题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】关于下列装置说法正确的是
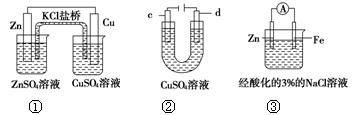
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.用装置②精炼粗铜,电解液浓度保持不变 |
| C.可以用装置②在铜上镀银,c极为银 |
| D.装置③中一段时间后会有Fe(OH)2生成 |
题号:3173105
题型:实验题
难易度:一般
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】研究NO、NO
2、SO
2等大气污染气体的处理具有重要意义。
(1)以石灰石为原料通过系列反应将硫元素以CaSO
4的形式固定,从而降低SO
2的排放.但是煤炭燃烧过程中产生的CO又会与CaSO
4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO
4 (s)+CO (g)

CaO(s)+SO
2 (g)+CO
2 (g)
△H=218.4kJ·mol
-1(反应Ⅰ)
CaSO
4 (s) +4CO (g)

CaS(s) +4CO
2(g)
△H2=﹣175.6kJ·mol
-1 (反应Ⅱ)
结合反应Ⅰ、Ⅱ写出CaSO
4 (s)与CaS (s) 反应的热化学反应方程式
。
(2)NO
2、SO
2气体混合存在氧化物间的相互转化平衡:
NO
2(g)+SO
2(g)

SO
3(g)+NO(g),某活动小组对此反应进行研究实验
| 实验内容
| 实验现象
| 结论
|
①
| 将充有NO2、SO2气体的密闭烧瓶放入热水中
| 气体红棕色加深,一段时间后颜色不再变化
| △H 0(填“>”、“<”或“=”)
|
②
| 在针筒中抽入5mL NO2和5mL SO2气体,封闭针筒前端,充分反应后,将活塞迅速推至5mL处
|
气体红棕色加深并保持不变
|
平衡 (填“向左”、“向右”或“不”)移动
|
③
| 在充有NO2、SO2混合气体的恒容容器中,达平衡后继续通入SO2气体
|
| 平衡向右移动,SO2的转化率 (填“增大”、“减小”或“不变”)
|
(3)工业上用活性炭还原法处理NO,有关反应为:C(s) +2NO(g)

N
2(g) +CO
2(g)。
为了提高NO的转化率,下列的措施可行的是
A.再加入一定量的碳 B.增大压强
C.用碱液吸收气体 D.使用催化剂
(4)用间接电化学法除去NO的原理如图所示。已知电解池的阴极室中溶液呈酸性,阴极的电极反应式为
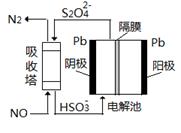
题号:3173106
题型:填空题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:
A(g)+
xB(g)

2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度随时间变化如下图所示。设35min和55min的平衡常数分别为
K1、
K2。
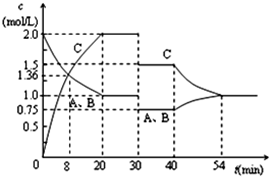
回答下列问题:
(1)反应方程式中的
x=
;20min时的平衡常数
K =
。
(2)8min时A的转化率为
。
(3)30min时改变的条件是
。
(4)若40min时改变的条件是升高温度,则
K1 K2(填“>”或“<”或“=”, 下同)。
(5)能判断反应A(g)+
xB(g)

2C(g),达到化学平衡状态的依据是
(填序号)。
A.恒容容器中压强不变 B.混合气体中
c(A)不变
C.2
v正(A)=
v逆(C) D.2
c(A)=
c(C)
题号:3173107
题型:填空题
难易度:较易
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】氯碱工业是最基本的化学工业之一,它的产品应用广泛。请回答氯碱工业的如下问题:
(1)原料粗盐中常含有泥沙和Ca
2+、Mg
2+、SO
42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na
2CO
3②HCl(盐酸)③BaCl
2,这3种试剂添加的合理顺序是___________(填序号)
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节能30%以上。在这种工艺设计中,相关物料的传输与转化关系示意图如下(其中的电极均为惰性电极,物料进出口未全部标出)。
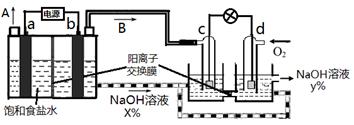
①图中A是
(填化学式),分析比较图示中两处氢氧化钠质量分数x%______y%
(填“>”或“<”或“=”)。
②写出燃料电池中正极上发生的电极反应:
。
③标准状态下,当燃料电池消耗22.4LO
2时,通过电池中阳离子交换膜的阳离子的物质的量为
mol。
④这样设计的主要节(电)能之处在于
。
题号:3173108
题型:填空题
难易度:一般
日期:2016-01-28
来源:2015-2016学年福建省宁德市部分一级达标中学高二上联考化学试卷(带解析)
【题文】材料是人类赖以生存和发展的重要物质基础,铁和碳是生活中常见的材料。
(1)碳可用于制取水煤气:C(s)+H
2O(g)=CO(g)+H
2(g)。相同温度下,在体积均为2L的两个密闭容器(已加入足量的碳)中进行上述反应,反应容器分别用编号A、B表示。
①写出该反应的平衡常数的表达式:
②已知该温度下平衡常数
K="1.5" mol·L
-1,若向A容器中另加入一定量的水蒸气,经过一段时间后达到平衡,此时
c(H
2O)=0.1mol·L
-1、
c(CO)=0.5
mol·L
-1,则
c(H
2)=
mol·L
-1。
③若向B容器中再加入一定量的水蒸气,某一时刻测得体系中物质的量如下:n(H
2O)=0.2mol、n(CO)=0.2mol、 n(H
2)=0.8mol则此时该反应
(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”)。
(2)钢铁在海水中常发生电化学腐蚀,其负极反应式为
;
(3)利用右图装置,可以模拟铁的电化学防护,为减缓铁的腐蚀,若开关K置于b处则Fe应与电源的
极相连。若开关置于a处,则下列可用作X极材料的是
。
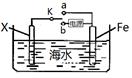
A.Zn B.Cu C.石墨 D.Pt

 2H2↑+Cl2↑
2H2↑+Cl2↑ 2Z(g)+W(s)
2Z(g)+W(s)  M(g)+N(g);△H=﹣49.0kJ·mol-1。一定条件下,向体积为2L的密闭容器中充入2mol A和6molB,测得A和M的浓度随时间变化曲线如图所示。下列叙述中正确的是
M(g)+N(g);△H=﹣49.0kJ·mol-1。一定条件下,向体积为2L的密闭容器中充入2mol A和6molB,测得A和M的浓度随时间变化曲线如图所示。下列叙述中正确的是
 zC(g),达到平衡后测得A气体的浓度为1mol·L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.7mol·L-1,则下列叙述正确的是
zC(g),达到平衡后测得A气体的浓度为1mol·L-1,当恒温下将密闭容器的容积扩大到2倍再达到平衡后,测得A的浓度为0.7mol·L-1,则下列叙述正确的是 2NH3(g) ΔH=-92.4 kJ·mol-1,则断裂1molN≡N键所需要的能量是
2NH3(g) ΔH=-92.4 kJ·mol-1,则断裂1molN≡N键所需要的能量是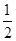 O2(g)═H2O(g)△H1
O2(g)═H2O(g)△H1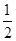 O2(g)═CO (g)△H2
O2(g)═CO (g)△H2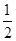 O2(g)═S(s)+H2O(l)△H4
O2(g)═S(s)+H2O(l)△H4
 2PbSO4(s)+2H2O(l),下列说法错误的是
2PbSO4(s)+2H2O(l),下列说法错误的是 2NH3(g)的平衡常数K=a, 则此温度下,
2NH3(g)的平衡常数K=a, 则此温度下,
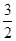 H2(g)+
H2(g)+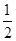 N2(g)的平衡常数为
N2(g)的平衡常数为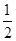 a
a

 CaO(s)+SO2 (g)+CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ)
CaO(s)+SO2 (g)+CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ) CaS(s) +4CO2(g) △H2=﹣175.6kJ·mol-1 (反应Ⅱ)
CaS(s) +4CO2(g) △H2=﹣175.6kJ·mol-1 (反应Ⅱ) SO3(g)+NO(g),某活动小组对此反应进行研究实验
SO3(g)+NO(g),某活动小组对此反应进行研究实验 N2(g) +CO2(g)。
N2(g) +CO2(g)。
 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度随时间变化如下图所示。设35min和55min的平衡常数分别为K1、K2。
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度随时间变化如下图所示。设35min和55min的平衡常数分别为K1、K2。
 2C(g),达到化学平衡状态的依据是 (填序号)。
2C(g),达到化学平衡状态的依据是 (填序号)。
