适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2015年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2015年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2015年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2015年')}}上传日期:2015-04-03题数:20
提示:单击题文可显示答案与解析。
题号:3210687
题型:选择题
难易度:较难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】常温下,电解质溶液的性质与变化是多样的,下列说法正确的是
| A.pH相同的①CH3COONa ②NaClO ③NaOH三种溶液c(Na+)大小:①>②>③ |
B.往稀氨水中加水, 的值变小 的值变小 |
| C.pH=4的H2S溶液与pH=10的NaOH溶液等体积混合,存在下列等式:c(Na+)+c(H+) = C(OH—)+2c(S2—) |
| D.Ca(ClO) 2溶液中通入少量CO2,ClO—水解程度增大,溶液碱性增强 |
题号:3210688
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列图示与对应的叙述相符的是

| A.图甲表示催化剂能改变化学反应的焓变 |
| B.图乙表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH—)大小:a<b |
C.由图丙可知反应2A(g)+B(g)  C(g)的△H >O,且 a=2 C(g)的△H >O,且 a=2 |
| D.图丁表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况 |
题号:3210689
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是

| A.电池工作时,电子由a流向b |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H+ +2e— ===Mn2+ +2 H2O |
题号:3210690
题型:选择题
难易度:较易
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列相关工业制法的描述不正确的是
| A.电解熔融氯化钠制取金属钠 |
| B.电解熔融的Al(OH) 3制取金属铝 |
| C.用石英、纯碱、石灰石为原料制玻璃 |
| D.用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
题号:3210691
题型:选择题
难易度:较易
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】利用下列图示进行相应实验,能达到目的的是

| A.用图1可萃取碘水中的碘 |
| B.用图2可除去NO2中的NO |
| C.用图3制取并收集干燥纯净的NH3 |
| D.用图4配制100mL一定物质的量浓度的稀硫酸 |
题号:3210692
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列物质间的转化在给定条件下能实现的是

题号:3210693
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】常温下,下列各组离子能常量共存的是 、
| A.Mg2+、K+、SO42—、NO3— | B.Fe2+、H+、Cl—、NO3— |
| C.Cu2+、Na+、OH—、Cl— | D.K+、HCO3—、Ca2+、OH— |
题号:3210694
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】ClO
2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:
2KClO
3+H
2C
2O
4+H
2SO
4
2ClO
2↑+K
2SO
4+2CO
2↑+2H
2O
据此,下列说法不正确的是
| A.KClO3发生还原反应 |
| B.H2C2O4在反应中被氧化 |
| C.H2C2O4的氧化性强于ClO2的氧化性 |
| D.每1 mol ClO2生成,该反应转移的电子数约为6.02×1023 |
题号:3210695
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将甲针筒内的物质压到乙针筒内,进行实验,对乙针筒里的现象所作的判断不正确的是

实验序号
| 甲针筒内物质
| 乙针筒内物质
| 乙针筒里的现象
|
A
| HCl
| AgNO3溶液
| 产生白色沉淀
|
B
| NH3
| FeCl3溶液
| 出现红褐色沉淀
|
C
| CO2
| BaCl2
| 产生白色沉淀
|
D
| Cl2
| 紫色石蕊溶液
| 先变红后褪色
|
题号:3210696
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列化学反应对应的离子方程式书写正确的是
| A.醋酸溶液与Mg(OH) 2反应:Mg(OH) 2 +2H+ ===Mg2+ +2H2O |
B.碳酸钠溶液呈碱性:CO32— +2H2O  H2CO3 +2OH— H2CO3 +2OH— |
| C.NH4HC03溶液与过量NaOH溶液反应:NH4+ +OH— ===NH3·H2O |
D.用惰性电极电解饱和食盐溶液:2Cl—+2H2O  2OH— +Cl2↑+H2↑ 2OH— +Cl2↑+H2↑ |
题号:3210697
题型:选择题
难易度:较易
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列关于有机物的表述正确的是
| A.油脂可水解生成丙三醇 |
| B.乙醇经还原可生成乙醛 |
| C.乙烯与苯均可使酸性高锰酸钾溶液褪色 |
| D.淀粉、蛋白质完全水解的产物互为同分异构体 |
题号:3210698
题型:选择题
难易度:一般
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】设N
A为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,8 g甲烷中含C-H键的数目为4NA |
| B.25℃时,1 L pH=13的Ba(OH) 2溶液中含有的OH—数为0.2NA |
| C.1 mol冰醋酸和1 mol乙醇经催化加热反应生成H2O分子数为NA |
| D.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
题号:3210699
题型:选择题
难易度:较易
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】下列对化学知识的认识正确的是
| A.H2与T2互为同位素 | B.氯化铵、氯化银都属于强电解质 |
| C.离子化合物中一定不含共价键 | D.SO2、CO均属于酸性氧化物 |
题号:3210700
题型:选择题
难易度:较易
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是
| A.稀的食盐水能杀死H7N9禽流感病毒 |
| B.煤经过分馏和干馏两个物理变化,可变为清洁能源 |
| C.电镀厂的废水直接用来灌溉农田,可提高水的利用率 |
| D.用CO2合成聚碳酸酯可降解塑料,有利于减少白色污染 |
题号:3210683
题型:实验题
难易度:困难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(14分)海波(Na
2S
2O
3·5H
2O)常用手纺织和造纸工业,海波是无色透明的晶体,易溶于水,遇酸立即分解:S
2O
32— + 2H
+ ="==" S↓+ SO
2↑+ H
2O。
硫化碱法是工业上制备海波的方法之一,反应原理为:2Na
2S+Na
2CO
3+4SO
2 ="==" 3Na
2S
2O
3+CO
2某研究小组在实验室用硫化碱法制备Na
2S
2O
3·5H
2O,实验装置如下图所示:

(1)装置A中滴加浓硫酸的仪器名称是
,发生反应的化学方程式是
,实验室还可以用A装置制取的气体单质有
(填化学式)。
(2)装置C中连接多孔球泡可以提高S O
2的吸收效率,其依据的原理是
。
(3)装置D的作用是检验装置C中SO
2的吸收效率,D中的试剂可以是
。
a.品红溶液 b.氢氧化钠溶液
c.酚酞溶液 d.酸性高锰酸钾溶液
(4)装置E的作用是
。
(5)实验制得的Na
2S
2O
3·5H
2O产品中可能含有Na
2SO
3、Na
2SO
4等杂质。请设计实验,检测Na
2S
2O
3·5H
2O产品中是否存在Na
2SO
4杂质,简要说明实验操作、现象和结论:
。
(6)Na
2S
2O
3溶液是定量实验中的常用试剂,为了测定某K
2Cr
2O
7溶液的浓度,研究小组的同学准确量取10.00mL K
2Cr
2O
7溶液于锥形瓶中,加入过量KI固体和适量的稀H
2SO
4,滴加指示剂,用0.1000 mol·L
-1 Na
2S
2O
3标准溶液滴定至终点,3次平行实验测得平均消耗Na
2S
2O
3溶液的体积为30.00 mL,则c(K
2Cr
2O
7) =
mol·L
-1。(已知:Cr
2O
72— +6I
— +14H
+ ="==" 2Cr
3+ +3I
2 +7H
2O,2S
2O
32— + I
2===S
4O
62—+2 I
—)
题号:3210682
题型:填空题
难易度:困难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(A)【化学—物质结构与性质】(13分)
物质中铁含量的测定方法是多种多样的。
I.土壤中铁含量的测定是先将Fe
3+还原为Fe
2+,然后使Fe
3+与邻啡罗啉

结合显橙红色,再用比色法测定。其中涉及反应:4FeCl
3 + 2NH
2OH·HCl ="==" 4FeCl
2 + N
2O↑+ 6HCI + H
2O
(1)基态Fe
2+的核外电子排布式为
。
(2)羟胺(NH
2OH)中采用sp3杂化的原子是
;
羟胺极易溶于水,主要原因是
。
(3)羟胺的组成各元素中,元素的第一电离能(I
1)由大到小的顺序为
(用元素符号表示)。
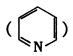
(4)吡啶和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为
mol。
Ⅱ.奶粉中铁含量的测定是在酸性介质中使Fe
3+与K
4Fe(CN)
6生成普鲁士蓝(Ⅱ)(化学式为Fe
4[Fe(CN)
6]
3),再用光度法测定铁的含量。反应原理:3K
4Fe(CN)
6+4FeCl
3 ="==" Fe
4[Fe(CN)
6]
3↓+12KCl
(5)Fe
4[Fe(CN)
6]
3是一种配合物,其中含有的化学键有
;
a.共价键
b.氢键
c.配位键
d.金属键
e.离子键
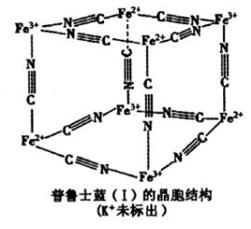
(6)若K
4 Fe(CN)
6和FeCl
3的物质的量按某种比例发生反应,可生成普鲁士蓝(I),其晶胞结构如下图所示:据此判断普鲁士蓝(I)中n(K
+):n(Fe
3+):n (Fe
2+):n (CN
—)=
。
题号:3210684
题型:填空题
难易度:较难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(14分)目前机动车使用的电池品种不少,其中铅蓄电池的使用量最大。

I.铅蓄电池的电极材料分别是Pb和PbO
2,电解质溶液为稀硫酸。铅蓄电池充放电的总反应方程式为:
PbO
2+Pb+2H
2SO
4
2PbSO
4+2H
2O,
请根据上述情况判断:
(1)电池的负极材料是
。
(2)充电时,铅蓄电池阳极的电极反应式为
。
Ⅱ.铅蓄电池使用量的急速增加引起铅污染日益严重,工业上从废铅蓄电池的铅膏回收铅的一种工艺流程如下:
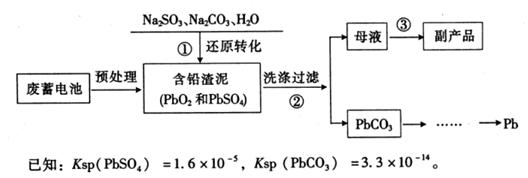
请回答下列问题:
(3)为提高步骤①的化学反应速率,你认为可采取的措施是
(写一条即可)。
(4)写出步骤①中PbSO
4转化为PbCO
3反应的平衡常数表达式:K =
。
(5)步骤①中发生氧化还原反应的化学方程式为
。
(6)步骤③从母液可获得的副产品为
(写化学式)。
(7)已知:PbCO
3在一定条件下可制得PbO,PbO通过进一步反应可制得Pb,写出一个由PbO生成Pb的化学方程式:
。
题号:3210685
题型:填空题
难易度:较难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(7分)环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH
4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH
4 (g)+ 4NO
2 (g)="==" 4NO(g)+ CO
2 (g)+ 2H
2O(1) △H
1 = -662kJ·mol
-1②CH
4 (g)+ 4NO(g) ="==" 2N
2 (g)+ CO
2 (g)+ 2H
2O(1) △H
2 =" -1251" kJ·mol
-1据此,写出CH
4将NO
2还原为N
2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g)

N
2 (g)+CO
2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加人0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T
1℃)条件下发生反应,经10min反应达到平衡,测得N
2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为
。
②下列各项能判断该反应达到平衡状态的是
。
| A.容器内压强保持不变 |
| B.速率关系:2v(NO)(正) =" v" (N2)(逆) |
| C.容器内CO2的体积分数不变 |
| D.混合气体的密度保持不变 |
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率
(填“增大”、“不变”或“减小”)。
题号:3210686
题型:填空题
难易度:较难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(10分)短周期元素W、X、Y、Z在元素周期表中的位置如图所示。

其中Z的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。
(1)W在元素周期表中的位置是
。
(2)Z的原子结构示意图为
。
(3)下列选项中,能证明元素非金属性X强于W的是
。
A.原子序数:X>W
|
B.最低化合价:X>W
|
C.最简单氢化物的稳定性:X>W
|
D.最高价氧化物的水化物酸性:X>W
|
(4)元素周期表中与Z同周期的某金属元素形成的单质A,可发生如下图所示的转化:

其中化合物D是一种白色沉淀,则B中溶质的化学式为
;
C转化生成D的离子方程式为
。
(5)表中Y的最高价氧化物对应水化物的化学式为Y(OH)
n ,在T℃时,其饱和溶液能使酚酞试液变红,原因是其溶液中的c(OH
—) =
mol·L
—1 (填计算数值,已知:T℃,Ksp[Y(OH)
n]=4.0×l0
-12)。
题号:3210681
题型:推断题
难易度:较难
日期:2015-04-03
来源:2015届福建省漳州市高三3月质量检查化学试卷(带解析)
【题文】(B)【化学—有机化学基础】(13分)

请根据上述合成路线,回答下列问题:
(1)氢化阿托醛所含官能团的名称为
;一定条件下,1 mol氢化阿托醛最多可跟
mol氢气加成。
(2)②的反应类型是
。
(3)写出反应③的化学方程式:
。
(4)④中所用试剂X为
。
(5)C与羧酸M在一定条件下可生成一种相对分子质量为178的酯类物质,则M的结构简式为
。
(6)氢化阿托醛具有多种同分异构体,写出符合下列特征的同分异构体的结构简式:
(写出一种即可)。
①苯环上有两个取代基
②苯环上的一溴代物只有两种
③其水溶液遇FeCl
3溶液呈特征颜色
④能发生加聚反应
 的值变小
的值变小
 C(g)的△H >O,且 a=2
C(g)的△H >O,且 a=2


 2ClO2↑+K2SO4+2CO2↑+2H2O
2ClO2↑+K2SO4+2CO2↑+2H2O
 H2CO3 +2OH—
H2CO3 +2OH— 2OH— +Cl2↑+H2↑
2OH— +Cl2↑+H2↑
 结合显橙红色,再用比色法测定。其中涉及反应:4FeCl3 + 2NH2OH·HCl ="==" 4FeCl2 + N2O↑+ 6HCI + H2O
结合显橙红色,再用比色法测定。其中涉及反应:4FeCl3 + 2NH2OH·HCl ="==" 4FeCl2 + N2O↑+ 6HCI + H2O


 2PbSO4+2H2O,
2PbSO4+2H2O,
 N2 (g)+CO2 (g)
N2 (g)+CO2 (g)

