适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2014年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2014年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2014年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2014年')}}上传日期:2014-06-30题数:22
提示:单击题文可显示答案与解析。
题号:1265720
题型:选择题
难易度:一般
日期:2016-11-09
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】能用离子方程式H
++OH
—=H
2O表示的是
| A.Ba(OH)2溶液和H2SO4溶液混合 | B.NaOH溶液和盐酸混合 |
| C.Cu(OH)2和稀H2SO4反应 | D.CO2通入NaOH溶液中 |
题号:3241762
题型:选择题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】如下图所示利用海洋资源可提取很多重要的化合原料。

下列有关说法正确的是
| A.第①步中除去粗盐中的SO42—、Ca2+、Mg2+、Fe3+等杂质加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.第②步中工业上可采用石墨为阴极、铁为阳极,采用阳离子交换膜的电解装置 |
| C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| D.第④步中溴元素被氧化,第④⑤步的目的是富集溴元素 |
题号:3241763
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】有NaCl和MgCl
2组成的混合物153.5g,溶于水配成1L溶液,此溶液中Cl
—的物质的量浓度为3mol/L,则原混合物中的MgCl
2的质量为
| A.95g | B.47.5g | C.58.5g | D.117g |
题号:3241764
题型:选择题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】海带中含碘元素,有人设计如下步骤来提取碘:①通足量氯气②将海带烧成灰,向灰中加水搅抖③加入CCl
4振荡④过滤⑤用分液漏斗分液。合理的操作顺序
| A.②—④—①—③—⑤ | B.②—①—③—④—⑤ |
| C.①—③—⑤—②—④ | D.③—①—②—⑤—④ |
题号:3241765
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】从海水中提取金属镁,没有涉及到的化学反应是
| A.Mg(OH)2+2HCl=MgCl2+2H2O |
| B.Mg2++2OH-=Mg(OH)2↓ |
| C.Mg(OH)2△MgO+H2O |
| D.MgCl2电解Mg+Cl2↑ |
题号:3241766
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】向NaOH溶液中通入一定量CO
2,结晶后得到白色固体,该白色固体配成溶液逐渐加入盐酸溶液(如图),则原白色固体的成分是
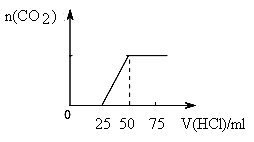
A.NaOH和Na
2CO
3 B
.Na
2CO
3 C
.Na
2CO
3和NaHCO
3 D.NaHCO
3
题号:3241767
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】NaCl是一种化工原料,可以制备一系列物质(如图)。下列说法正确的是

| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.图4所示转化反应都是氧化还原反应 |
题号:3241768
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】下列说法正确的是
| A.1mol Cl2与足量NaOH溶液反应转移电子的物质的量为2mol |
| B.用含有0.2mol HCl的浓盐酸与足量MnO2加热后,可制得1.12L Cl2(标况) |
| C.向新制氯水中通入SO2,氯水的漂白能力将增强 |
| D.向新制氯水中加入CaCO3,溶液中有气泡放出 |
题号:3241769
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】下列实验设计及其对应的离子方程式均正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
题号:3241771
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】在过量的稀硫酸溶液中加入5.6g Fe粉,待反应完全后,再加入50mL 0.5mol·L
-1KNO
3溶液,恰好反应完全。该反应的方程式为:
___FeSO
4+____KNO
3+____H
2SO
4═___K
2SO
4+___Fe
2(SO
4)
3+___N
xO
y+__H
2O,则对该反应的下列说法正确的是
| A.反应中还原产物是NO |
| B.氧化产物和还原产物的物质的量之比为1:4 |
| C.反应过程中转移的电子数为8e— |
| D.化学方程式中按物质顺序的化学计量数是8、2、5、1、4、1、5 |
题号:3241772
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】有3份等质量的小苏打,第1份直接与过量过酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应。假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是
A.V2>V3>V1 B.V1>V3>V2 C.V1=V2=V3 D.V1>V2>V3
题号:3241773
题型:选择题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】某溶液中含有下列六种离子:①HCO
3—②SO
32—③Na
+④CO
32-⑤NH
+4⑥NO
3—⑦SO
42—向其中加入一定量Na
2O
2后,溶液中离子浓度基本保持不变的是
题号:3241774
题型:选择题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】
| A.用量筒取5.00mL 1.00mol/L盐酸于50mL容量瓶中,加水稀释至刻度,可配制0.100mol/L盐酸 |
| B.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 |
| C.用10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
| D.质量分数为10%的氨水与质量分数为20%的氨水等体积混合,所得氨水的质量分数小于15% |
题号:3241775
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】能在水溶液中大量共存的一组离子是
| A.H+、I—、NO3—、SiO32— | B.Ag+、Fe3+、Cl—、SO42— |
| C.K+、SO42—、Cu2+、NO3— | D.NH+4、OH—、Cl—、HCO3— |
题号:3241776
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】设N
A为阿伏加德罗常数的值,下列有关叙述正确的是
| A.11.2L O3气体中含有的氧原子数是1.5NA |
| B.含12.0 gNaHSO4的水溶液中钠离子数为0.1NA |
| C.1mol—OH中电子数为10NA |
| D.每有1mol Cl2反应转移的电子数一定为2NA |
题号:3241777
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】分类是学习化学的重要方法,下列归纳正确的是
| A.纯碱、烧碱都属于碱类 | B.冰和干冰既是纯净物又是化合物 |
| C.铅笔芯、铅球主要成分都是铅 | D.液氯和氯水是同一种物质 |
题号:3241778
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】“化学是人类进步的关键”。下列有关说法能反映正确化学观点的是
| A.改变物质的性质不一定要通过化学变化 |
| B.天然物质都比人造物质好 |
| C.一种元素可有多种离子,但只有一种原子 |
| D.根据分散系是否具有丁达尔效应,分散系分为溶液、胶体和浊液 |
题号:4312973
题型:选择题
难易度:一般
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】若(NH
4)
2SO
4在强热时分解的产物是SO
2、N
2、NH
3和H
2O,则该反应中化合价发生变化和未发生变化的N原子数之比为
题号:3241759
题型:实验题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】高铁酸钾(K
2FeO
4)是一种集氧化、吸附、始凝于一体的新型多功能水处理剂。其生产工艺如下:
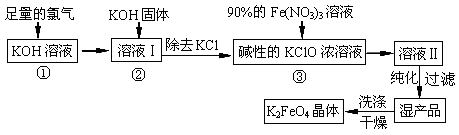
已知:
①2KOH+C1
2=KCl+KClO+H
2O(条件:温度较低)
②6KOH+3C1
2=5KCl+KClO
3+3H
2O(条件:温度较高)
③2Fe(NO
3)
3+2KClO+10KOH=2K
2FeO
4+6KNO
3+2KCl+5H
2O
回答下列问题:
(1)该生产工艺应在
(填“温度较高”或“温度较低”)的情况下进行;写出工业上制取Cl
2的化学方程式
;
(2)K
2FeO
4可作为新型多功能水处理剂的原因
;
(3)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
;
(4)在“反应液I”中加KOH固体的目的是①
②
;
(5)从“反应液II”中分离出K
2FeO
4后,副产品是
(写化学式)。
题号:3241761
题型:实验题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】实验室欲用胆矾(CuSO
4·5H
2O)固体配制480mL 0.5mol·L
-1 CuSO
4溶液:
(1)本实验需称取
g胆矾,必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管,还有
。
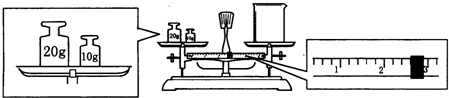
(2)某同学欲称量一定量的胆矾固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如下图,烧杯的实际质量为
g,配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④定容⑤转移,其正确的操作顺序为
。
(3)在配制过程中,其他操作都是正确的,下列操作会引起 浓度偏高的是
。
①没有洗涤烧烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
题号:4312974
题型:实验题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)
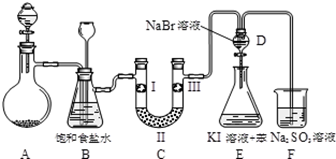
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为
。装置B中饱和食盐水的作用是
;同时装置B亦是安全瓶,滥测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:
。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入如下物质:
选项
| a
| b
| c
| d
|
I
| 干燥的有色布条
| 干燥的有色布条
| 湿润的有色布条
| 湿润的有色布条
|
II
| 碱石灰
| 硅胶
| 浓硫酸
| 无水氯化钙
|
III
| 湿润的有色布条
| 湿润的有色布条
| 干燥的有色布条
| 干燥的有色布条
|
其中,能证明氯气有漂白性的是
(填字母)。
(3)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为
色,说明氯的非金属性大于溴。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是
。
(4)装置F中用足量的Na
2SO
3溶液吸收余氯,试写出相应的离子反应方程式:
题号:3241760
题型:填空题
难易度:较难
日期:2014-06-30
来源:【百强校】2013-2014福建省福州三中高三上学期第三次月考化学试卷(带解析)
【题文】ClO
2气体是一种常用的消毒剂,我国从2000年起已逐步用ClO
2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO
2还可将Fe
2+、Mn
2+转化成Fe(OH)
3、MnO
2难溶物除去,在这个过程中,Fe
2+、Mn
2+的化合价升高,说明ClO
2具有
性。
(2)工业上可以通过下列方法制取ClO
2,请完成该反应化学方程式:2KClO
3+SO
2=2ClO
2+___。
(3)自来水厂用ClO
2处理后的水中,要求ClO
2的浓度在0.1—0.8mg/L之间。碘量法可以检测水中ClO
2的浓度,步骤如下:
I.取一定体积的水样用氢氧化钠溶液调至中性,然后加入一定量的碘化钾,并加入淀粉溶液,溶液变蓝。
II.加入一定量的Na
2S
2O
3溶液。(已知:2S
2O
32-+I
2═S
4O
62-+2I
-)
III.加硫酸调节水样pH至1.3。操作时,不同pH环境中粒子种类如下图所示:

请回答:
①操作I中反应的离子方程式是
。
②确定操作II完全反应的现象是
。
③在操作III过程中,溶液又呈蓝色,反应的离子方程式是
。
④若水样的体积为1.0L,在操作II时消耗了1.0×10
-3mol/L的Na
2S
2O
3溶液10mL,则水样中ClO
2的浓度是
mg/L。






