适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2011年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2011年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2011年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2011年')}}上传日期:2011-05-09题数:30
提示:单击题文可显示答案与解析。
题号:4355897
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】中国已经成为全球最大轿车生产国,汽车尾气正成为城市的主要空气污染源。NO和CO都是汽车尾气中的有害物质,它们能缓慢反应生成N
2和CO
2,为控制汽车污染有人提出以下建议,你认为合理的是
| A.增大压强 | B.使用催化剂 |
| C.降低压强 | D.升高反应温度加快反应速率 |
题号:4355898
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列说法正确的是
| A.某一反应的活化分子百分数是个定值 |
| B.升高温度会加快化学反应速率,其原因是增加了活化分子百分数 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子百分数,从而使反应速率增大 |
题号:4355899
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列是一些同学学习“化学反应速率和化学平衡”专题后,联系工业生产实际所发表的观点,你认为不正确的是
| A.怎样在一定时间内快出产品是运用了化学反应速率理论 |
| B.怎样使用有限原料多出产品是运用了化学平衡理论 |
| C.怎样提高原料转化率是运用了化学反应速率理论 |
| D.怎样使原料尽可能多地转化为产品是运用了化学平衡理论 |
题号:4355900
题型:选择题
难易度:一般
日期:2012-08-03
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】在体积都为1 L,pH都等于2的盐酸和醋酸溶液中,各投入0.65 g锌粒,则下图所示比较符合客观事实的是

题号:4355901
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列叙述正确的是
| A.根据Ksp(PbI2)>Ksp(AgCl)可以得出PbI2在水中的溶解能力比AgCl大 |
| B.常温下,同浓度的Na2CO3与NaHCO3溶液相比,NaHCO3溶液的pH大 |
| C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大 |
| D.常温下pH=7的氨水与硫酸铵的混合液中c(NH4+)与c(SO42-)之比小于2 |
题号:4355902
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】向某密闭容器中充入1 mol CO和2 mol H
2O(g),发生反应:CO+H
2O(g)

CO
2+H
2,当反应达到平衡时,CO的体积分数为
x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于
x的是
| A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 |
| B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
| C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 |
| D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 |
题号:4355903
题型:选择题
难易度:一般
日期:2012-11-19
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】用物质的量均是0.1 mol的CH
3COOH和CH
3COONa配成1L混合溶液,已知其中
c(CH
3COO
-)大于
c(Na
+),对该混合溶液的下列判断正确的是
| A.c(CH3COOH)>c(CH3COO-) |
| B.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1 |
| C.c(H+)>c(OH-) |
| D.c(CH3COO-)+c(OH-)=0.1mol·L-1 |
题号:4355904
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】室温下,给定的四组溶液,各组离子一定能够大量共存的是
| A.使酚酞试液变红的溶液: Na+、Cl-、SO42-、Fe3+ |
| B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| C.c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br- |
| D.所含溶质为Na2SO4的溶液:K+ 、HCO3-、NO3-、Al3+ |
题号:4355905
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】在Na
2HPO
4溶液中,存在着下列平衡:HPO
42-
H
++ PO
43- ;HPO
42-+H
2O

H
2PO
4-+OH
-,已知该溶液呈碱性。欲使溶液中的HPO
42-、H
+、PO
43-浓度都减小,可采取的方法是
题号:4355906
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】在容积为2升的密闭容器中,有反应:mA(g)+nB(g)

pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L
-1,B的平均反应速度V
B=a/15mol·L
-1·min
-1,C增加了2a/3 mol·L
-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为
| A.3:1:2:2 | B.1:3:2:2 | C.3:1:2:1 | D.1:1:1:1 |
题号:4355911
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列溶液中加入少量NaOH固体导电能力变化不大的是
| A.盐酸 | B.CH3COOH | C.NH3·H2O | D.H2O |
题号:4355912
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】常温下,若使pH=3的盐酸与pH=9的Ba(OH)
2溶液混合使其成为pH=7的溶液,混合时两溶液的体积比为
| A.1∶60 | B.3∶1 | C.100∶1 | D.1∶100 |
题号:4355913
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列说法中正确的是
| A.NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
B.常温下,反应 为熵增反应,可以自发进行 为熵增反应,可以自发进行 |
C.熵增加且放热的反应一定是自发反 应 应 |
| D.非自发反应在任何条件下都不能实现 |
题号:4355914
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列离子方程式正确的是
A.NaHS溶于水:NaHS Na++HS- Na++HS- |
| B.Na2HPO4溶于水:Na2HPO4 = 2Na++H++PO43- |
| C.熔融的NaHSO4:NaHSO4 = Na++H++SO42- |
D.HCO3-+H2O  H3O++CO32- H3O++CO32- |
题号:4355915
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】如图表示反应2 SO
2(g)+ O
2(g)

2 SO
3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是

| A.t1时减小了SO2的浓度,增加了SO3的浓度,平衡向逆反应方向移动 |
B.t1时降低了温度,平衡向正 反应方向移动 反应方向移动 |
| C.t1时减小了压强,平衡向逆反应方向移动 |
| D.t1时增加了SO2和O2的浓度,平衡向正反应方向移动 |
题号:4355916
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】某学生用碱式滴定管量取0.1mol/L的NaOH溶液,开始时仰视液面,读数为11.00mL,取出部分溶液后,俯视液面,读数为19.00mL,实际取出液体的体积是
| A.大于8.00mL | B.小于8.00mL | C.等于8.00mL | D.无法确定 |
题号:4355917
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】向三份0.1 mol·L
-1Na
2CO
3溶液中分别加入少量NH
4N

O
3固体、NaHCO
3固体、HCl气体(忽略溶液体积变化),则CO
32-浓度的变化依次为
| A.减小、增大、减小 | B.增大、减小、减小 |
| C.减小、增大、增大 | D.增大、减小、增大 |
题号:4355918
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列事实不能用勒夏特列原理解释的是
| A.打开碳酸饮料会有大量气泡冒出 |
| B.用难溶FeS固体除去工业废水中的Pb2+ |
| C.温度控制在500℃有利于合成氨反应 |
| D.实验室用排饱和食盐水的方法收集氯气 |
题号:4355919
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】将
a g 含NaOH样品溶解在
b mL 0.l mol·L
-1的硫酸中,再加入
c mL 0.1 mol·L
-1 的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是
| A.[(b-c)/125a]×100% | B.[(b-2c)/125a]×100% |
| C.[(b-c)/250a]×100% | D.[(8b-8c)/a]×100% |
题号:4355920
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】已知一种
c(H
+)=1×10
-3 mol·L
-1的酸和一种
c(OH
-)=1×10
-3 mol·L
-1碱溶液,等体积混合后溶液呈酸性,其原因可能是
| A.浓的强酸和稀的强碱溶液反应 | B.浓的弱酸和稀的强碱溶液反应 |
| C.等浓度的弱碱和强酸溶液反应 | D.生成了一种强酸弱碱盐 |
题号:4355921
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】把Ca(OH)
2放入蒸馏水中,一段时间后达到平衡:Ca(OH)
2(s)

Ca
2++2OH
-下列说法正确的是
| A.恒温下向溶液中加CaO,溶液的pH升高 |
| B.给溶液加热,溶液的pH升高 |
| C.向溶液中加入Na2CO3溶液,其中固体质量增加 |
| D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
题号:4355922
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】25℃时,水的

电离达到平衡:H
2O

H
++OH
-;ΔH>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
题号:4355923
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
题号:4355924
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L
-1 NaHC
2O
4溶液中滴加0.01 mol·L
-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
| A.V(NaOH) = 0时,c(H+) = 1×10-2 mol·L-1 |
| B.V(NaOH)<10 mL时,不可能存在c(Na+) = 2c(C2O42-)+c(HC2O4- ) |
| C.V(NaOH) =" 10" mL时,c(H+) = 1×10-7 mol·L-1 |
| D.V(NaOH)>10 mL时,c(Na+)>c(C2O42-)>c(HC2O4- ) |
题号:4355925
题型:选择题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】下列物质的溶液加热蒸干、灼烧后,所得的固体成份不相同的是
| A.FeCl2、FeCl3 | B.NaHCO3、Na2CO3 |
| C.Al2(SO4)3、AlCl3 | D.Mg(HCO3)2、MgCl2 |
题号:4355910
题型:实验题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】
(1)该学生的操作是
(填“正确的”或“错误的”)。
(2)如不正确,是否一定有误差?答:
(填“是”或“否”)
(3)若按此法分别测定C(H
+)相等的盐酸和醋酸溶液的pH,误差较大的是
,原因是
。
Ⅱ、(10分)
(1)如图表示50mL滴定管中液面的位置,其读数是
mL

(2)乙二酸俗名草酸,某化学学习小组的同学欲探究测定
草酸晶体(H
2C
2O
4·
xH
2O)中
x值。通过查阅资料得,草酸易溶于水,水溶液可以用酸性KMnO
4溶液进行滴定:2MnO
4-+5H
2C
2O
4+6H
+2Mn
2++10CO
2↑+8H
2O该组同学设计了滴定的方法测定
x值。请回答:①、下列仪器在进行滴定时,绝不可以事先润洗的是
(填编号)。
甲.酸式滴定管 乙.碱式滴定管 丙.25 mL量筒丁.锥形瓶
②、滴定时,将KMnO
4标准液装在
滴定管中。
③、本实验滴定达到终点的标志可以是
。
④、若滴定终点时俯视滴定管刻度,则由此测得的
x值会
(填“偏大”、“偏小”或“不变”)。
题号:4355907
题型:填空题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】(9分)完成以下小题:
(1)已知NaHSO3溶液显酸性,则溶液中各离子浓度从大到小的顺序是 。
(2)25℃时,向pH=4的NaHSO4溶液中,逐滴加入pH=9的Ba(OH)2溶液至中性,则该过程的离子反应方程式 ;已知25℃时BaSO4的Ksp=1.0×10-10,则以上过程中 沉淀生成(填“有” 或“无”)。
(3)某温度下,0.1 mol·L-1Na2CO3溶液中c(Na+)∕c(CO32-)=20/9,其原因是 ;现往Na2CO3溶液中通入一定量的CO2后,c(Na+)∕c(CO32-)=5∕2,其原因是 。(用离子方程式和必要的文字说明)
题号:4355908
题型:填空题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】(1

0分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H
2O(g)

CO
2(g)+H
2(g) △
H<0 ;试回答下列问题:
(1)若起始时
c(CO)="2" mol·L
-1,
c(H
2O)="3" mol·L
 -1
-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数
K=
(2)在相同温度下,起始物质按下列四种配比充入该容器中,
c(H
2O)=2mol·L
-1,
c(CO)=
c(CO
2)="1" mol·L
-1,
c(H
2)="1.5" mol·L
-1,则此时该反应是否达到平衡状态
(填“是”与“否”),此时
v(正) v(逆)(填“

大于”、“小于”或“等于”)。
(3)若降低温度,该反应的
K值将
,该反应的化学反应速率将
(均填“增

大”“减小”或“不变”)。
题号:4355909
题型:填空题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】(6分)氢氧化铜悬浊液中存在如下平衡:
Cu(OH)
2(s)

Cu
2+(aq)+2OH
-(aq),常温下其K
sp=2×10
-20则:
(1)某硫酸铜溶液里c(Cu
2+)=0.02mol/L,如要生成Cu(OH)
2沉淀,应调整溶液pH大于
。
(2)除去CuCl
2溶液中少量的Fe
2+,可以按照下面的流程进行:

已知Fe
2+、Cu
2+、Fe
3+ 三种离子开始沉淀和完全沉淀时溶液pH值如下:
金属
离子
| pH
|
开始沉淀
| 完全沉淀
|
Fe2+
| 7.6
| 9.6
|
Cu2+
| 4.4
| 6.4
|
Fe3+
| 2.7
| 3.7
|
①下列物质中适合作为试剂X的是

A.H
2O
2 B.KMnO
4 C.HNO
3 D.Cl
2②加入的Y及调节的pH范围是
A.CuCO
3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH
3·H
2O 3.7~4.0
题号:4355926
题型:填空题
难易度:一般
日期:2011-05-09
来源:2010-2011学年福建省莆田一中高二下学期第一学段考试化学试卷
【题文】(7分)25时,如果取0.1 mol·L
-1HA溶液与0.1 mol·L
-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液中由水电离出的
c(H
+)__
___0.1 mol·L
-1 NaOH溶液中由水电离出的c(H
+)。(填“

>”、“<”、“=”)
(2)求出混合液中下列算式的精确计算结果(填具体数字):
c (Na
+)-
c (A
-)=
mol·L
-1(3)已知NH
4A溶液为中性,又知将HA溶液加到Na
2CO
3溶液中有气体放出,试推断NH
4HCO
3溶液的pH
7 (填“>”、“<”、“=”)
(4)将相同温度下相同浓度的四种盐溶液:
| A.NH4HCO3 | B.NH4A | C.(NH4)2SO4 | D.NH4Cl |
按pH由大到小的顺序排列
(填序号)

 CO2+H2,当反应达到平衡时,CO的体积分数为x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
CO2+H2,当反应达到平衡时,CO的体积分数为x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是 H++ PO43- ;HPO42-+H2O
H++ PO43- ;HPO42-+H2O H2PO4-+OH-,已知该溶液呈碱性。欲使溶液中的HPO42-、H+、PO43-浓度都减小,可采取的方法是
H2PO4-+OH-,已知该溶液呈碱性。欲使溶液中的HPO42-、H+、PO43-浓度都减小,可采取的方法是 pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为 为熵增反应,可以自发进行
为熵增反应,可以自发进行 应
应 Na++HS-
Na++HS- H3O++CO32-
H3O++CO32- 2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
 反应方向移动
反应方向移动 O3固体、NaHCO3固体、HCl气体(忽略溶液体积变化),则CO32-浓度的变化依次为
O3固体、NaHCO3固体、HCl气体(忽略溶液体积变化),则CO32-浓度的变化依次为 Ca2++2OH-下列说法正确的是
Ca2++2OH-下列说法正确的是 电离达到平衡:H2O
电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
 mol·L-1·min-1和
mol·L-1·min-1和 mol·L-1
mol·L-1 mol·L-1·min-1和
mol·L-1·min-1和 mol·L-1
mol·L-1 mol·L-1·min-1和
mol·L-1·min-1和 mol·L-1
mol·L-1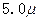 mol·L-1·min-1和
mol·L-1·min-1和 mol·L-1
mol·L-1
 0分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)
0分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0 ;试回答下列问题:
CO2(g)+H2(g) △H<0 ;试回答下列问题: -1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=  大于”、“小于”或“等于”)。
大于”、“小于”或“等于”)。 大”“减小”或“不变”)。
大”“减小”或“不变”)。 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
 A.H2O2 B.KMnO4 C.HNO3 D.Cl2
A.H2O2 B.KMnO4 C.HNO3 D.Cl2 >”、“<”、“=”)
>”、“<”、“=”)