适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2015年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2015年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2015年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2015年')}}上传日期:2016-01-21题数:20
提示:单击题文可显示答案与解析。
题号:3174011
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】已知下表数据:
物质
| Fe(OH)2
| Cu(OH)2
| Fe(OH)3
|
完全沉淀时的pH范围
| ≥9.6
| ≥6.4
| ≥3
|
对于含等物质的量的CuSO
4、FeSO
4、Fe
2(SO
4)
3的混合溶液,下列说法正确的是
A.向该混合溶液中逐滴加入NaOH溶液,最先看到的是红褐色沉淀
B.该溶液中c(SO
42﹣):[c(Cu
2+)+c(Fe
2+)+c(Fe
3+)]==5:4
C.向该溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO
4溶液
D.向该溶液中加入适量氨水,调节pH到9.6后过滤,将所得沉淀灼烧,可得等物质的量的CuO、FeO、Fe
2O
3三种固体的混合物
题号:3174012
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是
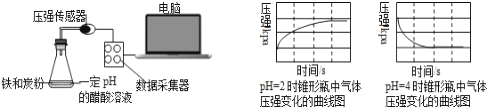
| A.溶液pH≤2时,生铁发生析氢腐蚀 |
| B.在酸性溶液中生铁可能发生吸氧腐蚀 |
| C.析氢腐蚀和吸氧腐蚀的速率一样快 |
| D.两溶液中负极反应均为:Fe﹣2e﹣=Fe2+ |
题号:3174013
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】某溶液仅含Fe
2+、Na
+、Al
3+、Ba
2+、SO
42﹣、NO
3﹣、Cl
﹣中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是
| A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.该溶液中所含的离子是:Fe2+、Na+、SO42﹣、NO3﹣ |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
题号:3174014
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】一定条件下,通过下列反应可实现燃煤烟气中硫的回收,其中Y是单质。 SO
2(g) + 2CO(g)

2X(g)+Y(l),为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO
2和CO浓度如下表:
时间/s
| 0
| 1
| 2
| 3
| 4
|
c(SO2)/mol·L-1
| 1.00
| 0.50
| 0.23
| 3.00×10-37
| 3.00×10-37
|
c(CO)/mol·L-1
| 4.00
| 3.00
| 2.46
| 2.00
| 2.00
|
下列说法不正确的是
A.X的化学式为CO
2B.前1s内v(X)=" 1.00" mol·L
-1·s
-1C.该回收原理运用了SO
2的还原性
D.该温度下,此反应的平衡常数的数值是3.33×10
36
题号:3174015
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】某ⅡA族元素是该族元素中在自然界最广泛存在的元素,常以化合物F的形式存在,其单质A可发生一系列如图所示的化学反应。下列说法正确的是
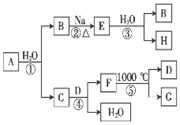
| A.D与H溶液反应后所得溶液的溶质成分有三种可能 |
| B.电解F与盐酸反应后的溶液以制取单质A |
| C.反应①、③中消耗相同H2O时反应转移电子数相同 |
| D.工业上常用F的悬浊液与Cl2反应制取漂白粉 |
题号:3174016
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】某硫酸厂废气中SO
2的回收利用方案如图所示.下列说法错误的是
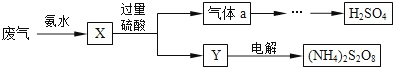
| A.X可能含有2种盐 |
| B.Y可能含有NH4HSO4 |
| C.a是SO3 |
| D.(NH4)2 S2O8中S的化合价不可能为+7 |
题号:3174017
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】科技工作者提出用铝粉处理含亚硝酸盐废水的思路:调节亚硝酸盐废水酸碱性,使其pH>12,然后加入适量的铝粉、搅拌,生成可进入大气循环的气体,从而实现预期目的。下列判断错误的是
| A.处理过程中,pH减小 |
| B.废水处理中,亚硝酸盐被还原 |
| C.废水处理时铝单质转化为AlO2- |
| D.铝粉颗粒大小影响废水处理的速率 |
题号:3174018
题型:选择题
难易度:一般
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】短周期元素X、Y、Z、W的原子序数依次增大,X和Z同主族,Y和W同主族,原子半径X小于Y,四种元素原子最外层电子数之和为14。下列叙述正确的是
| A.同周期元素中W的最高价氧化物对应水化物的酸性最强 |
| B.氢化物的热稳定性:HnY>HnW |
| C.Y和X、Z和X组成的常见化合物中化学键的类型相同 |
| D.原子半径的大小顺序: rW>rZ>rY>rX |
题号:3174019
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】固体X中可能含有MgCl
2、Na
2CO
3、K
2SO
3、KAlO
2中的一种或几种。为确定该固体粉末的成分,现取X进行下列实验,实验过程及现象如下:
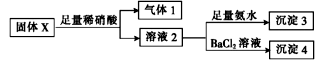
根据上述实验,下列说法正确的是
| A.气体1可能为SO2和CO2的混合物 |
| B.沉淀3可能为Mg(OH)2和Al(OH)3的混合物 |
| C.沉淀4可能为BaCO3、BaSO3或二者混合物 |
| D.固体粉末X中一定有Na2CO3,可能有KAlO2 |
题号:3174020
题型:选择题
难易度:一般
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】下图装置用于气体的干燥、收集和尾气吸收,其中X、Y、Z对应都正确的是
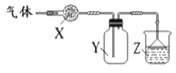
| X
| Y
| Z
|
A
| 无水硫酸铜
| 氯气
| 饱和食盐水
|
B
| 碱石灰
| 氨气
| 水
|
C
| 氯化钙
| 二氧化硫
| 氢氧化钠
|
D
| 氯化钙
| 一氧化氮
| 氢氧化钠
|
题号:3174021
题型:选择题
难易度:一般
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去).则W、X不可能是
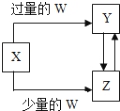
选项
| W
| X
|
A
| 盐酸
| Na2CO3溶液
|
B
| Cl2
| Fe
|
C
| CO2
| Ca(OH)2溶液
|
D
| NaOH溶液
| AlCl3溶液
|
题号:3174022
题型:选择题
难易度:一般
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】下列叙述正确的是
①向久置于空气中的NaOH溶液中加盐酸时有气体产生 ②浓硫酸可用于干燥H
2、NO
2等气体,但不能干燥NH
3、SO
2等气体 ③CO
2和Na
2O
2反应生成Na
2CO
3和O
2,SO
2和Na
2O
2反应生成Na
2SO
3和O
2④足量硫单质与64 g铜反应,有2 mol电子发生转移 ⑤蔗糖炭化的演示实验中,浓硫酸既体现了强氧化性又体现了脱水性⑥氢氧化铁胶体与氯化铁溶液分别蒸干灼烧得相同的物质
题号:3174023
题型:选择题
难易度:较易
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】下列工业生产的主要反应中,涉及置换反应的是(
题号:3174024
题型:选择题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】用N
A表示阿伏加德罗常数的值,下列叙述中正确的是
| A.标准状况下,22.4 L SO3中含有O数目为3.0NA |
| B.常温常压下,12.2 gNaHSO4中含有离子总数为0.3NA |
| C.在1 L 0.1 mol·L-1碳酸钠溶液中,阴离子总数大于0.1NA |
| D.某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
题号:3174025
题型:选择题
难易度:一般
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】依据下列说法来判断相应元素的金属性、非金属性强弱,不合理的是
| A.卤素单质Cl2、Br2、I2的氧化性强弱 |
| B.气态氢化物NH3、H2O、HF的稳定性 |
| C.碱金属单质Li、Na、K与水反应的剧烈程度 |
| D.1mol Na、Mg、Al分别与足量盐酸反应时失电子数的多少 |
题号:3174026
题型:选择题
难易度:容易
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】化学与生产、生活、社会密切相关,下列有关说法不正确的是
| A.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印机属于“低碳生活”方式 |
| B.我国神七宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
C.日本福岛核电站爆炸时释放的2种放射性核素 的中子数不等 的中子数不等 |
| D.食品保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |
题号:3174007
题型:实验题
难易度:困难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
【探究一】
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe
3+外还可能含有Fe
2+。若要确认其中的Fe
2+应选用______(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.KMnO
4酸性溶液
②乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:[SO
2+Br
2+2H
2O=2HBr+H
2SO
4然后加入足量BaCl
2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO
2的体积分数为
。
【探究二】
分析上述实验中SO
2体积分数的结果,丙同学认为气体Y中还可能含有H
2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
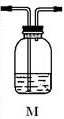
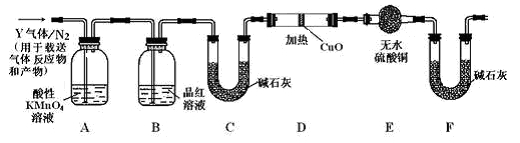
(3)装置B中试剂的作用是
(4)认为气体Y中还含有Q的理由是
(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于____________(选填序号)。
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H
2,预计实验现象应是__________________
(7)若要测定336mL气体中H
2的含量(标准状况下约有28 mL H
2),可否用托盘天平称量D或E反应前后的质量差的方法做出判断?并说明理由
题号:3174008
题型:填空题
难易度:困难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】CoCl
2·6H
2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co
2O
3、Co(OH)
3,还含少量Fe
2O
3、Al
2O
3、MnO等)制取CoCl
2·6H
2O的工艺流程如下:
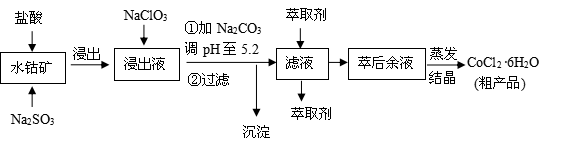
已知:①浸出液含有的阳离子主要有H+、Co
2+、Fe
2+、Mn
2+、Al
3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物
| Fe(OH)3
| Fe(OH)2
| Co(OH)2
| Al(OH)3
| Mn(OH)2
|
开始沉淀
| 2.7
| 7.6
| 7.6
| 4.0
| 7.7
|
完全沉淀
| 3.7
| 9.6
| 9.2
| 5.2
| 9.8
|
③CoCl
2·6H
2O熔点为86℃,加热至110~120℃时,失去结晶生成无水氯化钴。
(1)写出浸出过程中Co
2O
3发生反应的离子方程式
。
(2)写出NaClO
3发生反应的主要离子方程式
;若不慎向“浸出液”中加过量NaClO
3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式
(3)“加Na
2CO
3调pH至5.2”,过滤所得到的沉淀成分为
,加入萃取剂的目的是
。
(4)制得的CoCl
2·6H
2O在烘干时需减压烘干的原因是
。
(5)为测定粗产品中CoCl
2·6H
2O含量,称取一定质量的粗产品溶于水,加入足量HNO
3酸化的AgNO
3 溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl
2·6H
2O的质量分数大于100%,其原因可能是
。(答一条即可)
题号:3174010
题型:填空题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】氯元素是生产生活中常见的非金属元素
(1)将Cl
2通入NaOH溶液中得到以NaClO为有效成分的漂白液,写出该反应的离子方程式:
。
(2)使用Cl
2为自来水消毒时,会与水中的有机物生成对人体有害的有机氯化物。下列物质中可以替代Cl
2为自来水杀菌消毒的是
(填字母序号)。
a. 臭氧 b.NH
3 c. 明矾 d.ClO
2(3)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl
2等物质,对金属炉壁造成腐蚀。
① NaCl和Cl
2中化学键的类型分别是
和
。
② 燃煤过程中生成的SO
2会与NaCl等物质发生反应,生成硫酸盐和Cl
2。若生成Cl
2 22.4 L(标况)时转移电子数为4×6.02×10
23,该反应的化学方程式是
。
③ 已知:2H
2O
2(l) ="==" 2H
2O(l)+O
2(g) ΔH
1=-196.46 kJ·mol
-1H
2(g)+1/2O
2(g) ="==" H
2O(l) ΔH
2=-285.84 kJ·mol
-1Cl
2(g)+H
2(g) ="==" 2HCl(g) ΔH
3=-184.60 kJ·mol
-1在催化剂作用下,用H
2O
2(l)可除去上述燃烧过程中产生的Cl
2。依据上述已知反应,写出该反应的热化学方程式:
。
(4)工业上通过如下转化可制得KClO
3晶体:
NaCl溶液
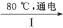
NaClO
3溶液

KClO
3晶体
完成Ⅰ中电解过程中阳极的反应式:
。
题号:3174009
题型:推断题
难易度:较难
日期:2016-01-21
来源:2016届福建省漳州八校高三上学期12月联考化学试卷(带解析)
【题文】下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
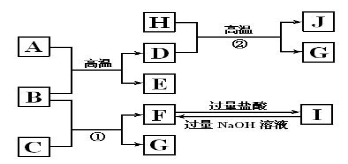
根据图示回答问题:
(1)按要求写出下列化学用语:若B原子中子数比质子数多1,则B的原子符号为
;C的电子式为
,若D最外层只有两个电子,则D的原子结构示意图
;
(2)写出反应①的化学方程式是
;写出反应②的化学方程式并标出电子转移的方向和数目__________________
(3)J与稀硝酸反应的离子方程式是
;用排水法收集满该反应的还原产物后,将试管倒扣在水槽中并通入O
2使试管刚好全部充满水,假设液体不外溢,则所得溶液的物质的量浓度为
。

 2X(g)+Y(l),为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
2X(g)+Y(l),为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:




 的中子数不等
的中子数不等


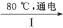 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体