适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2014年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2014年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2014年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2014年')}}上传日期:2014-06-03题数:12
提示:单击题文可显示答案与解析。
题号:4313625
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
题号:4313626
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】在25℃、1×10
5Pa时,等质量的H
2、Cl
2、CO
2、C
2H
2四种气体中( )
| A.H2分子数最大 | B.C2H2原子数最大 |
| C.CO2密度最大 | D.Cl2分子间平均距离最大 |
题号:4313627
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】基于实验现象的推论,你认为合理的是( )
选项
| 实验现象
| 推论
|
A
| 乙烯气体可以使溴水褪色
| 乙烯发生取代反应
|
B
| 浓硫酸电导率比较低
| 硫酸浓度大时是弱电解质
|
C
| 氨气用于喷泉实验
| 氨气极易溶于水
|
D
| 硝酸溶液使pH试纸先变红后变白
| 硝酸酸性太强不能用pH试纸检测
|
题号:4313628
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】对于相应化学用语的推论合理的是( )
选项
| 化学用语
| 推论
|
A
|  U3+ U3+
| 该铀离子核外有89个电子
|
B
| 2H2(g)+O2(g)=" " 2H2O(g);△H=-483.6kJ•mol
| 1mol氢气完全燃烧放出热量483.6kJ.
|
C
| 2NaCl+2H2O 2NaOH+H2↑+Cl2↑ 2NaOH+H2↑+Cl2↑
| NaCl氧化性比Cl2强
|
D
| FeO+4H++NO3―= Fe3++NO2↑+2H2O
| 氧化亚铁溶于稀硝酸的离子方程式
|
题号:4313629
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】在密闭容器中进行反应:X(g)+3Y(g)
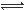
2Z(g),下列说法正确的是 ( )
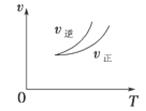
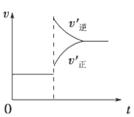
| A.左上图说明正反应为吸热反应 |
| B.反应达平衡后,增大压强气体密度将减小 |
| C.右上图可表示升高温度使平衡向逆反应方向移动 |
| D.右上图虚线可表示使用催化剂后引发的反应速率变化 |
题号:4313630
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH
4O + 3O
2 = 2CO
2↑+ 4H
2O,下图是该燃料电池的示意图。下列说法错误的是( )
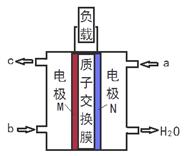
| A.燃料电池将化学能转化为电能 |
| B.a是甲醇、b是氧气 |
| C.质子从M电极区穿过交换膜移向N电极区 |
| D.负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+ |
题号:4313631
题型:选择题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】常温下,向l00mL 0.01 mol•L
-1盐酸中逐滴加入0.02 mol•L
-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是( )
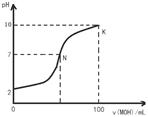
| A.MOH是弱碱 |
| B.N点c(Cl-) = c(M+) |
C.随着MOH溶液的滴加,比值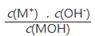 不变 不变 |
| D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol•L-1 |
题号:4313632
题型:填空题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】(15分)四种主族元素的性质或结构信息如下:
元素编号
| 相关信息
|
X
| 地壳中含量最大的金属元素;元素最高价为+3价。
|
Y
| 原子最外层电子数是电子层数的2倍,最外层电子数是X最外层电子数的2倍。
|
Z
| 同周期主族元素中原子半径最小,常温下单质呈液态。
|
M
| 能从海水中提取的金属元素,单质可在氮气或二氧化碳中燃烧。
|
(1)M的原子结构示意图是
;上述元素最高价氧化物对应的水化物碱性最强的是(写分子式)
(元素用元素符号表示,下同!)。
(2)Y单质溶于热浓的硫酸产生的气体的化学式为
。
(3)能体现Z单质比Y单质活泼性强的一个化学方程式:
。
(4)常温下,不能与X的单质持续发生反应的是(填选项序号)
。
A.CuSO
4溶液 B.Fe
2O
3 C.浓硫酸 D.NaOH溶液 E.Na
2CO
3固体
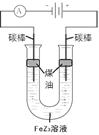
(5)铁元素与Z元素形成化合物FeZ
3,FeZ
3溶液按下图所示进行试验。装置通电后,连接电源
(填“正极”或“负极”)碳棒边的煤油颜色将变深,另一碳棒附近溶液将出现的现象是
。
题号:4313633
题型:填空题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】(15分)含铬污水处理是污染治理的重要课题。污水中铬元素以Cr
2O
72-和CrO
42-形式存在,常见除铬基本步骤是:
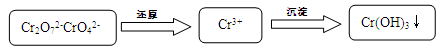
(1)加酸可以使CrO
42-转化为Cr
2O
72-: 2CrO
42- + 2H
+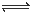
Cr
2O
72- + H
2O
若常温下pH=1溶液中Cr
2O
72-浓度为0.1 mol•L
-1,Cr
2O
72-浓度是CrO
42-浓度的10倍,该化学平衡常数K=
。
(2)六价铬的毒性大约是三价铬的100倍,二氧化硫还原法是在酸性溶液中通SO
2将Cr
2O
72-还原,反应的离子方程式为
。而后再加碱将Cr
3+沉淀,已知常温下K
sp[Cr(OH)
3] =10
-32,要使c(Cr
3+)降低到10
-5mol•L
-1,溶液的pH应升高到
。
(3)电解还原法是利用电解产生的Fe
2+将Cr
2O
72-还原为Cr
3+.电解装置所用的电极材料是碳棒和铁片,其中铁片连接直流电源的
极。
(4)Cr(OH)
3为绿色粘性沉淀,类似于Al(OH)
3既溶于酸又能溶于强碱溶液。Cr(OH)
3溶于稀硫酸的化学方程式为
。往100.00mL 0.1000 mol•L
-1CrCl
3溶液滴加1.000mol•L
-1NaOH溶液, 请画出生成沉淀的物质的量与加入NaOH溶液体积的关系图:
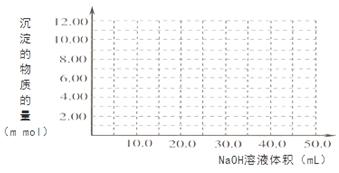
题号:4313635
题型:填空题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】(13分)(1)钠镁铝三种元素中第一电离能最大的是
。
(2)某正二价阳离子核外电子排布式为[Ar]3d
54s
0,该金属的元素符号为
。
(3)微粒间存在非极性键、配位键、氢键及范德华力的是
。
| A.NH4Cl晶体 | B.Na3AlF6晶体 | C.Na2CO3•10H2O晶体 |
| D.CuSO4溶液 E. CH3COOH溶液 |
(4)部分共价键键能数据如下表:
键
| H-H
| N-H
| N-N
| N=N
| N≡N
|
键能/kJ•mol-1
| 436
| 391
| 159
| 418
| 945
|
根据上表数据推算并写出由氮气和氢气合成氨气的热化学方程式:
。
(5)乙醇和乙醚是同分异构体,但它们性质存在差异:
| 分子式
| 结构简式
| 熔点
| 沸点
| 水溶性
|
乙醇
| C2H6O
| C2H5OH
| -114.3℃
| 78.4 °C
| 互溶
|
二甲醚
| C2H6O
| CH3OCH3
| -138.5℃
| -24.9℃
| 微溶
|
乙醇和二甲醚沸点及水溶性差异的主要原因是
。
(6)金属铜溶于在浓氨水与双氧水的混合溶液,生成深蓝色溶液。该深蓝色的浓溶液中加入乙醇可见到深蓝色晶体析出,请画出呈深蓝色的离子的结构简式
。
题号:4313634
题型:简答题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】(15分)乙醇、乙酸都是有机化工重要的基础原料。
(1).空气中,乙醇蒸气能使红热铜丝保持红热,该反应的化学方程式为
。
(2).浓硫酸催化下,乙酸和乙醇生成乙酸乙酯
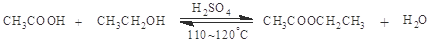
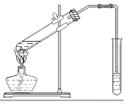
某化学兴趣小组的同学用以下装置进行该酯化反应的探究实验:
①要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是
。
②小试管中装的是浓Na
2CO
3溶液,导气管不插入液面下是为了防止
。
③相关物质的部分性质:
| 乙醇
| 乙酸
| 乙酸乙酯
|
沸点
| 78.0℃
| 117.9℃
| 77.5℃
|
水溶性
| 易溶
| 易溶
| 难溶
|
根据上表数据有同学提出可用水替代小试管中的Na
2CO
3溶液,你认为可行吗?说明理由:
。④分离小试管中的乙酸乙酯应使用的仪器名称是
;
⑤分离时,乙酸乙酯应该从仪器
(填“下口放” 或“上口倒出”)。
⑥兴趣小组多次试验后,测出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
实验序号
| 乙醇(mL)
| 乙酸(mL)
| 乙酸乙酯(mL)
|
a
| 2
| 2
| 1.33
|
b
| 3
| 2
| 1.57
|
c
| 4
| 2
| X
|
d
| 5
| 2
| 1.76
|
e
| 2
| 3
| 1.55
|
表中数据X的范围是
;实验a与实验e探究的目的是
。
题号:4313636
题型:推断题
难易度:一般
日期:2014-06-03
来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(带解析)
【题文】(13分)(1).PET是应用广泛的五大工程塑料之一,PET结构片段:
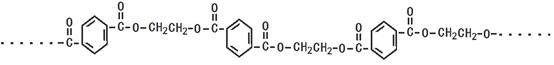
①PET由两种有机物通过缩聚反应生成,其中分子较大的单体分子结构简式为
,分子较小的单体含氧官能团名称是
。
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子。该反应的化学方程式为:
。
(2).水杨酸(邻羟基苯甲酸)是合成阿司匹林(
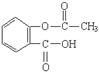
)的原料。
①水杨酸与乙酸酐(
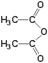
)反应生成阿司匹林的化学方程式:
。
②写出一种阿司匹林同分异构体的结构式
,该同分异构体符合以下条件:
a.芳香族化合物;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种。
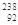 U3+
U3+ 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑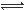 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )



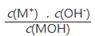 不变
不变

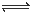 Cr2O72- + H2O
Cr2O72- + H2O
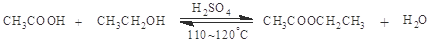


 )的原料。
)的原料。 )反应生成阿司匹林的化学方程式: 。
)反应生成阿司匹林的化学方程式: 。