适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2014年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2014年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2014年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2014年')}} 上传日期:2014-12-01 题数:29
题号:3228527
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】设N
A 为阿伏加德罗常数,下列叙述正确的是( )
A.1mol铁与足量盐酸完全反应转移的电子数目为3NA B.28 g乙烯和环丁烷(C4 H8 )的混合气体中含有的碳原子数为2NA C.100mL 1mol/L FeCl3 溶液中含有Fe3+ 为0.1NA D.32g氧气和32g臭氧(O3 )所含有的氧原子数之比为2:3
题号:3228528
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】 在8NH
3 + 3Cl
2 = N
2 + 6NH
4 Cl反应中,被氧化的原子与被还原的原子的物质的量之比为
题号:3228529
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】对于反应KClO
3 + HCl = KC1 + Cl
2 ↑+ H
2 O(未配平)若有0.1 mol KClO
3 参加反应,下列说法正确的是 ( )
A.转移0.5 mol电子 B.生成0.1 mol Cl2 C.被氧化的HC1为0.6 mol D.Cl2 是只是氧化产物不是还原产物
题号:3228530
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】将0.5 mol Na和0.5 mol Mg分别投入到过量的m
1 g水和m
2 g盐酸中,分别得到溶液a和b,若m
1 = m
2 ,则a和b的质量关系是 ( )
题号:3228531
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列有关实验原理或操作正确的是 ( )
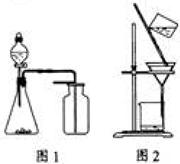
A.选择合适的试剂,用图1所示装置可分别制取收集少量CO2 、NO、O2 B.配制FeSO4 溶液时,一般加一定量稀硫酸和足量铁粉,并且现配现用 C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干 D.用干燥的pH试纸可测得新制氯水的pH="2"
题号:3228532
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列各组试剂中,只用试管和胶头滴管,不用其他试剂就可以鉴别的是( )
A.NaHSO4 溶液和Na2 CO3 溶液 B.稀盐酸和AgNO3 溶液 C.AlCl3 溶液和NH3 ·H2 O溶液 D.Ba(OH)2 溶液和NaHCO3 溶液
题号:3228533
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】能正确表示下列反应的离子方程式是 ( )
A.向氢氧化钠溶液中通入Cl2 :Cl2 + 2OH- = Cl- +ClO- +H2 O B.向次氯酸钙溶液通入SO2 :Ca2+ +2ClO- +H2 O+SO2 =CaSO3 ↓+2HClO C.氢氧化钡溶液与硫酸溶液反应:Ba2+ +SO4 2 - =BaSO4 ↓ D.高锰酸钾溶液与浓盐酸混合:2MnO4 - +2Cl- +16H+ =2Mn2+ +Cl2 ↑+8H2 O
题号:3228534
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
题号:3228535
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列实验现象的描述正确的是
A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾 B.氧化铁溶于水生成红褐色沉淀 C.铜在氯气中燃烧,产生棕黄色烟 D.钠在空气中燃烧,发出黄色的火焰,生成白色固体
题号:3228536
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】根据世界环保联盟的要求ClO
2 将逐渐取代Cl
2 成为生产自来水的消毒剂。工业上ClO
2 常用NaClO
3 和Na
2 SO
3 溶液混合并加H
2 SO
4 酸化后反应制得,在以上反应中NaClO
3 和Na
2 SO
3 的物质的量之比为 ( )
题号:3228537
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】能正确表示下列化学反应的离子方程式是 ( )
A.过量的NaHSO4 与Ba(OH)2 溶液反应:Ba2 + +2OH- +2H+ +SO4 2 - =BaSO4 ↓+2H2 O B.硫酸镁溶液跟氢氧化钡溶液反应:SO4 2 - +Ba2 + =BaSO4 ↓ C.NH4 HCO3 溶液与过量NaOH溶液反应:NH4 + +OH- =NH3 ↑+H2 O D.向碳酸氢钠溶液中滴加少量稀硝酸:CO3 2 - + 2H + = CO2 + H2 O
题号:3228538
题型:选择题
难易度:较易
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】向FeCl
3 和BaCl
2 的酸性混合溶液中,通入SO
2 气体,有白色沉淀生成。此沉淀是( )
题号:3228539
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】某溶液中Cl
- 、Br
- 、I
- 三者物质的量之比是1:2:3,通入一定量的Cl
2 ,当反应完全后,该比值变为3:2:1,则反应的Cl
2 和原溶液中I
- 的物质的量之比是( )
题号:3228540
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】将0.2molMnO
2 和50mLl2mol·L
-1 盐酸混合后缓缓加热,反应完全后向留下的溶液中加入足量AgNO
3 溶液,生成AgCl沉淀物质的量为( )(不考虑盐酸的挥发)
A.等于0.3 mol B.小于0.3mol C.大于0.3mol、小于0.6mol D.以上结论都不正确
题号:3228541
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】某溶液仅含Fe
2+ 、Na
+ 、Al
3+ 、Ba
2+ 、SO
4 2- 、NO
3 - 、Cl
- 中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是( )
A.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 C.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 D.该溶液中所含的离子是:Fe2+ 、Na+ 、SO4 2- 、NO3 -
题号:3228542
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列各说法正确的是
A.弱电解质的导电能力一定比强电解质的导电能力弱 B.pH=4的醋酸与pH=10的NaOH溶液等体积混合后溶液显碱性 C.豆浆中加入硫酸钙会使蛋白质聚沉. D.同浓度①NaHCO3 、②Na2 CO3 、③CH3 COONa四种溶液,pH大小顺序是②>③>①
题号:3228543
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列实验过程中,始终无明显现象的是( )
A.CO2 通入饱和Na2 CO3 溶液中 B.CO2 通入CaCl2 溶液中 C.NH3 通入AlCl3 溶液中 D.SO2 通入已酸化的Ba(NO3 )2 溶液中
题号:3228544
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列有关实验的叙述正确的是( )
A.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液 B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 D.读取滴定管内液体的体积,俯视读数导致读数偏小
题号:4310366
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】下列现象或变化过程与胶体的性质无关的是 ( )
A.清晨森林中的道道光柱 B.夕阳下的晚霞 C.海水的淡化 D.明矾净水
题号:4310367
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】市场上销售的“84”消毒液,其商品标识上有如下叙述:①本品为无色液体,呈碱性②使用时加水稀释③可对餐具、衣物进行消毒,可漂白浅色衣物。其有效成分可能是( )
A.Cl2 B.SO2 C.NaClO D.KMn04
题号:4310368
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】把500 mL含有BaCl
2 和KCl的混合溶液分成5等份,取一份加入含a mol 硫酸钠的溶液恰好使钡离子完全沉淀;另取一份加入含b mol 硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为( )
A.0.1 ( b – 2a ) mol/L B.10 ( 2a – b ) mol/L C.10 ( b – a ) mol/L D.10 ( b – 2a ) mol/L
题号:4310369
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
⑴Cl
2 +2KI=2KCl+I
2 ; ⑵2FeCl
2 +Cl
2 =2FeCl
3 ;
⑶2FeCl
3 +2HI=2FeCl
2 +2HCl+I
2 ,⑷H
2 S+I
2 =S+2HI;
A.S>I2 >Fe3 + >Cl2 B.Cl2 >Fe3 + >I2 >S C.Fe3 + >Cl2 >S>I2 D.Cl2 >I2 >Fe3 + >S
题号:4310370
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】在强酸性溶液中能大量共存的无色透明离子组是 ( )
A.K+ 、Na+ 、NO3 - 、MnO4 - B.Mg2+ 、Na+ 、Cl- 、SO4 2 - C.K+ 、Na+ 、Br- 、Cu2+ D.Na+ 、Ba2+ 、OH- 、SO4 2 -
题号:4310371
题型:选择题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】同温同压下,相同体积的CO和CO
2 ,下列比较中正确的是( )
①所含的分子数目之比为1︰1 ②所含的O原子数目之比为1︰2
③所含的原子总数目之比为2︰3 ④两者的密度之比为:7:11
⑤所含的电子数目之比为7︰11
题号:3228523
题型:实验题
难易度:较难
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】(13分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量,请填写下列空白:
移取10.00 ml密度为ρ g/mL的过氧化氢溶液至烧杯后全部将其转移到250 ml
(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
(3)滴定时,将高锰酸钾标准溶液注入
(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是
。
(4)复滴定三次,平均耗用c mol/L KMnO
4 标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为
。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表:
实 验 内 容 实 验 方 法 实 验 现 象 验证氧化性 验证不稳定性
题号:3228524
题型:实验题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】(10分)实验室常用的几种气体发生装置如图A、B、C所示:
A B C D
(1)实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是
。
(2)气体的性质是气体收集方法选择的主要依据。下列性质与收集方法无关的是
(填序号,下同。)①密度 ②颜色 ③溶解性 ④热稳定性
下图是某学生设计收集气体的几种装置,其中不可行的是
。
(3)若用A装置与D装置相连制取收集X气体,则X可能是下列气体中的_______,
①CO
2 ② NO ③ Cl
2 ④H
2 其中在D装置中连接小烧杯的目的是________________________。
题号:3228525
题型:实验题
难易度:较难
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】(13分) 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程:
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为______________________________________。
(2)混合①中使用冰水的目的是___________
______________________。
(3)操作Ⅱ和Ⅲ的名称分别是________、__________。操作Ⅲ一般适用于分离_______混合物(选填编号)。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中加入Na
2 SO
3 的目的是____________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)常带有淡淡的黄色。 于是甲、乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe
3 + ,则用于证明该假设所用的试剂为____________,若假设成立可观察到的现象为____________________________。乙同学假设工业氢溴酸呈淡黄色是因为_____________________________,其用于证明该假设所用的试剂为______________。
题号:3228522
题型:填空题
难易度:较易
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】(6分)开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH
4 )
3 是一种储氢材料,可由TiCl
4 和LiBH
4 反应制得。
①基态Ti
3+ 的未成对电子数有______个。
②LiBH
4 由Li
+ 和BH
4 - 构成,BH
4 - 呈正四面体构型。LiBH
4 中不存在的作用力有______(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为______。
(2) 金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li
+ ______H
- (填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是______(填元素符号)。
(3)某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有______种。
题号:3228526
题型:填空题
难易度:一般
日期:2014-12-01
来源:2015届福建省清流县第一中学高三上学期第一次阶段考试化学试卷(带解析)
【题文】(10分)填写下列空白:4 在熔融状态下的的电离方程式为: ;4 溶液中滴入Ba(OH)2 溶液至中性,其离子方程式为 ;3 溶液中加过量的Ba(OH)2 溶液 ,其离子方程式为 ___ ___ __ 2 溶液中通入过量的CO2 ,其离子方程式为 __________ _____
 白色沉淀
白色沉淀 沉淀不溶解 结论:试液中一定含SO42-
沉淀不溶解 结论:试液中一定含SO42- 无色气体
无色气体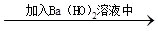 白色沉淀结论:原气体一定是CO
白色沉淀结论:原气体一定是CO 冒白雾
冒白雾 白烟
白烟 变红色结论:原溶液中一定含Fe3+
变红色结论:原溶液中一定含Fe3+




