适用年级:{{getGradeNameByProperty('高二|月考试卷|福建|2016年')}} 试卷类型:{{getTestPaperTypeName('高二|月考试卷|福建|2016年')}} 使用省份:{{getAreaName('高二|月考试卷|福建|2016年')}}
试卷年份:{{getYear('高二|月考试卷|福建|2016年')}}上传日期:2017-01-11题数:21
提示:单击题文可显示答案与解析。
题号:4736701
题型:选择题
难易度:容易
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】下列说法正确的是( )
| A.NH3溶于水溶液能导电,所以NH3是电解质 |
| B.钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+ |
| C.等量的氢气和氧气分别完全燃烧生成气态水和液态水,前者放出的热量多 |
| D.H2(g)+F2(g)==="2HF(g)" ΔH=-271 kJ·mol-1,ΔS=+8 J·mol-1·K-1,该反应在任意温度下都能自发进行 |
题号:4736702
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】能用勒夏特列原理解释的是( )
| A.煅烧粉碎的硫铁矿有利于SO2生成 |
| B.由H2、I2、HI三种气体组成的平衡体系加压后颜色变深 |
| C.使用铁触媒,使N2和H2的混合气体有利于合成NH3 |
| D.实验室常用排饱和和食盐水法收集Cl2 |
题号:4736703
题型:选择题
难易度:容易
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】为探究锌与稀硫酸的反应速率(以v(H
2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A.加入Na2SO4固体,v(H2)增大 | B.加入NaHSO4固体,v(H2)不变 |
| C.加入CH3COONa固体,v(H2)减小 | D.滴加少量CuSO4溶液,v(H2)减小 |
题号:4736704
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】下列事实不能证明甲酸(HCOOH,一元酸)为弱酸的是( )
| A.0.1mol/L甲酸的pH为2.3 |
| B.将pH=2的甲酸稀释100倍后,溶液的pH小于4 |
| C.温度升高,溶液的导电能力增强 |
| D.等体积等浓度的甲酸和HCl与足量的锌反应,产生等量的氢气 |
题号:4736705
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】已知CO
2(g)+CH
4(g)

2CO(g)+2H
2(g),达到平衡,若其它条件不变,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法不正确的是( )
| A.正、逆反应速率都加快 | B.氢气的浓度与原平衡比减少 |
| C.甲烷的物质的量增加 | D.重新平衡时c(CO2) /c(CO)增大 |
题号:4736706
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确是( )
①生成物的质量分数一定增加
②生成物的产量一定增大
③反应物的转化率一定增大
④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率
⑥平衡常数一定增大
题号:4736707
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
题号:4736708
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】全钒电池以惰性材料做电解,在电解质溶液中发生的总反应式为:
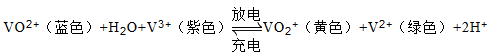
下列说法正确的是( )
| A.当电池放电时,VO2+离子被氧化 |
| B.放电时,负极反应为:VO2+ +2H+ +2e- =VO2+ +H2O |
| C.充电时,阳极附近溶液由绿色逐渐变为紫色 |
| D.放电过程中,正极附近溶液的pH变大 |
题号:4736709
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】COCl
2 (g)

CO(g)+Cl
2 (g) △H>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④加催化剂 ⑤恒压通入惰性气体,能提高COCl
2转化率的是( )
题号:4736710
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】已知反应2SO
2(g)+O
2(g)

2SO
3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO
2和O
2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )

| A.O2的体积分数 | B.SO2的转化率 |
| C.密闭容器内的压强 | D.混合气体的密度 |
题号:4736711
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】观察下列几个装置示意图,有关叙述正确的是( )
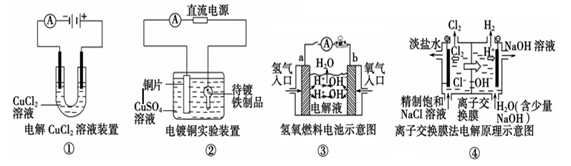
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③中闭合开关后,外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
题号:4736712
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】水的电离平衡为H
2O

H
+﹢OH
-,△H>0,下列叙述不正确的是( )
| A.将水加热,pH减小 |
| B.恒温下,向水中加入少量固体KOH,Kw不变 |
| C.向水中滴入稀醋酸,c(H+)增大 |
| D.向水中加入少量固体NaClO,平衡逆向移动 |
题号:4736713
题型:选择题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】将2molSO
2和1molO
2分别置于相同体积的甲乙两密闭容器中发生反应2SO
2+O
2(g)

2SO
3(g),并达到平衡。在这过程中,甲容器保持恒温恒容,乙容器保持恒温恒压,达到平衡时,下列说法正确的是( )
| A.达到平衡所需的时间为:甲>乙 | B.甲的转化率>乙的转化率 |
| C.混合气体中SO3的含量为:甲>乙 | D.气体的总物质的量:甲<乙 |
题号:4736714
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】室温下,下列有关两种溶液的说法不正确的是( )
A. ①②两溶液中c(OH
-)相等
B. ①溶液的物质的量浓度为0.01mol·L
-1C. ①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>②
D. 等体积的①②两溶液分别与0.01mol·L
-1的盐酸完全中和,消耗盐酸的体积:①>②
题号:4736715
题型:选择题
难易度:一般
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】下图所示原电池工作时,右池中Y
2O
72-转化为Y
3+。下列叙述正确的是( )
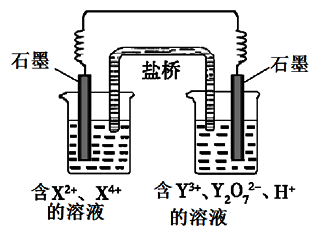
| A.左池电极反应式:X4+ + 2e- = X2+ |
| B.每消耗1mol Y2O72-,转移3mol电子 |
| C.左池中阴离子数目增加 |
| D.在工作中,电流的方向:左池→导线→右池 |
题号:4736716
题型:选择题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】反应N
2O
4(g)
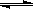
2NO
2(g) ΔH=+57kJ·mol
-1,在温度为T
1、T
2时,平衡体系中NO
2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
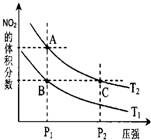
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
题号:4736719
题型:实验题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】已知将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生。若再加入双氧水,将发生反应H
2O
2+2H
++2I
-═2H
2O+I
2,且生成I
2立即与试剂X反应而被消耗.一段时间后,试剂X将被反应生成I
2完全消耗.由于溶液中I
-继续被H
2O
2氧化,生成I
2与淀粉作用,溶液立即变蓝.因此,根据试剂X量、滴入双氧水至溶液变蓝所需时间,即可推算反应H
2O
2+2H
++2I
-═2H
2O+I
2反应速率。下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
编号
| 往烧杯中加入的试剂及其用量(mL)
| 催化剂
| 溶液开始变蓝时间(min)
|
0.1mol·L-1
KI溶液
| H2O
| 0.01mol·L-1
X溶液
| 0.1mol·L-1
双氧水
| 0.1mol·L-1
稀盐酸
|
1
| 20.0
| 10.0
| 10.0
| 20.0
| 20.0
| 无
| 1.4
|
2
| 20.0
| m
| 10.0
| 10.0
| n
| 无
| 2.8
|
3
| 10.0
| 20.0
| 10.0
| 20.0
| 20.0
| 无
| 2.8
|
4
| 20.0
| 0
| 10.0
| 10.0
| 40.0
| 无
| t
|
5
| 20.0
| 10.0
| 10.0
| 20.0
| 20.0
| 5滴Fe2(SO4)3
| 0.6
|
回答下列问题:
(1)已知:实验1、2的目的是探究H
2O
2浓度对H
2O
2+2H
++2I
-═2H
2O+I
2反应速率的影响。
实验2中m=
,n=
。
(2)一定温度下,H
2O
2+2H
++2I
-═2H
2O+I
2,反应速率可以表示为v=k·c
a(H
2O
2)·c
b (I
-)·c(H
+)(k为反应速率常数),则:
①实验4时,烧杯中溶液开始变蓝的时间t=__________min;
②根据上表数据可知,a、b的值依次为
和
。
(3)若要探究温度对H
2O
2+2H
++2I
-=2H
2O+I
2反应速率影响,在实验中温度不宜过高且采用水浴加热,其原因是
。
题号:1208420
题型:填空题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】化学在能源开发与利用中起到十分关键的作用。甲烷是一种新型的绿色能源,又是一种重要的化工原料。甲烷燃料电池能量转化率高,具有广阔的发展前景,现用甲烷燃料电池进行如图实验(图中所用电极均为惰性电极)
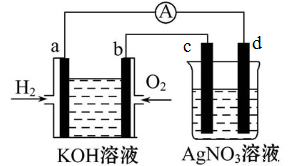
(1)电极b为______________极,溶液中OH
-移向_____________极(填a或b);
(2)电极a处所发生的电极反应方程式为
;
(3)乙装置所发生的总反应方程式
;
(4)如图装置中盛有100mL0.2mol•L
-1AgNO
3溶液,当氢氧燃料电池中消耗氧气56mL(标准状况下)时,则此时右图装置中溶液的pH=__________(溶液体积变化忽略不计),d极增重
g。
题号:1208421
题型:填空题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液
(1)实验测得0.1 mol·L-1一元弱酸HA 的pH为4,则HA的电离平衡常数Ka= ;
(2)0.1mol·L-1的H2SO4中水电离出的C(H+)为 ;
(3)向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为 ;
(4)向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是 ;
①c(H+) ② 电离度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
题号:4736717
题型:填空题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】I.已知:P
4(白磷)+3O
2(g)= P
4O
6(g)的反应热△H=-1638 kJ·mol
-1,白磷和P
4O
6的分子结构如图所示,化学键的键能(kJ·mol
-1):P—P:198 P—O:360,则断开1molO
2所需要的能量为
kJ
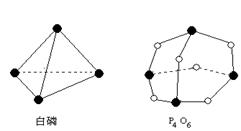
II.已知:①CO(g)+1/2O
2(g)=CO
2(g) △H=-141kJ·mol
-1②2H
2(g)+O
2(g)=2H
2O(g) △H=-484kJ·mol
-1③CH
3OH(g)+3/2O
2(g)=CO
2(g)+2H
2O(g) △H=-883kJ·mol
-1(1)利用CO、H
2化合制得1mol气态甲醇的热化学方程式为
;
(2)若在恒温2L密闭容器中,将1molCO与3mol H
2充分反应,当吸收能量为129KJ时,此时H
2的转化率为
,平衡常数为
。
题号:4736718
题型:填空题
难易度:较难
日期:2017-01-09
来源:2016-2017学年福建省四地六校高二上学期12月月考化学试卷(带解析)
【题文】700℃时,向容积为2L的密闭容器中充入一定量的CO和H
2O,发生反应:
CO(g)+H
2O(g)

CO
2(g)+H
2(g)反应过程中测定的部分数据见下表(表中t
2>t
1):
反应时间/min
| n(CO)/mol
| n(H2O)/ mol
|
0
| 1.20
| 0.60
|
t1
|
| 0.20
|
t2
| 0.80
|
|
依据题意回答下列问题:
(1)反应在t
1min内的平均速率为v(H
2)=
mol·L
-1·min
-1(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH
2O,到达平衡时,n(CO
2)=
mol。
(3)温度升至800℃,上述反应平衡常数为0.64,则正反应为
反应(填“放热”或“吸热”)。
(4)700℃时,向容积2L的密闭容器中充入CO(g)、H
2O(g)、CO
2(g)、H
2(g)的物质的量分别为1.20mol、2.00mol、1.20mol、1.20mol,则此时该反应v(正)
v(逆)(填“>”、“<”或“=”)。
(5)该反应在t
1时刻达到平衡、在t
2时刻因改变某个条件浓度发生变化的情况:图中t
2时刻发生改变的条件是
、
(写出两种)。

(6)若该容器体积不变,能判断反应达到平衡的是
。
①c(CO)与c(H
2)的比值保持不变
②v(CO
2)
正=v(H
2O)
逆③体系的压强不再发生变化
④混合气体的密度不变
⑤体系的温度不再发生变化
⑥气体的平均相对分子质量不变
 2CO(g)+2H2(g),达到平衡,若其它条件不变,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法不正确的是( )
2CO(g)+2H2(g),达到平衡,若其它条件不变,将体积压缩至原来的1/2,达到新的平衡后,下列有关该体系的说法不正确的是( )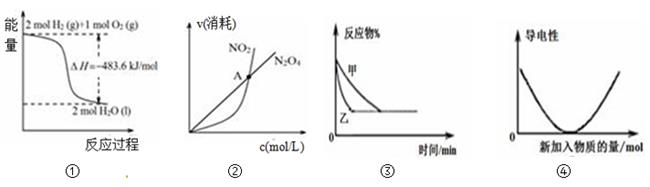
 N2O4(g),A点为平衡状态
N2O4(g),A点为平衡状态 3C(g)+D(s)的影响
3C(g)+D(s)的影响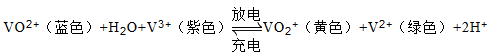
 CO(g)+Cl2 (g) △H>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④加催化剂 ⑤恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2 (g) △H>0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO 的浓度 ④加催化剂 ⑤恒压通入惰性气体,能提高COCl2转化率的是( ) 2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )
2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是( )

 H+﹢OH-,△H>0,下列叙述不正确的是( )
H+﹢OH-,△H>0,下列叙述不正确的是( ) 2SO3(g),并达到平衡。在这过程中,甲容器保持恒温恒容,乙容器保持恒温恒压,达到平衡时,下列说法正确的是( )
2SO3(g),并达到平衡。在这过程中,甲容器保持恒温恒容,乙容器保持恒温恒压,达到平衡时,下列说法正确的是( )
 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )


 CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t2>t1):