适用年级:{{getGradeNameByProperty('高三|月考试卷|福建|2013年')}} 试卷类型:{{getTestPaperTypeName('高三|月考试卷|福建|2013年')}} 使用省份:{{getAreaName('高三|月考试卷|福建|2013年')}}
试卷年份:{{getYear('高三|月考试卷|福建|2013年')}}上传日期:2014-01-09题数:19
提示:单击题文可显示答案与解析。
题号:3257980
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】某兴趣小组为探究外界条件对可逆反应A(g)+B(g)

C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
针对上述系列实验,下列结论中错误的是( )
| A
| B
| C
|
Ⅰ
| 0.050mol·L-1
| 0.050mol·L-1
| 0.050mol·L-1
|
Ⅱ
| 0.070mol·L-1
| 0.070mol·L-1
| 0.098mol·L-1
|
Ⅲ
| 0.060mol·L-1
| 0.060mol·L-1
| 0.040mol·L-1
|
Ⅳ
| 0.080mol·L-1
| 0.080mol·L-1
| 0.12mol·L-1
|
A.由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol
-1·L
B.Ⅱ可能是通过增大C的浓度实现的
C.若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应
D.第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现
题号:3257981
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】按如图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
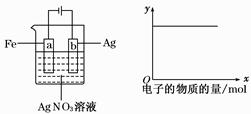
①c(Ag
+) ②c(AgNO
3) ③a棒的质量 ④b棒的质量 ⑤溶液的pH
题号:3257983
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】已知:①H
+(aq)+OH
-(aq)=H
2O(l);ΔH
1;②2SO
2(g)+O
2(g)

2SO
3(g);ΔH
2。其他条件不变时,增加反应物的量,则下列判断正确的是( )
| A.ΔH1增大,ΔH2减小 | B.ΔH1增大,ΔH2增大 |
| C.ΔH1减小,ΔH2减小 | D.ΔH1不变,ΔH2不变 |
题号:3257984
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】如图为用惰性电极电解CuCl
2溶液并验证其产物的实验装置,则下列说法不正确的是( )
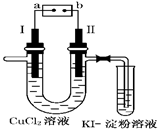
| A.电源a极为负极 |
| B.KI—淀粉溶液会变蓝色 |
| C.若加入适量CuCl2可使电解后的溶液恢复原状态 |
| D.电极Ⅰ上发生的电极反应为:Cu-2e-=Cu2+ |
题号:3257985
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
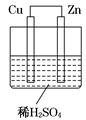
卡片号:2 2013.3.15,实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生
③SO42– 向Cu极移动
④ 若有0.5mol电子流经导线,则可产生0.25mol气体
⑤ 电子的流向是:Cu→Zn
⑥正极反应式:Cu +2e- = Cu2+
|
A.①②③ B.②④ C.④⑤⑥ D.③④⑤
题号:3257986
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
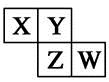
| A.X的最常见气态氢化物的水溶液显酸性 |
| B.最高价氧化物对应水化物的酸性W比Z强 |
| C.Z的单质与氢气反应较W剧烈 |
| D.X的原子半径小于Y |
题号:3257987
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】根据下表信息,判断以下叙述正确的是( )
短周期元素代号
| L
| M
| Q
| R
| T
|
原子半径/nm
| 0.160
| 0.143
| 0.112
| 0.104
| 0.066
|
主要化合价
| +2
| +3
| +2
| +6、-2
| -2
|
A.M与T形成的化合物具有两性
B.单质与稀盐酸反应的速率为L<Q
C.氢化物的热稳定性为H
2T<H
2R
D.氢化物的沸点为H
2T<H
2R
题号:3257988
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】下列有关热化学方程式的叙述正确的是( )
| A.在稀溶液中:H+(aq)及+OH-(aq) = H2O(l) ΔH=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.需要加热的反应说明它是吸热反应 |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2,则ΔH1>ΔH2 |
题号:3257989
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】下列有关说法正确的是(N
A为阿伏加德罗常数) ( )
| A.工业上粗铜的电解精炼时,每转移1mol电子时阳极上溶解的铜小于0.5NA |
| B.1.12L Cl2含有1.7NA个质子 |
| C.1mol NaHSO4固体中含阴阳离子数为3NA |
| D.将1mol NO2气体在降温后颜色变浅,但其所含的分子数仍然为NA |
题号:3257990
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
题号:3257991
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】下列叙述
不正确的是( )
| A.铁表面镀锌,锌作阳极 |
| B.船底镶嵌锌块,锌作正极,以防船体被腐蚀 |
| C.钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-=4OH- |
| D.工业上电解饱和食盐水的 |
题号:3257992
题型:选择题
难易度:较易
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】下列设备工作时,将化学能转化为电能的是( )

题号:4318170
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
题号:4318171
题型:选择题
难易度:较难
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16。A、B、C为常见的化合物,X、Y、Z三种元素的常见单质在适当条件下可发生右图所示变化,其中B和C均为10电子分子。下列说法不正确的是( )
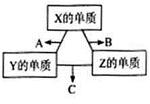
A.X元素位于ⅥA B.A不能溶解于B中
C.A和C不可能发生氧化还原反应 D.B的沸点高于C的沸点
题号:4318172
题型:选择题
难易度:一般
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】如图所示是298 K时N
2与H
2反应过程中能量变化的曲线图。下列叙述正确的是( )

A.该反应的热化学方程式为:N2+3H2 2NH3 ΔH=-92 kJ/mol 2NH3 ΔH=-92 kJ/mol |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
题号:3257976
题型:填空题
难易度:困难
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】 “富煤、贫油、少气”是我国能源发展面临的现状。随着能源的日益紧张,发展“煤化工”对我国能源结构的调整具有重要意义。下图是煤化工产业链之一。
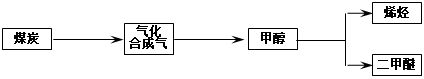
“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出热值很高的煤炭合成气,其主要成分是CO和H
2。CO和H
2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O
2(g)=CO
2(g) ΔH
1=-393.5 kJ·mol
–1 ①
C(s)+H
2O(g)=CO(g)+H
2(g) ΔH
2=+131.3 kJ·mol
–1 ②
则反应CO(g)+H
2(g) +O
2(g)= H
2O(g)+CO
2(g),ΔH= _________kJ·mol
–1。在标准状况下,33.6 L的煤炭合成气(设全部为CO和H
2)与氧气完全反应生成CO
2和H
2O,反应中转移______mole
-。
(2)在一恒容的密闭容器中,由CO和H
2合成甲醇:CO(g)+2H
2(g)

CH
3OH(g)
①下列情形能说明上述反应已达到平衡状态的是_______
a.体系压强保持不变
b.密闭容器中CO、H
2、CH
3OH(g)3种气体共存
c.CH
3OH与H
2物质的量之比为1:2
d.每消耗1 mol CO的同时生成2molH
2②CO的平衡转化率(α)与温度、压强的关系如图所示。
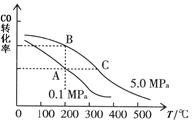
A、B两点的平衡常数_____(填“前者”、“后者”或“一样”)大;达到A、C两点的平衡状态所需的时间t
A t
C(填“大于”、“小于”或“等于”)。
在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是_____________(答出两点即可)。
(3)工作温度650℃的熔融盐燃料电池,是用煤炭气(CO、H
2)作负极燃气,空气与CO
2的混合气体为正极燃气,用一定比例的Li
2CO
3和Na
2CO
3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的。负极的电极反应式为:CO + H
2-4e
- + 2CO
32-= 3CO
2+H
2O;则该电池的正极反应式为____________。
题号:3257977
题型:填空题
难易度:困难
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】(1)R
+与S
2–所含电子数相同,则R元素的原子序数为
(2)一种基于酸性燃料电池原理设计的酒精检测仪,正极上的反应为:O
2 + 4e
– + 4H
+ = 2H
2O,检测有酒精时,电解质溶液中的H
+向
极移动,该电池负极上的反应为:
(3)X、Y、Z、M、G五种分属三个短周期主族元素,且原子序数依次增大。Z存在质量数为23,中子数为12的核素A;Y、M同主族,可形成MY
2、MY
3两种分子。
回答下列问题:
①用化学符号表示核素A:
;
②上述元素的最高价氧化物对应的水化物酸性最强的是
(写化学式),写出该物质与氢氧化钠溶液反应的离子方程式:
;
③X
2M的电子式为
;
④ZG用途广泛,下列说法正确的是:
。
A.作调味剂
| B.用于食物防腐
| C.用于氯碱工业
| D.用于医疗
|
题号:3257978
题型:填空题
难易度:困难
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】(12分)
Ⅰ.短周期元素组成的单质X
2、Y,标准状况下X
2的密度为3.17g·L
-1;常温下,Y为浅黄色固体。Z是一种化合物,焰色反应呈浅紫色(透过钴玻璃);0.1mol·L
-1Z的水溶液pH=13。X
2、Y 和Z之间有如下转化关系(其他无关物质已略去)
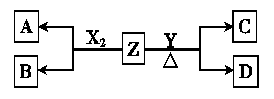

(1)写出常温下单质X
2与Z反应的离子方程式
(2)已知C能与硫酸反应生成能使品红溶液褪色的气体
①D的化学式是
;D的水溶液pH>7,原因是(用离子方程式表示)
②将20mL 0.5mol·L
-1 C溶液逐滴加入到20 mL 0.2mol·L
-1KMnO
4溶液(硫酸酸化)中,溶液恰好褪为无色。写出反应的离子方程式
Ⅱ.下表是元素周期表的一部分,表中所列的字母分别代表某一元素.
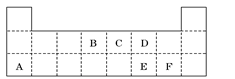
某种金属元素的单质G,可以发生如下图所示转化:

其中化合物M是一种白色胶状沉淀;K的溶液与过量B的某种氧化物反应的化学方程式为___________________________;一种新型无机非金属材料由G元素和C元素组成,其化学式为
。
题号:3257979
题型:填空题
难易度:较难
日期:2014-01-09
来源:2014届福建省四地六校高三上学期第三次月考化学试卷(带解析)
【题文】(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:


①ⅡA族元素的价电子数__________。
②第三周期元素的最高正价__________。
③F
-、Na
+、Mg
2+、Al
3+的离子半径__________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N
-、Z
+、X
+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
①化合物XN的化学式为________。
②化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液均呈碱性,组成元素的原子数目之比均为1∶1∶1,B是家庭“84”消毒液的有效成份。则化合物A中的化学键类型为__________,B的化学式为
。
③工业上制取单质M的化学方程式为
。
 C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ。然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ。
 2SO3(g);ΔH2。其他条件不变时,增加反应物的量,则下列判断正确的是( )
2SO3(g);ΔH2。其他条件不变时,增加反应物的量,则下列判断正确的是( )

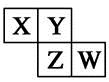
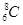

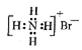

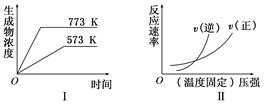
 2NH3(g) ΔH<0
2NH3(g) ΔH<0 2SO2(g) + O2(g) ΔH>0
2SO2(g) + O2(g) ΔH>0 4NO(g) + 6H2O(g) ΔH<0
4NO(g) + 6H2O(g) ΔH<0 CO(g) + H2O(g) ΔH>0
CO(g) + H2O(g) ΔH>0

 2NH3 ΔH=-92 kJ/mol
2NH3 ΔH=-92 kJ/mol
 CH3OH(g)
CH3OH(g)
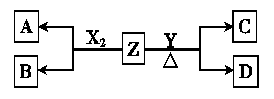
 (1)写出常温下单质X2与Z反应的离子方程式
(1)写出常温下单质X2与Z反应的离子方程式 


